Презентация на тему: Свойства электрона

Лектор Турло Евгений Михайлович Доцент кафедры химии, кандидат педагогических наук ׀-410

Консультации Четверг 15-25-18-30 д/з №3635 Методичка к лабораторным работам

Электрон имеет двойственную природу (частица и волна). Движение электрона подчиняется законам квантовой механики. Связь между волновыми и корпускулярными свойствами электрона отражает соотношение де Бройля: l =h/mv ,где l - длина волны электрона; m - его масса; v - скорость; h = 6.62Ч10-34 ДжЧс - постоянная Планка. Свойства электрона

Энергию и координаты электрона, невозможно одновременно измерить с одинаковой точностью (принцип неопределенности Гейзенберга) Часть пространства, в котором велика вероятность нахождения электрона, называют орбиталью или электронным облаком. Свойства электрона

Свойства электрона
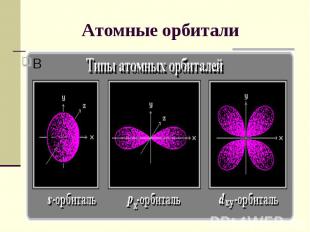
Атомные орбитали В

Квантовые числа Квантовые числа - энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится. 1. Главное квaнтовое число n определяет общую энергию электрона и степень его удаления от ядра (номер энергетического уровня); оно принимает любые целочисленные значения, начиная с 1 (n = 1, 2, 3, . . .).

Квантовые числа 2. Орбитальное (побочное) квантовое число l определяет форму атомной орбитали. Значения от 0 до n-1 (l = 0, 1, 2, 3,..., n-1). Каждому значению l соответствует орбиталь особой формы. l = 0 s-орбиталь, l = 1 - р-орбиталь, l = 2 - d-орбиталь, l = 3 - f-орбиталь

Квантовые числа 3. Магнитное квантовое число m определяет ориентацию орбитали в пространстве относительно внешнего магнитного или электрического поля. m = 2 l +1 Значения изменяются от +l до -l, включая 0. Например, при l = 1 число m принимает 3 значения: +1, 0, -1, поэтому существуют 3 типа р-АО: рx, рy, рz.

Квантовые числа 4.Спиновое квантовое число s может принимать лишь два возможных значения +1/2 и -1/2. Они соответствуют двум возможным и противоположным друг другу направлениям собственного магнитного момента электрона, называемого спином. Для обозначения электронов с различными спинами используются символы: ↑ и ↓ .

Пример орбиталей
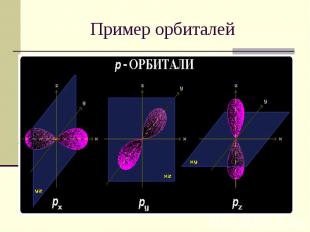
Пример орбиталей

Заполнение атомных орбиталей электронами При заполнении атомных орбиталей электронами соблюдаются три основные правила. Принцип Паули. Правило Хунда. Принцип устойчивости Клечковского.

Заполнение атомных орбиталей электронами Принцип Паули: В атоме не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковыми

Заполнение атомных орбиталей электронами Принцип Хунда: Устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня, при котором абсолютное значение суммарного спина атома максимально

Заполнение атомных орбиталей электронами Принцип устойчивости Клечковского. АО заполняются электронами в порядке повышения их энергетических уровней. В первую очередь заполняются те орбитали, у которых min сумма n+l. При равных суммах n+l заполняются те, у которых n меньше 1s < 2s < 2p < 3s < 3p < 4s < 3d ... 4s (4+0)