Презентация на тему: «Получение оксида углерода (4) и изучение его свойств.

Практическая работа № 2 «Получение оксида углерода (4) и изучение его свойств. Распознавание карбонатов» Цель работы: научиться получать и исследовать свойства оксида углерода (4). Приборы и реактивы: пробирки, стакан, раствор HCL, CaCO3, лучина, пробка с газоотводной трубкой, спички, раствор лакмуса. Директор:
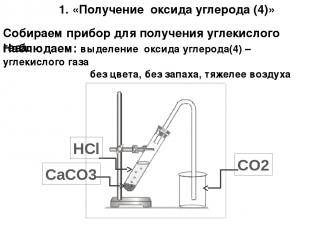
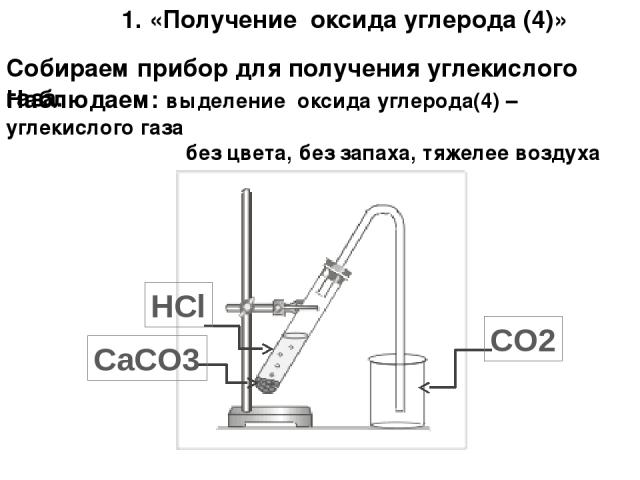
Собираем прибор для получения углекислого газа. Наблюдаем: выделение оксида углерода(4) – углекислого газа без цвета, без запаха, тяжелее воздуха 1. «Получение оксида углерода (4)» CO2 CaCO3 HCl

2. Изучение химических свойств оксида углерода (4) Горящая лучинка гаснет Наблюдаю: в оксиде углерода(4) – углекислом газе горящая лучинка гаснет Вывод: оксид углерода(4) – углекислый газ не поддерживает горение 2.1.Взаимодействие оксида углерода (4) с кислородом 2.2. Взаимодействие оксида углерода (4) с водой Наблюдаем: при пропускании углекислого газа через подкрашенную лакмусом воду - вода приобретает красный цвет, что доказывает образование кислотной среды CO2 ↑+ Н2О =Н2СО3 Угольная кислота Вывод: оксид углерода(4) – кислотный оксид при растворении в воде образует угольную кислоту СО2

Вывод по практической работе: - CO2 - кислотный оксид, при растворении в воде образует угольную кислоту; CO2 не поддерживает горения, горящая лучина гаснет в углекислом газе, качественной реакцией на CO32- является взаимодействие с кислотой. 3. Качественная реакция на соли угольной кислоты - карбонаты. CO32- + 2Н+ =Н2О+СО2↑ Наблюдаем: при взаимодействии раствора карбоната натрия с раствором кислоты выделяется углекислый газ CaCO3+ 2НCl =Н2О+СО2↑ + CaCl2 Вывод: для распознавания солей угольной кислоты необходимо провести реакцию с кислотой.

Взаимодействие оксида углерода (4) с гидроксидом натрия CO2 ↑+ 2NaOН=Na2СО3+Н2О Наблюдаю: при пропускании через подкрашенный фенолфталеином раствор гидроксида натрия углекислого газа происходит химическая реакция и малиновая окраска фенолфталеина исчезает Вывод: оксид углерода(4) – кислотный оксид вступает в реакцию со щелочами. Взаимодействие оксида углерода (4) с известковой водой - гидроксидом кальция. Качественная реакция на углекислый газ. CO2 ↑+ Ca(OН)2=CaСО3↓+Н2О Наблюдаю: при пропускании углекислого газа через известковую воду известковая вода мутнеет из-за выпавшего в осадок карбоната кальция