Презентация на тему: Общие свойства металлов

Общие свойства металлов МАОУ Домодедовский лицей №3 Разинькова Н.М.

Цель: обобщить знания учащихся об основных свойствах элементов-металлов и образуемых ими простых и сложных веществ. Задачи: Развитие умения записывать уравнения реакций в молекулярном и окислительно-восстановительном виде; проводить сравнения, делать выводы, обобщения; формировать мировоззренческие понятия о познаваемости природы.
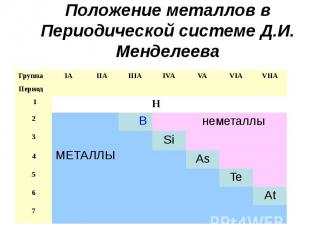
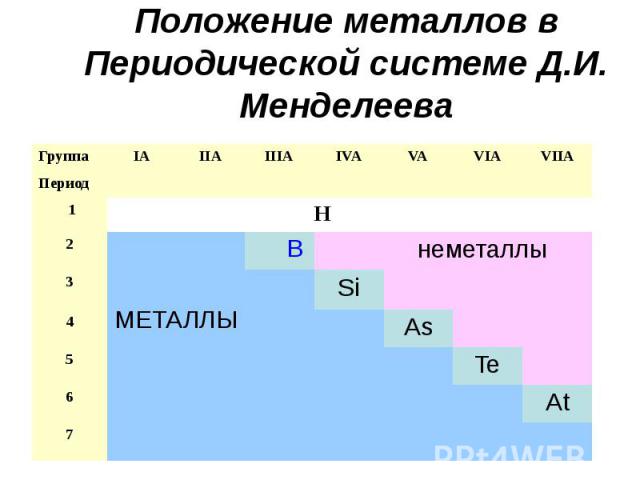
Положение металлов в Периодической системе Д.И. Менделеева
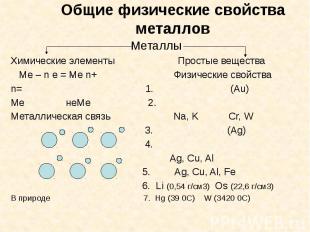
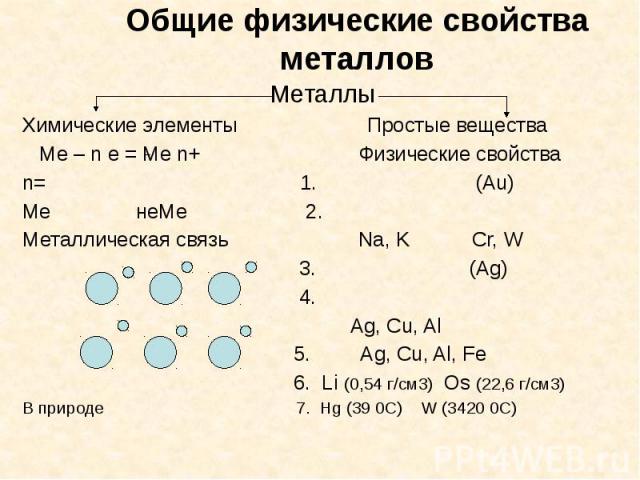
Общие физические свойства металлов Металлы Химические элементы Простые вещества Ме – n e = Ме n+ Физические свойства n= 1. (Au) Me неМе 2. Металлическая связь Na, K Cr, W 3. (Ag) 4. Ag, Cu, Al 5. Ag, Cu, Al, Fe 6. Li (0,54 г/см3) Os (22,6 г/см3) В природе 7. Hg (39 0C) W (3420 0C)
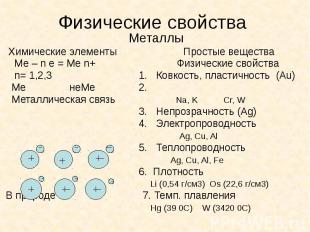
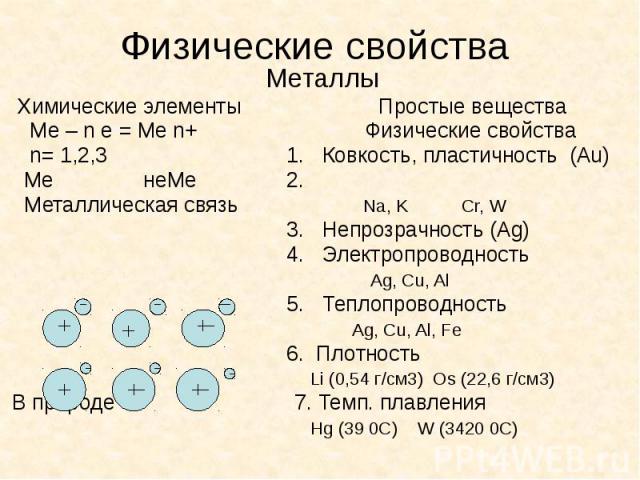
Физические свойства Металлы Химические элементы Простые вещества Ме – n e = Ме n+ Физические свойства n= 1,2,3 1. Ковкость, пластичность (Au) Me неМе 2. Металлическая связь Na, K Cr, W 3. Непрозрачность (Ag) 4. Электропроводность Ag, Cu, Al 5. Теплопроводность Ag, Cu, Al, Fe 6. Плотность Li (0,54 г/см3) Os (22,6 г/см3) В природе 7. Темп. плавления Hg (39 0C) W (3420 0C)

Химические свойства Электрохимический ряд напряжений металлов Li→Rb→K→Ba→Sr→Ca→Na→Mg→Al→Mn→Zn→Cr→Fe→Cd→Co→Ni→Sn→Pb→H→ Sb→Bi→Cu→Hg→Ag→Pd→Pt→Au Металл, находящийся в ряду напряжений левее водорода, способен вытеснить водород из кислот или солей.

Химические свойства ( с простыми веществами )

Взаимодействие со сложными веществами с кислотами Mg + 2HCl (разб) = MgCl2 + H2 Mg – 2e- = Mg2+ 2H+ +2e- = H20. ______________________ Mg + 2H+ = Mg 2+ + H0

с водными растворами солей менее активных металлов с водными растворами солей менее активных металлов Zn + CuSO4 = ZnSO4 + Cu Zn0 – 2е- = Zn2+ Cu2+ + 2е- = Cu0 _______________________________ Zn0 + Cu2+ = Zn2++ Cu0

Металлы в природе Наиболее активные – в виде солей: NaCl – поваренная соль. NaCl * KCl – сильвинит. CaCO3 – входит в состав мела, мрамора, известняка. CaSO4* 2H2O – гипс.

Al2O3 – корунд, рубин, сапфир. Al2O3 – корунд, рубин, сапфир.

FeS – сульфид железа.

Мало активные – в свободном виде: Cu и Pt

Au и Ag

Применение металлов Конструкционные материалы. Металлы и их сплавы -- один их главных конструкционных материалов современной цивилизации. Это определяется прежде всего их высокой прочностью. Электротехнические материалы. Металлы используются как в качестве хороших проводников электричества (медь, алюминий). Инструментальные материалы. Металлы и их сплавы широко применяются для изготовления инструментов (их рабочей части). В основном это инструментальные стали и твёрдые сплавы.


Выводы и итоги урока: Все металлы имеют металлическую кристаллическую решетку. В металлах существует металлическая связь. Основные признаки металлов – металлический блеск, непрозрачность, электро- и теплопроводность. Металлы проявляют только восстановительные свойства, потому что в реакциях они всегда отдают свои электроны. Металлы используют в основном в виде сплавов. Металлы имеют важное значение в жизни человека.

Использованные материалы: [email protected] ( 17/01-2011 г.) www.bibliard.ru ( 17/01-2011 г.) http://chemister.da.ru/Chemie/electrohimicheskii-rad.htm ( 17/01-2011 г.) http://www.newyork.ru/common/arc/story.php?id_cr=54&id=231768 ( 17/01-2011 г.) http://www.uralgold.ru/au_rudn.html ( 17/01-2011 г.) © Allbest.Ru. ( 17/01-2011 г.)