Презентация на тему: Металлы IА-группы щелочные металлы

Металлы IА-группы ЩЕЛОЧНЫЕ МЕТАЛЛЫ Аблямитова Татьяна АлексеевнаУчитель первой кв. категорииг. Казань, Республика Татарстан педагогический стаж 19 лет

Что узнаем… Положение щелочных металлов в Периодической системеИзменение свойств в группеИстория названияНахождение в природеФизические свойстваХимические свойстваОкраска пламениЗакреплениеЛитература

Щелочные металлы находятся в IA-группеСтроение внешнего энергетического уровня ns1 Максимальная степень окисленияПервой группы элементыодинаково валентны

Изменение свойств группе В ряду щелочных металлов: Радиус атома увеличивается Увеличиваются восстановительные свойства (способность отдавать электроны) Уменьшается прочность химической связи металл – металл Уменьшается температура плавления, температура кипения

«Если не знать имен - умрет и познание вещей» Карл Линней

ОТКРЫТИЕ ЩЕЛОЧНЫХ МЕТАЛЛОВ Литий был открыт шведским химиком Й. Арведсоном в 1817 г. по предложению Й.Берцелиуса назван литием (от греч. литос – камень)Натрий и калий были впервые получены английским химиком и физиком Г. Дэви в 1807 г. при электролизе едких щелочей Й. Берцелиус предложил назвать один новый элемент натрием (от араб. натрун – сода), а второй элемент по предложению Гильберта назван калием (от араб. алкали – щелочь)Гемфри Дэви(1778 – 1829)Йенс-Якоб Берцелиус (1779–1848)
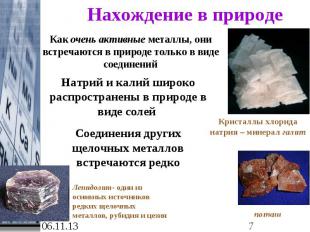
Нахождение в природе Как очень активные металлы, они встречаются в природе только в виде соединенийНатрий и калий широко распространены в природе в виде солей Соединения других щелочных металлов встречаются редкоКристаллы хлорида натрия – минерал галитЛепидолит- один из основных источников редких щелочных металлов, рубидия и цезия

Кислородные соединения щелочных металлов

Физические свойства Щелочные металлы легкоплавки и мягки, серебристы, как снежки…Литий - мягкий и пластичный, твёрже натрия, но мягче свинцаНатрий – мягкий металл, его можно резать ножомМеталлический рубидий в ампулеМеталлический цезий в ампуле

Эти металлы получили название щелочных, потому что большинство их соединений растворимы в воде. По-славянски «выщелачивать» означает «растворять», это и определило название данной группы металлов

Химические свойства Щелочные металлы активно взаимодействуют почти со всеми неметаллами:2Ме0 + Н20 = 2Ме+1Н-1 (гидрид)2Na + H2 = 2NaH2Ме0 + Cl20 = 2Mе+1Cl-1 (хлорид)2Ме0 + S0 = Mе+12S (сульфид)опытС кислородом натрий образует пероксиды:2Ме0 + О20 = Ме+12О2-1 пероксид2Na + O2 = Na2O2

Химические свойстваВсе щелочные металлы активно реагируют с водой, образуя щелочи и восстанавливая воду до водорода:2Ме0 + 2Н2О = 2Ме+1ОН + Н22Na + 2Н2О = 2NaOH + H2Скорость взаимодействия щелочного металла с водой увеличивается от лития к цезию опытКусочек металлического натрия реагирует с водой в присутствии фенолфталеина

Окраска пламени ионами щелочных металлов

Закрепление С помощью уравнений реакций осуществите превращения:1) Na → Na2O2 → Na2O NaOH → Na2CO3Li → Li2O → LiOH → LiCl LiOH

Домашнее задание § 11, упр. 4, 5

Литература http://ru.wikipedia.org/wiki/%D0%9B%D0%B5%D0%BF%D0%B8%D0%B4%D0%BE%D0%BB%D0%B8%D1%82http://ru.wikipedia.org/wiki/%D0%A9%D0%B5%D0%BB%D0%BE%D1%87%D0%BD%D1%8B%D0%B5_%D0%BC%D0%B5%D1%82%D0%B0%D0%BB%D0%BB%D1%8BХимия. 9 класс; учеб.для общеобразоват. учреждений/ О.С.Габриелян,-11-е изд., испр. - М. : Дрофа, 2006. – 267, с. : ил.




























