Презентация на тему: Магний химия

Презентация по химии на тему: «Магний» выполнила ученица 11б Иванова Дарья 900igr.net
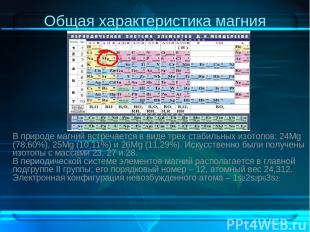
Общая характеристика магния ). В природе магний встречается в виде трех стабильных изотопов: 24Mg (78,60%), 25Mg (10,11%) и 26Mg (11,29%). Искусственно были получены изотопы с массами 23, 27 и 28. В периодической системе элементов магний располагается в главной подгруппе II группы; его порядковый номер – 12, атомный вес 24,312. Электронная конфигурация невозбужденного атома – 1s22s2p63s2;

Природные соединения Магний – по распространенности занимает VI место . Содержание в земной коре составляет 2,1%. Встречается только в виде соединений. магнезит MgCO3 и доломит MgCO3(CaCO3),карналлита MgCl2*KCl*6H2O ,оливин [(Mg, Fe)2SiO4] форстерит (Mg2SiO4бруцит Mg(OH)2, кизерит MgSO4, эпсонит MgSO4*7H2O, каинит MgSO4*KCl*3H2O. На поверхности Земли магний легко образует водные силикаты (тальк, асбест и др.), примером которых может служить серпентин 3MgO*2SiO2*2H2O. Из известных науке 1500 минералов около 200 (более 13%) содержат магний.

Получение Металлический магний был впервые получен в 1828 г. А. Бюсси. Основной способ получения магния – электролиз расплавленного карналлита или MgCl2. MgCl2 =Mg(на катоде)+Cl2(на аноде)

Физические свойства Магний – серебристо-белый блестящий металл, сравнительно мягкий и пластичный , хороший проводник тепла и электричества. На воздухе он покрывается тонкой оксидной пленкой, придающей ему матовый цвет. Кристаллическая решетка магния относится к гексагональной системе. |Атомный радиус, ( |1,6 | |Радиус иона Mg2+, ( |0,74 | |Энергия ионизации, эв, для Mg0 ( Mg+ |7,64 | | для Mg+ ( Mg2+ |15,03 | |Плотность (20 oC), г/см3 |1,739 | |Температура плавления., oC |651 | |Температура кипения, oC |1107 | |Теплота плавления, кал/г-атом |2100 | |Теплота испарения, кал/г-атом |31000 | |Теплота возгонки (при 25 oC), кал/г-атом |35000 | |Удельная теплоемкость (20 oC), кал/г-град |0,248 | |Теплопроводность (20 oC), кал/см(сек. град |0,37 | |Удельное электрическое сопротивление, Ом(см |4,5(10-6 | |Поперечное сечение захвата тепловых электронов, барн |0,059 | |Электропроводность (Hg=1) |22 |

Химические свойства I.Взаимодействие с простыми веществами 1) 2Mg+O2=2MgO (магний горит в кислороде воздуха ослепительно-белым пламенем 2)взаимодействие с галогенами Mg+Cl2=MgCl2(хлорид магния) 3)взаимодействие с серой Mg+S=MgS 4)взаимодействие с водородом Mg+H2=MgH2

II.взаимодействие со сложными веществами 1)взаимодействие с кислотами Mg+2HCl=MgCl2+H2 2)взаимодействие с водой Mg+H2O=Mg(OH)2+H2( (реакция идет очень медленно при кипячении).

Биологическая роль магния недостаток магния в организме способствует заболеванию инфарктом миокарда. Недостаточное количество магния в крови – признак переутомления или стрессового состояния. Основные продукты, содержащие магний – это абрикосы, персики, цветная и белокочанная капуста, помидоры, картофель. Потребность взрослого организма в магнии составляет 300–500 мг/день.

Магний как лекарственное средство Английская соль (MgSO4(7H2O) используется как слабительное и желчегонное средство. Водные растворы тиосульфата магния используются для лечения ожогов и других заболеваний кожи. Жженая магнезия (MgO) нейтрализует желудочный сок. Кроме того ,она применяется внутрь при кислотных отравлениях.

Применение Металлический магний имеет важное значение для народного хозяйства. Он используется при изготовлении сверхлегких сплавов для авиационной и ракетной техники, как легирующий компонент в алюминиевых сплавах, как восстановитель при магниетермическом получении металлов (титана, циркония ит.п.), в производстве высокопрочного “магниевого” чугуна со включенным графитом. Другие соединения магния – окись, карбонат, сульфат и т.п. –совершенно необходимы при изготовлении огнеупорных материалов, цементов и прочих строительных материалов.



![Природные соединения Магний – по распространенности занимает VI место . Содержание в земной коре составляет 2,1%. Встречается только в виде соединений. магнезит MgCO3 и доломит MgCO3(CaCO3),карналлита MgCl2*KCl*6H2O ,оливин [(Mg, Fe)2SiO4] форстерит… Природные соединения Магний – по распространенности занимает VI место . Содержание в земной коре составляет 2,1%. Встречается только в виде соединений. магнезит MgCO3 и доломит MgCO3(CaCO3),карналлита MgCl2*KCl*6H2O ,оливин [(Mg, Fe)2SiO4] форстерит…](https://fs3.ppt4web.ru/images/132073/183643/640/img2.jpg)


















