Презентация на тему: Ионная химическая связь

* Муниципальное общеобразовательное учреждение «Волхонщинская средняя общеобразовательная школа» Гарифзянов А.Р. Ионная химическая связь 900igr.net

* Цель урока обобщить и систематизировать знания о видах химической связи и их классификации как о важнейшем универсальном понятии теоретической химии

* План изучения темы урока Понятие «химическая связь». Ионная химическая связь: механизм образования; характеристики связи; ионная кристаллическая решетка.

* Что такое химическая связь?
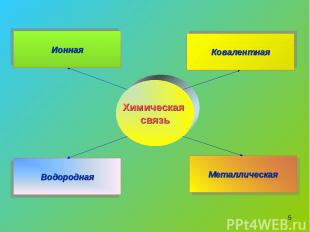
* Химическая связь Водородная Металлическая Ковалентная Ионная
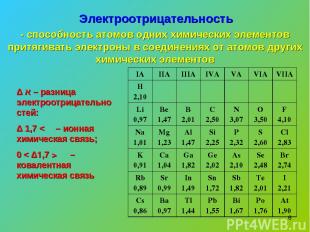
* Электроотрицательность - способность атомов одних химических элементов притягивать электроны в соединениях от атомов других химических элементов Δ א – разница электроотрицательностей: Δ א > 1,7 – ионная химическая связь; 0 < Δא < 1,7 – ковалентная химическая связь IA IIA IIIA IVA VA VIA VIIA H 2,10 Li 0,97 Be 1,47 B 2,01 C 2,50 N 3,07 O 3,50 F 4,10 Na 1,01 Mg 1,23 Al 1,47 Si 2,25 P 2,32 S 2,60 Cl 2,83 K 0,91 Ca 1,04 Ga 1,82 Ge 2,02 As 2,10 Se 2,48 Br 2,74 Rb 0,89 Sr 0,99 In 1,49 Sn 1,72 Sb 1,82 Te 2,01 I 2,21 Cs 0,86 Ba 0,97 Tl 1,44 Pb 1,55 Bi 1,67 Po 1,76 At 1,90

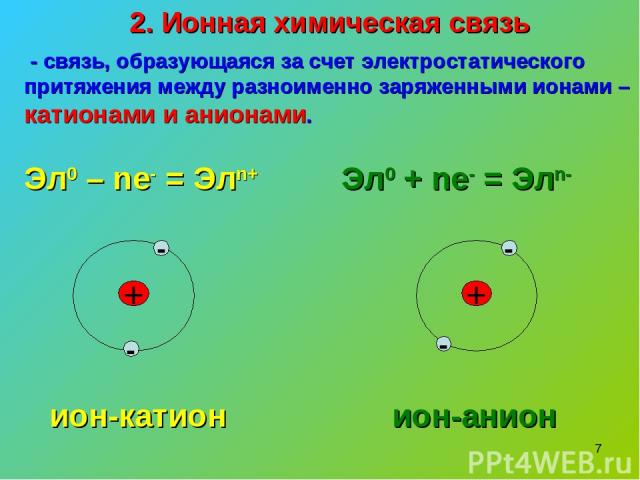
* 2. Ионная химическая связь - связь, образующаяся за счет электростатического притяжения между разноименно заряженными ионами – катионами и анионами. Эл0 – nе- = Элn+ Эл0 + nе- = Элn- + - - + - ион-катион - ион-анион

* Механизм образования ионной связи 1s22s22p63s1 1s 2s 3s 2p 1s 2s 3s 2p 3p 1s22s22p63s23p5 Na0 – 1e- = Cl20 + 2e- = 2 Na+ Cl- хлорид натрия Na . + Cl . . . . . . . = Na+ Cl . . . . . . . [ -[ . +11Na +17 Cl Составьте электронные и графические формулы атомов:

* Запомни!!! полного перехода электронов при образовании ионной химической связи не происходит. Об этом свидетельствуют величины эффективных зарядов в соединениях
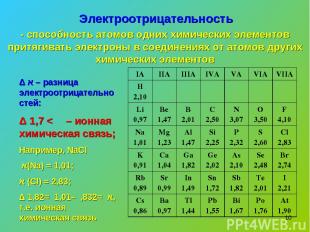
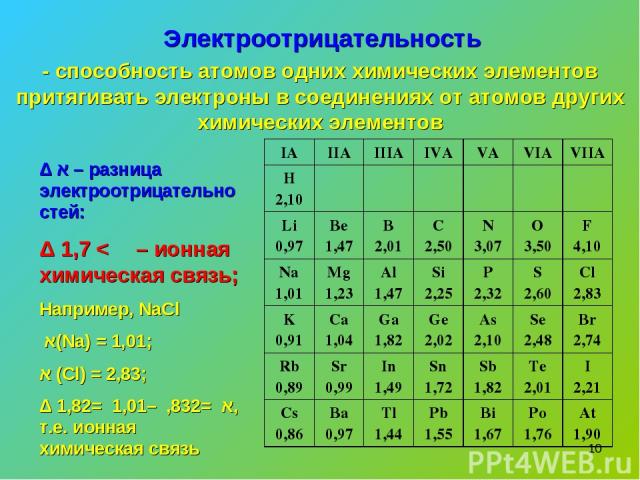
* Электроотрицательность - способность атомов одних химических элементов притягивать электроны в соединениях от атомов других химических элементов Δ א – разница электроотрицательностей: Δ א > 1,7 – ионная химическая связь; Например, NaCl א(Na) = 1,01; א (Cl) = 2,83; Δ א = 2,83 – 1,01 = 1,82, т.е. ионная химическая связь IA IIA IIIA IVA VA VIA VIIA H 2,10 Li 0,97 Be 1,47 B 2,01 C 2,50 N 3,07 O 3,50 F 4,10 Na 1,01 Mg 1,23 Al 1,47 Si 2,25 P 2,32 S 2,60 Cl 2,83 K 0,91 Ca 1,04 Ga 1,82 Ge 2,02 As 2,10 Se 2,48 Br 2,74 Rb 0,89 Sr 0,99 In 1,49 Sn 1,72 Sb 1,82 Te 2,01 I 2,21 Cs 0,86 Ba 0,97 Tl 1,44 Pb 1,55 Bi 1,67 Po 1,76 At 1,90
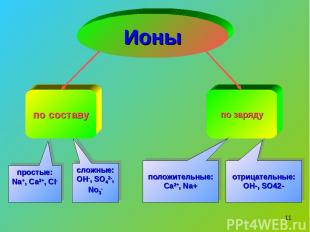
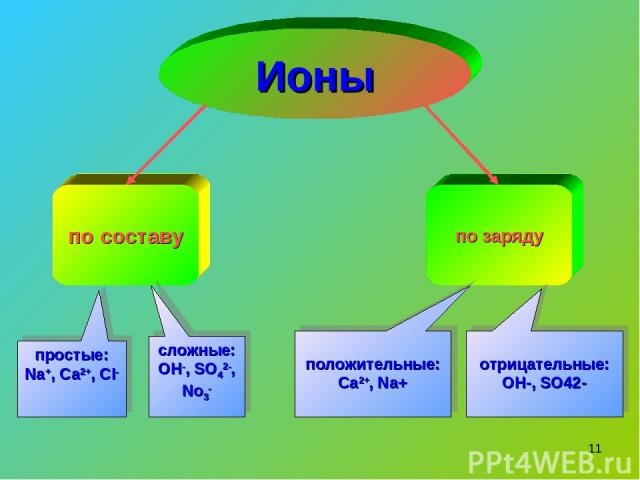
* по составу по заряду простые: Na+, Ca2+, Cl- сложные: OH-, SO42-, No3- положительные: Ca2+, Na+ Ионы отрицательные: OH-, SO42-
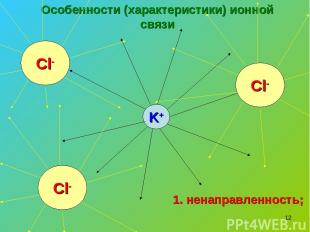
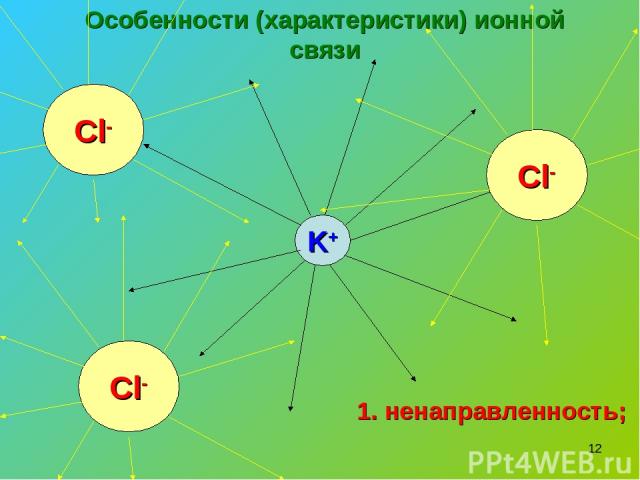
* Особенности (характеристики) ионной связи K+ Cl- Cl- Cl- 1. ненаправленность;
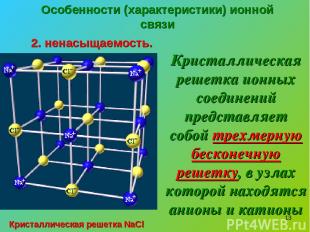
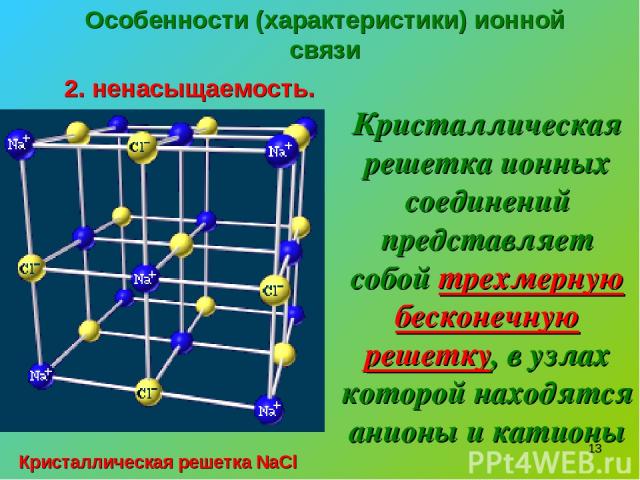
* Особенности (характеристики) ионной связи 2. ненасыщаемость. Кристаллическая решетка ионных соединений представляет собой трехмерную бесконечную решетку, в узлах которой находятся анионы и катионы Кристаллическая решетка NaCl

* Домашнее задание §6 (стр. 44-46), упр. 4 на стр. 56, распишите механизм образования ионной связи в молекулах: 1 вариант - хлорида кальция; 2 вариант – бромида калия; 3 вариант – нитриде натрия.

*