Презентация на тему: Эмульсии

Жидкость-жидкость. Эмульсии - грубодисперные системы из несмешивающихся жидкостей с размером капель от 100 до 5000 нм. Свойства эмульсии: 1. Эмульсии имеют поверхность раздела. 2. Эмульсии неустойчивы. 3. Эмульсии нуждаются в стабилизаторах [эмульгаторах]. Главным фактором устойчивости эмульсии – заряд [ ], или дзета-потенциал, образующийся при адсорбировании ионов стабилизатора на капельках эмульсии. Роль стабилизатора (эмульгатора): 1. Эмульгатор сообщает капелькам эмульсии заряд, за счёт диссоциации адсорбированных молекул. 2. Эмульгатор создаёт вокруг капелек эмульсии оболочку, препятствующую коалесценции (слипанию).
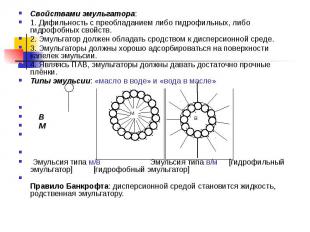
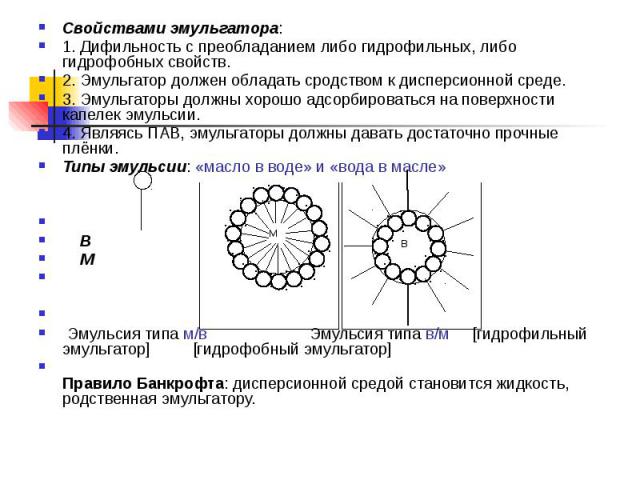
Свойствами эмульгатора: Свойствами эмульгатора: 1. Дифильность с преобладанием либо гидрофильных, либо гидрофобных свойств. 2. Эмульгатор должен обладать сродством к дисперсионной среде. 3. Эмульгаторы должны хорошо адсорбироваться на поверхности капелек эмульсии. 4. Являясь ПАВ, эмульгаторы должны давать достаточно прочные плёнки. Типы эмульсии: «масло в воде» и «вода в масле» В М Эмульсия типа м/в Эмульсия типа в/м [гидрофильный эмульгатор] [гидрофобный эмульгатор] Правило Банкрофта: дисперсионной средой становится жидкость, родственная эмульгатору.

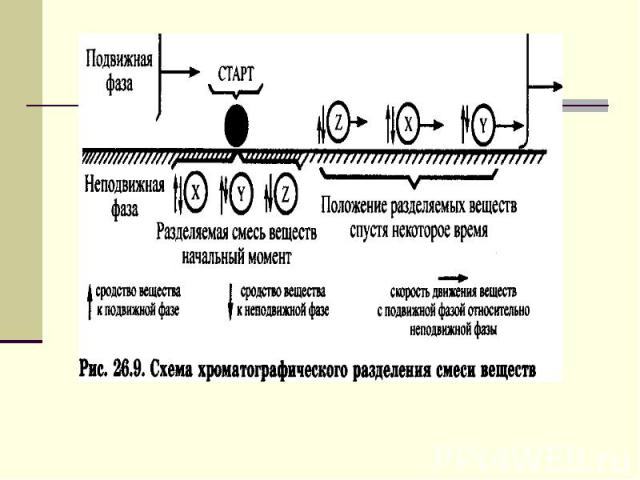
Хроматография - физико-химический метод разделе­ния и анализа смесей веществ, основанный на процессах сорбции и десорбции разделяемых веществ между подвижной и неподвижной фазами Требования: - разделяемые вещества должны иметь различные константы сорбции по отношению к подвижной и неподвижной фазам; - неподвижная фаза должна быть такой, чтобы процессы сорбции разделяемых веществ на ней были обратимы.
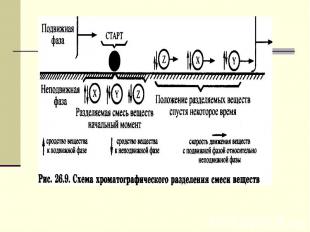

Хроматографическая методика 1) выбор и подготовка используемых образцов п и н/п фаз; 2) нанесение смеси на н. фазу и введение п. фазы; 3) собственно хроматографирование4) детектирование веществ, т. е. 5) количественное определение содержания веществ в разделенных зонах. Хроматографическая методика 1) выбор и подготовка используемых образцов п и н/п фаз; 2) нанесение смеси на н. фазу и введение п. фазы; 3) собственно хроматографирование4) детектирование веществ, т. е. 5) количественное определение содержания веществ в разделенных зонах. Эффективность хроматографического процесса зависит: 1) от физико-химических свойств неподвижной и подвижной фаз; 2) от сродства разделяемых веществ к контактирующим фазам; 3) от условий хроматографирования (скорости движения подвижной фазы, температуры, времени разделения).

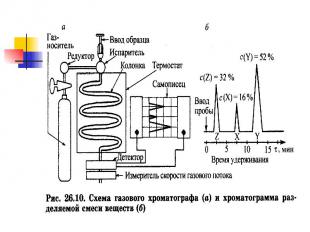
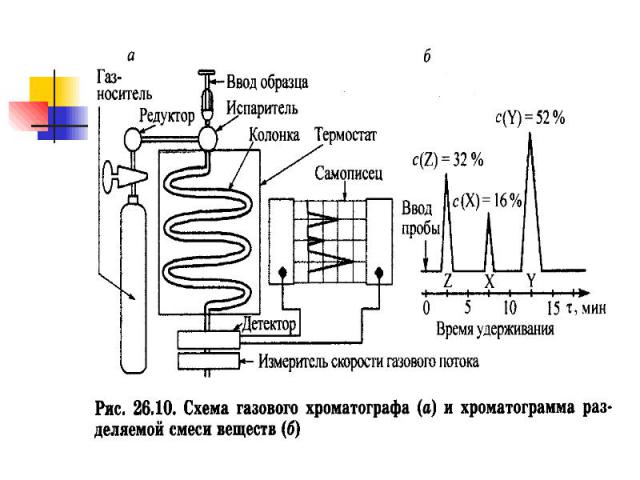
Классификация хроматографических методов. Классификация хроматографических методов. По цели проведения: - аналитическая хроматография используется для качественного и количественного анализа смеси веществ; - препаративная хроматография предназначена для очистки вещества от примесей. По агрегатному состоянию подвижной фазы: газовая жидкостная. Жидкостная хроматография делится - на плоскостную (тонкослойную или бумажную) - объемную (колоночную).
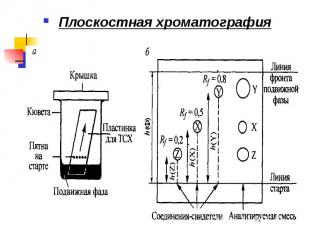
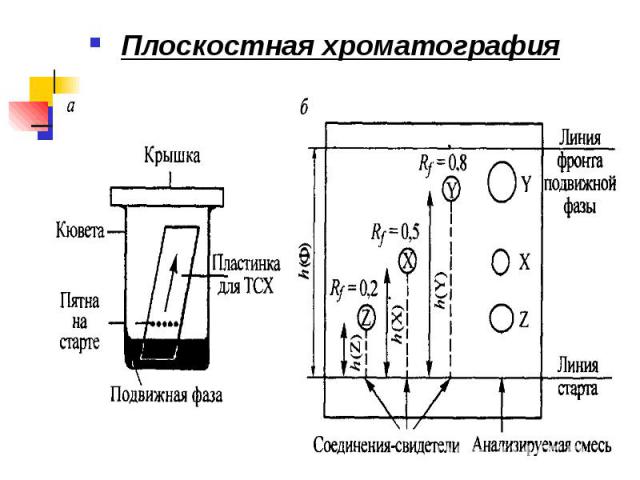
Плоскостная хроматография Плоскостная хроматография

Для идентификации веществ Для идентификации веществ -соединения-свидетели, - значения коэффициента распределения Rf(X)= h(Х)/ h(Y) Количественный анализ - путем измерения оптической плотности пятна, образующегося при взаимодействии определяемого вещества с цветообразующим реагентом

По механизму разделения веществ хроматографию подразделяют По механизму разделения веществ хроматографию подразделяют -В адсорбционной - благодаря различию их констант адсорбции в системах г—т или ж— т. - В распределительной - вследствие различия констант распределения при абсорбции веществ жидкой неподвижной фазой, которая обычно нанесена тонким слоем на твердый носитель. -В ионообменной - на различии их констант ионного обмена между раствором и ионитом. АК –анализатор- -В молекулярно-ситовой (гель-фильтрация) -различий в размерах их частиц. -В биоспецифической хроматографии -на избирательном взаимодействии -фермента с субстратом, антигена с антителом, гормона с рецептором,
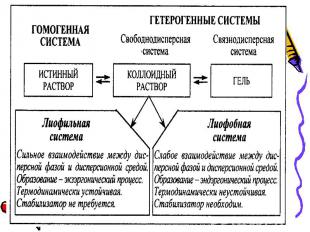

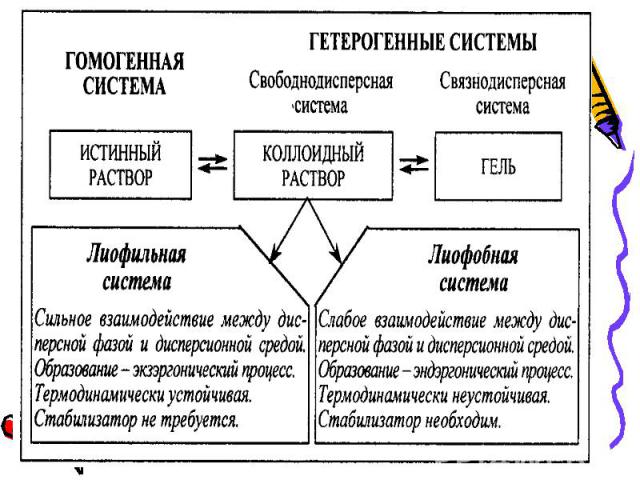
Дисперсная система – Дисперсная система – одна из фаз представлена мелкими частицами, равномерно распределенными в объеме другой однородной фазы. Дисперсная система состоит из дисперсной фазы и дисперсионной среды



ЛИОФОБНЫЕ КОЛЛОИДНЫЕ РАСТВОРЫ - золи. ЛИОФОБНЫЕ КОЛЛОИДНЫЕ РАСТВОРЫ - золи. Получение золей . А. Дисперсионный метод. а/ Механические методы - дроблением, измельчением, истиранием б/ Ультразвуковой метод - под действием сжатий и расширений системы, но механизм еще мало изучен. в/ Метод пептизации. для свежих осадков Fе(ОН)3 пептизатором служит FеСl3; лечение тромбофлебита гепарином г/ Распыление под водой в вольтовой дуге благородных металлов с последующей конденсацией паров металла при охлаждении [метод Бредига].

Б. Конденсационный метод. Б. Конденсационный метод. -на переводе веществ в нерастворимое состояние при помощи химических реакций а/ Метод окисления. 2 H2S + SO2 3 S + 2 H2O б/ Метод восстановления. Ag2O + H2 2 Ag + H2O [так образуется золь серебра] в/ Реакция двойного обмена с образованием труднорастворимого вещества: BaCl2 + K2SO4 BaSO4 + 2KCl [золь сульфата бария] г / метод гидролиза. FeCl3 + 3 H2O Fe(OH)3 + 3 HCl д/ метод замены растворителя.
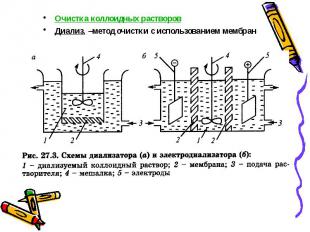
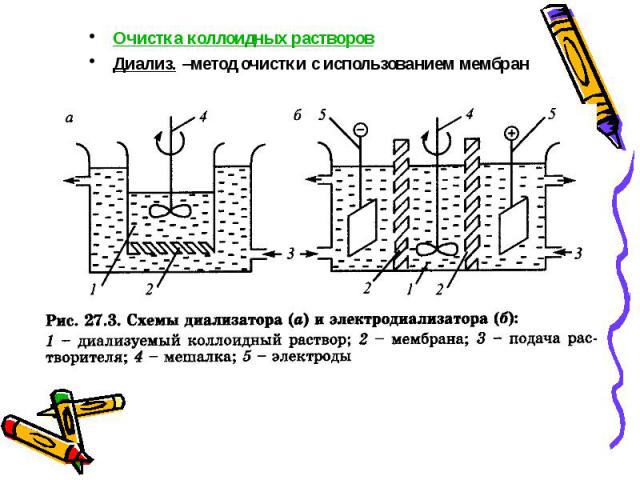
Очистка коллоидных растворов Очистка коллоидных растворов Диализ. –метод очистки с использованием мембран

Электродиализ — это диализ при использовании постоянного электрического тока Электродиализ — это диализ при использовании постоянного электрического тока Вивидиффузия. Через трубочки из коллодия протекает кровь, из которой в окружающий физраствор или воду выходят НМС обмена веществ — «система искусственной почки» — АИП Ультрафильтрация — это отделение дисперсной фазы от диспер­сионной среды путем фильтрования через мембраны под давлением или в вакууме. Гельфильтрация. В поры декстринового гель НМС входят и выходят, а ВМС (белки) нет . При элюировании сначала появится фракция ВМС, а затем НМС

Молекулярно-кинетические свойства коллоидных систем Молекулярно-кинетические свойства коллоидных систем 1.Броуновское движение для К.С. замедленно и - Не зависит от природы вещества. -Зависит от размеров частиц. - от температуры [абсолютной]. - от вязкости дисперсионной среды - от коэффициента диффузии 2.Диффузия - Для К.С. замедленна, т.к. крупные частицы. 3. Росм К.С ниже Росм истинных растворов вследствие большого размера частиц и малых концентраций 4. Способность дисперсной системы сохранять по всему объёму распределение частиц называется седиментационной или кинетической устойчивостью. 4. Ультрацентрифугирование. Оседание коллоидов под действием центробежной силы . А.В.Думанский в 1913 г., Сведберг(ультрацентрифуга)

……. …….

Нефелометрия Нефелометрия метод определения концентрации и степени дисперсности коллоидных систем на явлении светорассеяния. Интенсивность рассеянного света прямо пропорциональна концентрации частиц, и весовой концентрации дисперсной фазы Зная концентрацию одного из золей С1 [стандартный золь известной концентрации], можно определить концентрацию второго золя:

Окраска золей Окраска золей связана с избирательным поглощением световых лучей. Если золь только рассеивает, а не поглощает световые лучи — он бесцветен. Опалесценция- рассеяние света в коллоидных системах и изменение окраски коллоида По Рэлею : светорассеяние обратно пропорционально длине волны падающего света Дихроизм— наложение опалесценции на собственную окраску золя.

Ультрамикроскопия использует эффект рассеяния света отдельными частицами. Ультрамикроскопия использует эффект рассеяния света отдельными частицами. В 1903 году Зигмонди, : наблюдения на тёмном фоне при боковом освещении. С=N/V , где N – число световых точек V-объем Для электронного микроскопа увеличение - 900 000 раз. Рентгеноструктурный анализ - используется дифракция рентгеновских лучей, направляемых на частицу под разными ракурсами

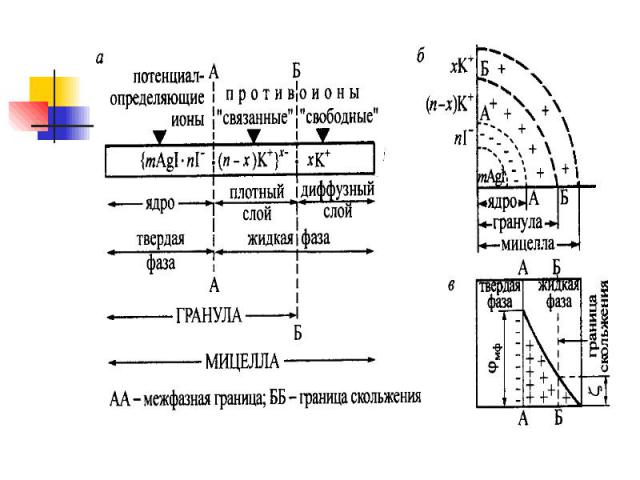
СТРОЕНИЕ МИЦЕЛЛ СТРОЕНИЕ МИЦЕЛЛ Мицелла - гетерогенная микросистема, которая состоит из микрокристалла дисперсной фазы, окруженного сольватированными ионами стабилизатора. Ядро мицеллы - микрокристалл малорастворимого вещества, на поверхности которого адсорбированы, потенциалопределяющие ионы, сообщающие заряд ядру мицеллы.
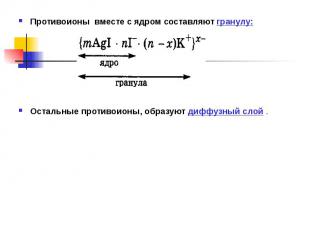
Противоионы вместе с ядром составляют гранулу: Противоионы вместе с ядром составляют гранулу: Остальные противоионы, образуют диффузный слой .
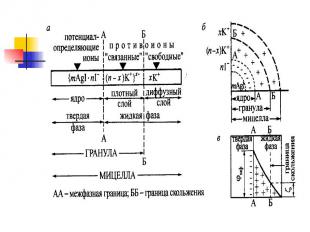

Межфазным потенциалом –(электродинамическим)(фи) называется потенциал ДЭС на границе раздела между твердой и жидкой фазами в мицелле (на схемах мицеллы - граница АА). Межфазным потенциалом –(электродинамическим)(фи) называется потенциал ДЭС на границе раздела между твердой и жидкой фазами в мицелле (на схемах мицеллы - граница АА). Электрокинетическим потенциалом (дзета) называется потенциал на границе скольжения между адсорбционной и диффузионной частями ДЭС











![Б. Конденсационный метод. Б. Конденсационный метод. -на переводе веществ в нерастворимое состояние при помощи химических реакций а/ Метод окисления. 2 H2S + SO2 3 S + 2 H2O б/ Метод восстановления. Ag2O + H2 2 Ag + H2O [так образуется золь серебра] … Б. Конденсационный метод. Б. Конденсационный метод. -на переводе веществ в нерастворимое состояние при помощи химических реакций а/ Метод окисления. 2 H2S + SO2 3 S + 2 H2O б/ Метод восстановления. Ag2O + H2 2 Ag + H2O [так образуется золь серебра] …](https://fs1.ppt4web.ru/images/95236/144716/640/img15.jpg)

![Молекулярно-кинетические свойства коллоидных систем Молекулярно-кинетические свойства коллоидных систем 1.Броуновское движение для К.С. замедленно и - Не зависит от природы вещества. -Зависит от размеров частиц. - от температуры [абсолютной]. - от в… Молекулярно-кинетические свойства коллоидных систем Молекулярно-кинетические свойства коллоидных систем 1.Броуновское движение для К.С. замедленно и - Не зависит от природы вещества. -Зависит от размеров частиц. - от температуры [абсолютной]. - от в…](https://fs1.ppt4web.ru/images/95236/144716/640/img18.jpg)