Презентация на тему: Анализ ЕГЭ по химии 2011

Анализ ЕГЭ по химии 2011 По результатам аналитического отчёта ФИПИ
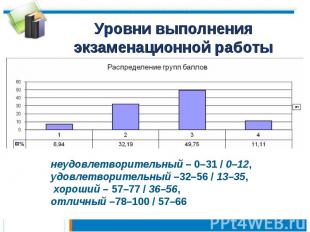
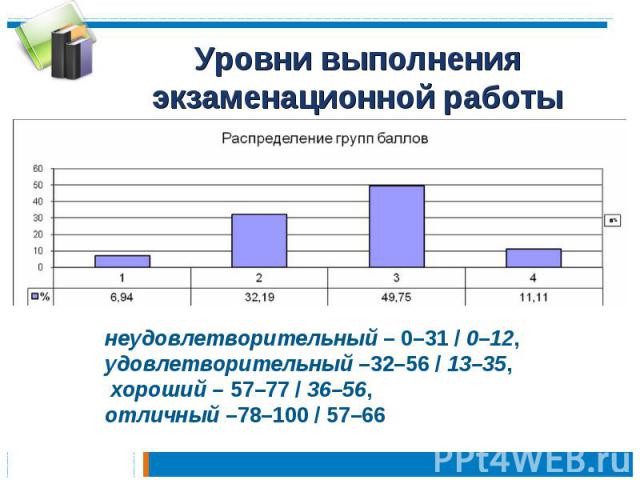
Уровни выполнения экзаменационной работы неудовлетворительный – 0–31 / 0–12, удовлетворительный –32–56 / 13–35, хороший – 57–77 / 36–56, отличный –78–100 / 57–66

Результаты выполнения заданий, проверяющих усвоение содержания блока «Теоретические основы химии»Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атома. Основное и возбужденное состояние атомов - 80,8% Закономерности изменения химических свойств элементов и их соединений по периодам и группам - 74,7% Общая характеристика металлов IА–IIIА групп в связи с их положением в п.с.х.э. и особенностями строения их атомов - 72,5% Характеристика переходных элементов (меди, цинка, хрома, железа) по их положению в п.с.х.э. и особенностям строения их атомов - 62,3% Общая характеристика неметаллов IVА–VIIА групп в связи с их положением в п.с.х.э. и особенностями строения их атомов - 77,6% Ковалентная химическая связь, ее разновидности, механизмы образования. Характеристики ковалентной связи. Ионная связь. Металлическая связь. Водородная связь - 76,2% Электроотрицательность. Степень окисления и валентность химических элементов - 88,1%

8. Вещества молекулярного и немолекулярного строения. Зависимость свойств веществ от особенностей их кристаллической решетки - 71,2% 9. Классификация химических реакций в неорганической и органической химии - 76,8% 10. Скорость реакции, ее зависимость от различных факторов - 64,6% 11. Тепловой эффект реакции - 72,6% 12. Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов - 65,5% 13. Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты - 77,8% 14. Реакции ионного обмена - 83,0% 15. Гидролиз солей - 73,7% 16. Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от неё – 72,2% 17. Электролиз расплавов и растворов - 64,6% 18. Механизмы реакций замещения и присоединения в органической химии. Правило В.В. Марковникова - 62,9%

Пример 1Верны ли следующие суждения о металлах и их соединениях? А. Высшие оксиды всех элементов IIA группы проявляют только основные свойства. Б. Восстановительные свойства магния выражены сильнее, чем у бериллия. 1) верно только А (14%) 2) верно только Б (43%) 3) верны оба суждения (37%) 4) оба суждения неверны (5%)

Пример 2Скорость реакции омыления сложного эфира CH3COOC2H5 + OH → CH3COO + C2H5OH не зависит от 1) температуры (26%) 2) концентрации щелочи (11%) 3) концентрации спирта (52%) 4) концентрации эфира (11%)

Пример 3Химическое равновесие в системе С2Н5ОН + СН3СООН → СН3СООС2Н5 + Н2О – Q смещается в сторону продуктов реакции при 1) добавлении воды (14%) 2) уменьшении концентрации уксусной кислоты (18%) 3) увеличении концентрации эфира (16%) 4) удалении воды (51%)

Пример 4Взаимодействие 2-метилпропана и брома при комнатной температуре на свету 1) относится к реакциям замещения 2) протекает по радикальному механизму 3) приводит к преимущественному образованию 1-бром-2-метилпропана 4) приводит к преимущественному образованию 2-бром-2-метилпропана 5) протекает с разрывом связи C – C 6) является каталитическим процессом

Блок «Неорганическая химия»Классификация и номенклатура неорганических веществ - 85,4% Характерные химические свойства простых веществ – металлов: щелочных, щелочноземельных, алюминия; переходных металлов – меди, цинка, хрома, железа - 73,4% Характерные химические свойства простых веществ –неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния - 73,4% Характерные химические свойства оксидов - 71,7% Характерные химические свойства кислот, оснований и амфотерных гидроксидов – 66,1% Характерные химические свойства солей: средних, кислых, основных; комплексных (на примере соединений алюминия и цинка) - 62,2% Реакции, подтверждающие взаимосвязь различных классов неорганических веществ – 60,1%

Пример 5Карбонат бария реагирует с водным раствором каждого из двух веществ: 1) H2SO4 и NaOH (28%) 2) NaCl и CuSO4 (13%) 3) HCl и CH3COOH (50%) 4) NaHCO3 и HNO3 (8%)

Пример 6В схеме превращений ZnO → X1 → X2 → Zn(OH)2 веществами Х1 и Х2 могут быть соответственно 1) ZnS и ZnSO4 (17%) 2) ZnSO4 и ZnCl2 (52%) 3) Zn(OH)2 и Zn (20%) 4) ZnCO3 и Zn3(PO4)2 (10%)

Блок «Органическая химия»Теория строения органических соединений. Изомерия структурная и пространственная. Гомологи и гомологический ряд - 69,4% Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа - 69,4% Классификация и номенклатура органических соединений - 81,9% Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола) - 66,1% Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола - 59,1% Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров - 66,6% Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот - 60,0% Биологически важные вещества: жиры, белки, углеводы - 66,0% Взаимосвязь органических веществ – 71,4%

Пример 7С раствором гидроксида натрия реагирует 1) CH2 = CH2 (16%) 2) CH3 – O – CH3 (8%) 3) CH3 – CH2 – OH (17%) 4) C6H5OH (59%)

Пример 8С 2-аминопропановой кислотой реагируют 1) этан 2) сульфат натрия 3) пропанол-1 4) толуол 5) гидроксид бария 6) бромоводород

Пример 9В схеме превращений HC ≡ CH → X → CH3COOH веществом Х является 1) CH3CHO(71%) 2) CH3 − CO − CH3 (8%) 3) CH3 − CH2OH(15%) 4) CH3 − CH3 (5%)

Пример 10Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: X1→бензол

Блок «Методы познания веществ и химических реакций»Раздел «Экспериментальные основы химии» Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии. Научные методы исследования химических веществ и превращений. Методы разделения смесей и очистки веществ. Качественные реакции на неорганические вещества и ионы. Идентификация органических соединений - 58,4% Основные способы получения углеводородов (в лаборатории) - 59,9% Основные способы получения кислородсодержащих соединений (в лаборатории) - 69,3% Раздел «Основные представления о промышленных способах получения важнейших веществ» 1. Понятие о металлургии: общие способы получения металлов. Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и его последствия. Природные источники углеводородов, их переработка. Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки – 63,5%

Раздел «Расчеты по химическим формулам и уравнениям реакций» Вычисление массы растворенного вещества, содержащегося в определенной массе раствора с известной массовой долей – 52,0% Расчеты объемных отношений газов при химических реакциях – 73,0% Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ – 52,4% Расчеты теплового эффекта реакции – 71,0% Расчеты массы (объема, количества вещества) продуктов реакции, если одно из веществ дано в виде раствора с определенной массовой долей растворенного вещества – 31,8% Нахождение молекулярной формулы вещества – 34,3%

Пример 11Верны ли следующие суждения о правилах техники безопасности? А. Пробирку с бензолом запрещается нагревать на открытом пламени. Б. Для приготовления раствора серной кислоты нужно приливать воду к концентрированной кислоте. 1) верно только А (46%) 2) верно только Б (12%) 3) верны оба суждения (29%) 4) оба суждения неверны (13%)

Пример 12Синтез-газ, используемый в производстве метанола, представляет собой смесь 1) CH4 и CO2 (22%) 2) CO2 и H2 (14%) 3) CH4 и CO (13%) 4) CO и H2 (49%)

Пример 13В 15%-ном растворе серной кислоты массой 300 г растворили карбид алюминия. Выделившийся при этом метан занял объем 2,24 л (н.у.). Рассчитайте массовую долю серной кислоты в полученном растворе.
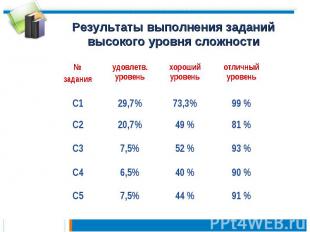
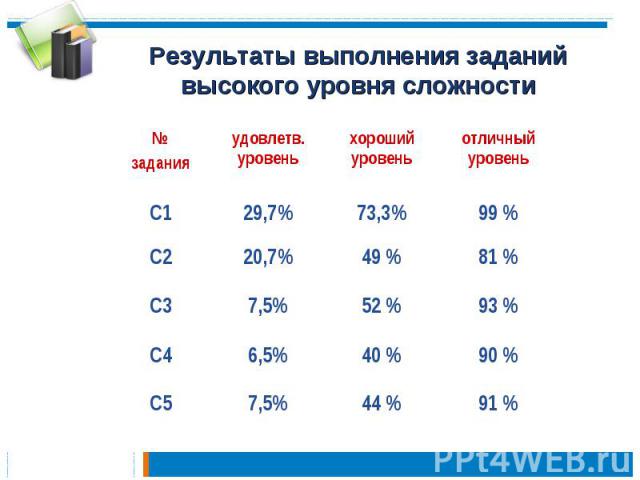
Результаты выполнения заданий высокого уровня сложности

Общая характеристика уровня подготовкиМинимальный уровень: тестовый балл – 0–31; первичный балл – 0–12; процент выпускников данной категории – 6,94 (5419 человек) Удовлетворительный уровень: тестовый балл – 32–56; первичный балл – 12–35; процент выпускников данной категории – 32,19 (25 130 человек) Хороший уровень: тестовый балл – 57–77; первичный балл – 36–56; процент выпускников данной категории – 49,75 (38 838 человек) Отличный уровень: тестовый балл – 78–100; первичный балл – 57–66; процент выпускников данной категории – 11,11 (8674 человека)
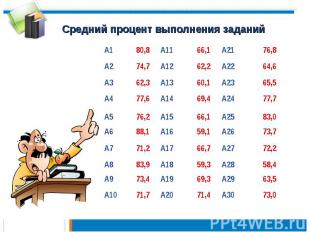
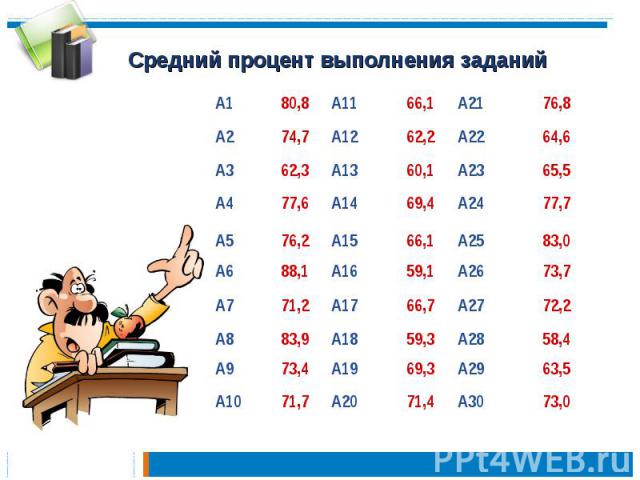
Средний процент выполнения заданий
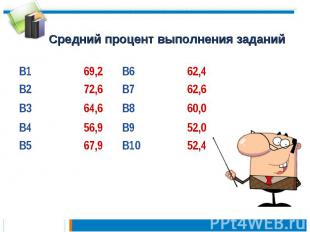
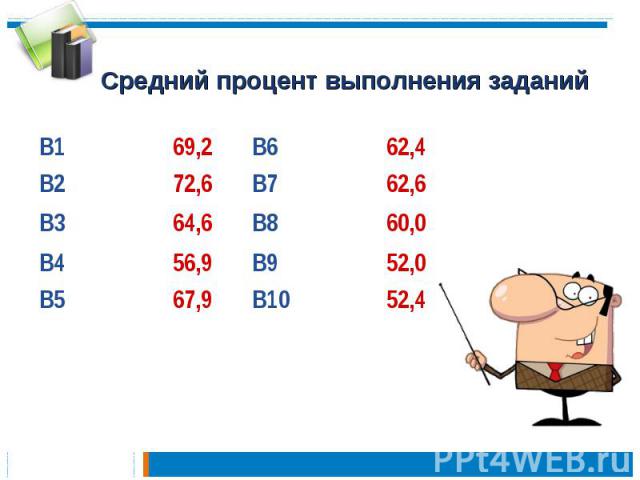
Средний процент выполнения заданий

Средний процент выполнения заданий