Презентация на тему: Теория по молекулярной физике

Молекулярная физика Лектор Кунашенко Юрий Петрович ----------------------- д.ф.м.н. профессор http://portal.main.tpu.ru:7777/SHARED/k/KUNASHENKO 900igr.net

Молекулярная физика Литература Основная 1. Савельев «Курс Общей Физики», Москва, Апрель, 2002 г. т.3 2. А.А. Деталаф, В.М. В.М. Яворский «Курс Общей Физики» М., Высшая школа, 2000. 3. В.С. Волькинштейн . «Сборник задач по общему курсу физики», - С.-Петербург, 2001. Дополнительная 1. Берклеевский Курс физики. – М., Наука, 1986. 2., Фейнмановские лекции по физике, М.: Мир, 1967.

Термодинамика Молекулярная физика – раздел физики, изучающий свойства тел в зависимости от характера движения и взаимодействия частиц, образующих тело. Термодинамика анализирует условия и количественные соотношения превращения энергии. Её первоначальная задача – изучение закономерностей превращения тепла в работу (в тепловых машинах). Основным содержанием современной физической термодинамики является изучение закономерностей тепловой формы движущейся материи и связанных с ней физических явлений.

Термодинамика Совокупность тел, составляющих макроскопическую систему, называется термодинамической системой. Система может находиться в различных состояниях. Величины, характеризующие состояние системы называются параметрами состояния: давление, температура, объём и так далее. Любой параметр, имеющий определённое значение для каждого равновесного состояния, является функцией состояния Равновесной называется такая система, параметры состояния которой одинаковы во всех точках системы и не изменяются со временем (при неизменных внешних условиях). Процесс – переход из одного равновесного состояния в другое. Релаксация – возвращение системы в равновесное состояние

Термодинамика Атомная единица массы (а.е.м.) – mед – единица массы, равная 1/12 массы изотопа углерода С12. mед = 1,66·10 27 кг Количество вещества, в котором содержится число молекул, равное числу атомов в 12 г С12 (изотопа углерода) называется молем (в 12 кг – киломолем). Число молекул в одном моле называется числом Авагадро NА = 6,02·1023 моль 1 = 6,02·1026 кмоль 1 Молярная масса – масса одного моля (µ) µ = АmедNА. При одинаковых температурах и давлениях все газы содержат в единице объёма одинаковое число молекул. Число молекул, содержащихся в 1 м3 при нормальных условиях, называется числом Лошмидта: NL = р0/kT0 = 2,68·1025 м 3. Нормальные условия: p0 = 105 Па; Т0 =273 К; k – постоянная Больцмана равная 1,38·10 23Дж/К.

Давление. Основное уравнение молекулярно-кинетической теории. n – концентрация молекул в сосуде; m0 – масса одной молекулы в единицу времени (1/6) nυ молекул при абсолютно-упругом ударе m0υx – ( m0υx) = 2m0υx За время dt о стенку, площадью S успеет удариться n = Sυxdt число молекул Общий импульс, который получит стенка S: p = dF/dS.

Давление. Основное уравнение молекулярно-кинетической теории. Более точно случайную величину характеризует среднеквадратичная величина. где Ek – средняя энергия одной молекулы. Это и есть основное уравнение молекулярно-кинетической теории газов. Иногда за основное уравнение принимают p = nkT. Единицы измерения давления: 1 Па = 1 Н/м2; 1 ат. = 9,8 Н/см2 = 98066 Па 105 Па 1 мм.рт.ст. = 1 тор = 1/760 ат. = 133,3 Па 1 бар = 105 Па; 1 ат. = 0,98 бар.

Температура. Чем выше температура тела тем больше кинетическая энергия его молекул! Чтобы связать единицу энергии с градусом, Больцман ввел коэффициент пропорциональности k который впоследствии был назван его именем: k – постоянная Больцмана равная 1,38·10 23 Дж·К 1 на одну молекулу идеального газа R – универсальная газовая постоянная для молярной массы и газа р = nkT

Изопроцессы идеальных газов. Изопроцессы идеального газа – процессы, при которых один из параметров остаётся неизменным. Изохра Изохорический процесс. Закон Шарля. V = const. Изохорическим процессом называется процесс, протекающий при постоянном объёме.
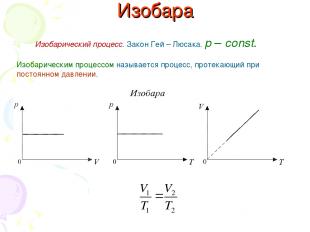
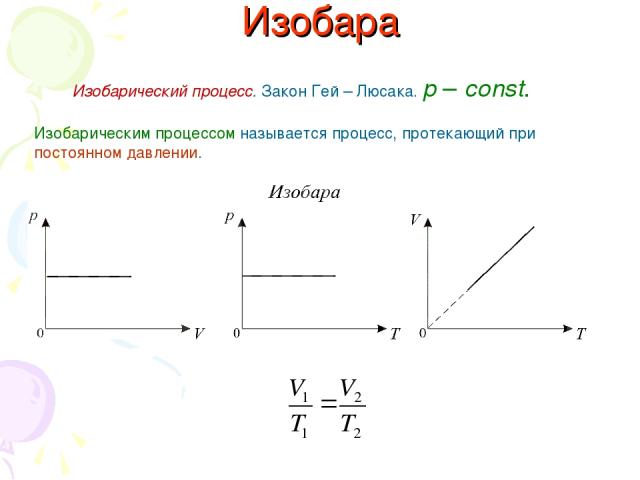
Изобара Изобарический процесс. Закон Гей – Люсака. р – const. Изобарическим процессом называется процесс, протекающий при постоянном давлении.
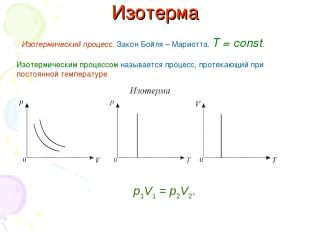
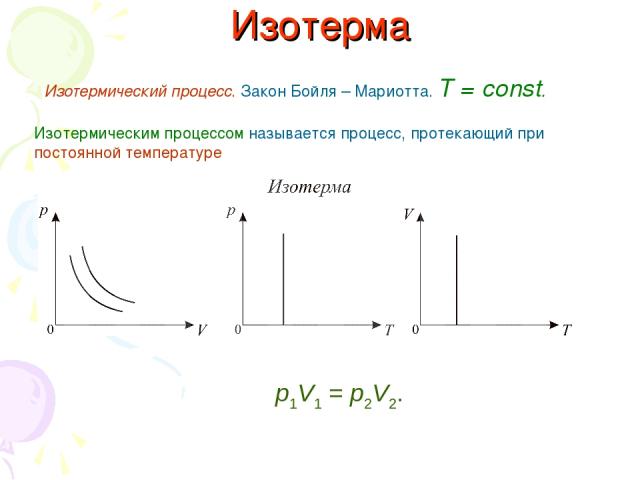
Изотерма Изотермический процесс. Закон Бойля – Мариотта. T = const. Изотермическим процессом называется процесс, протекающий при постоянной температуре р1V1 = р2V2.

Термодинамика Адиабатический процесс – термодинамический процесс, происходящий без теплообмена с окружающей средой. Закон Авогадро. При одинаковых давлениях и одинаковых температурах, в равных объёмах различных идеальных газов содержится одинаковое число молекул. В одном моле различных веществ содержится NA = 6,02·1023 молекул (число Авогадро). Закон Дальтона. Давление смеси идеальных газов равно сумме парциальных давлений р, входящих в неё газов р = р1 + р2 + ... + рn (р1 – давление, которое оказывал бы определённый газ из смеси, если бы он занимал весь объём)

Объединённый газовый закон (Закон Клапейрона). Из законов Бойля – Мариотта и Гей – Люссака можно сделать заключение, что для данной массы газа

Уравнение состояния идеального газа - уравнение Менделеева - Клапейрона. Идеальный газ - газ, молекулы которого пренебрежимо малы, по сравнению расстояния между ними, и не взаимодействуют друг с другом на расстоянии. МЕНДЕЛЕЕВ объединил известные законы Бойля-Мариотта, Гей – Люсака и Шарля с законом Авогадро. m – масса газа; μ – молярная масса газа; R – универсальная газовая постоянная; V – объём газа; – это уравнение Менделеева – Клапейрона для смеси газов

ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Внутренняя энергия. Работа и теплота. под внутренней энергией в термодинамике подразумевают энергию теплового хаотического движения молекул Тогда: внутренняя энергия U одного моля идеального газа равна Обмен механической энергией характеризуется совершенной работой (А), а обмен внутренней энергии – количеством переданного тепла (Q).

Внутренняя энергия. Работа и теплота. U = Q – А изменение внутренней энергии тела равно разности сообщаемой телу теплоты и произведённой телом работы Q = U + А количество теплоты, сообщаемой телу идёт на увеличение внутренней энергии и на совершение телом работы Или Это есть первое начало термодинамики или закон сохранения энергии в термодинамики. dQ = dU + dA. Если U = 0, то согласно первому началу термодинамики А = Q т.е. нельзя построить периодически действующий двигатель, который совершал бы большую работу, чем количество сообщенной ему энергии. Иными словами вечный двигатель первого рода невозможен. Это одна из формулировок первого начала термодинамики.

Теплоёмкость идеального газа. Уравнение Майера. Теплоёмкость тела характеризуется количеством теплоты, необходимой для нагревания этого тела на один градус Удельная теплоёмкость (Суд) – есть количество теплоты, необходимое для нагревания единицы массы вещества на один градус [Cуд] = Дж/К. молярной теплоемкостью Сμ количество теплоты необходимое для нагревания 1 кмоля газа на 1 градус Сμ = Суд μ молярная масса – масса одного моля: Μ = А mед NА где А – атомная масса; mед атомная единица массы; NА число Авогадро; μ (моль) – количество вещества

Теплоёмкость идеального газа. Уравнение Майера. Теплоёмкость термодинамической системы зависит от того, как изменяется состояние системы при нагревании. Если газ нагревать при постоянном объёме СV, то всё подводимое тепло идёт на нагревание газа, то есть изменение его внутренней энергии. Если нагревать газ при постоянном давлении (Ср) в сосуде с поршнем, то поршень поднимется на некоторую высоту h, то есть газ совершит работу. Следовательно проводимое тепло затрачивается и на нагревание и на совершение работы. Ср > CV.

Теплоёмкость идеального газа. Уравнение Майера. Пусть мы нагреваем один моль идеального газа при постоянном объёме, то первое начало термодинамики: d'Q = dU (d'А = 0) Внутренняя энергия идеального газа является только функцией Т (и не зависит от V, Р и тому подобным), поэтому формула справедлива для любого процесса. U = CV T. Для произвольной идеальной массы газа:

Теплоёмкость идеального газа. Уравнение Майера. При изобарическом процессе кроме увеличения внутренней энергии происходит совершение работы газом: d QP = dUμ + рdVμ из основного уравнения молекулярно-кинетической теории рVμ = RT, так как при изобарическом процессе р = const СР = СV + R. Это уравнение Майера для одного моля газа.

Теплоёмкости одноатомных газов Так как энергия одной молекулы идеального газа , то внутренняя энергия одного моля идеального газа равна Внутренняя энергия произвольного количества газа: Её изменение: Теплоёмкости одноатомных газов СV и СР:

Теплоёмкости одноатомных газов для изобарических процессов можно записать: dQP = dUμ + RdT (для одного моля). или внутренняя энергия Учитывая:

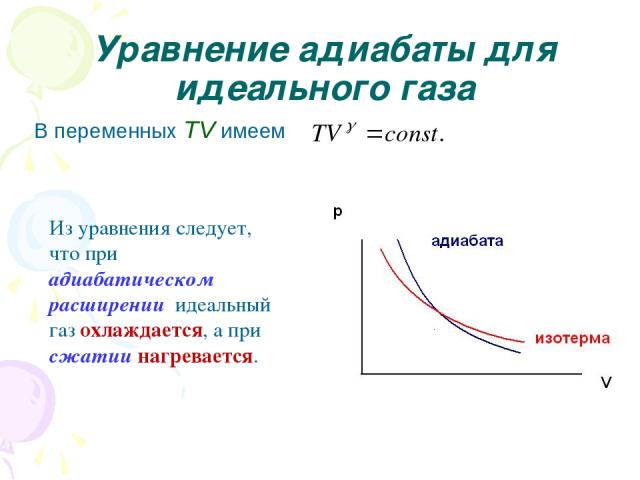
Уравнение адиабаты для идеального газа P = const – изобарический процесс; V = const - изохорический процесс; T = const – изотермический процесс. При изотермическом процессе pV=const (ур. изотермы). Процесс, протекающий без обмена энергий с внешней средой – адиабатический.
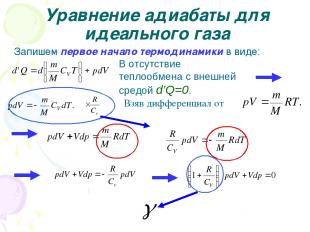
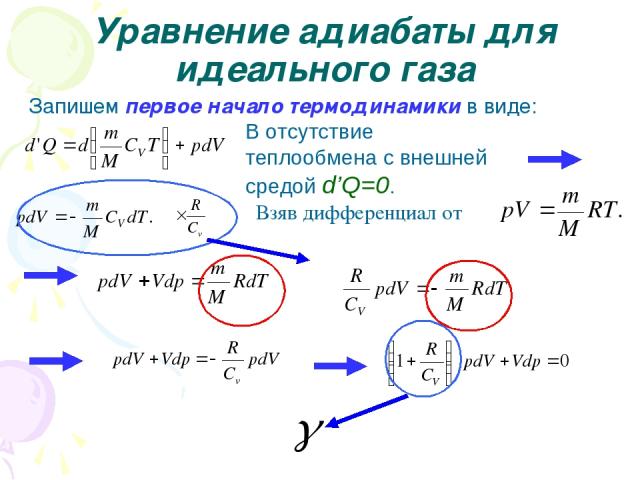
Уравнение адиабаты для идеального газа Запишем первое начало термодинамики в виде: В отсутствие теплообмена с внешней средой d’Q=0. Взяв дифференциал от

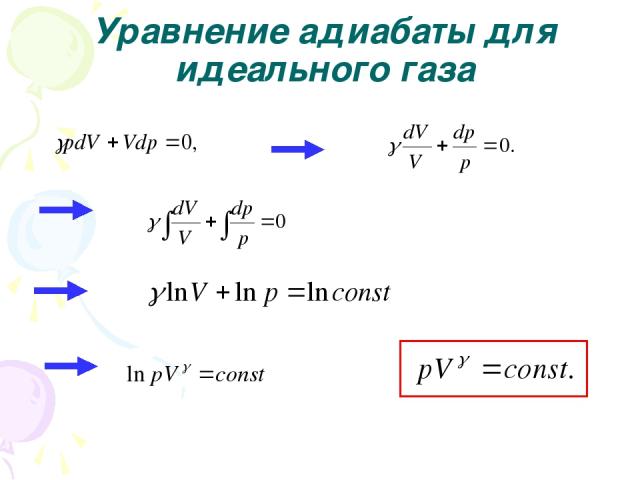
Уравнение адиабаты для идеального газа
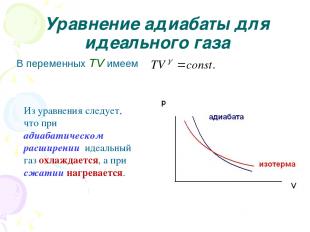
Уравнение адиабаты для идеального газа В переменных TV имеем Из уравнения следует, что при адиабатическом расширении идеальный газ охлаждается, а при сжатии нагревается.

Политропические процессы. Процесс n C Изобарический 0 Cp Изотермический 1 Адиабатический 0 Изохорический СV
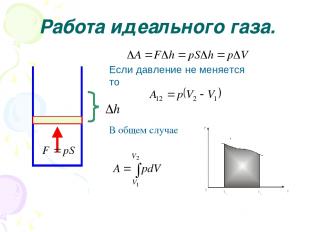
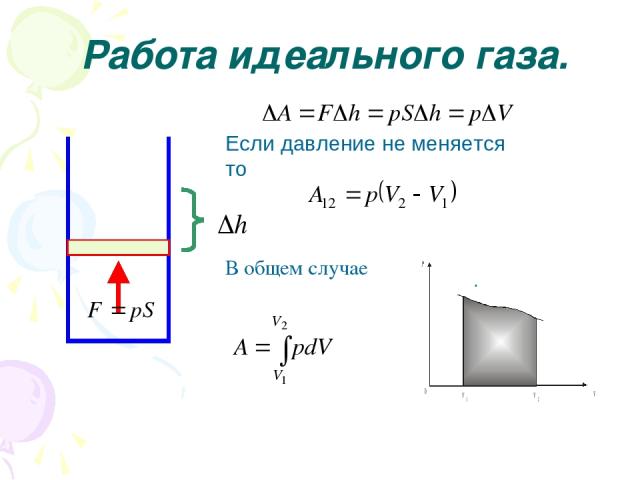
Работа идеального газа. Если давление не меняется то . В общем случае

Работа идеального газа. Работа А не определяется знанием начального и конечного состояния системы. Её значение зависит от способа («пути») перехода из начального в конечное состояние. Рассмотрим работу, совершаемую 1 молем идеального газа при изотермическом (T=const) процессе. Учитывая PV = RT = const, имеем

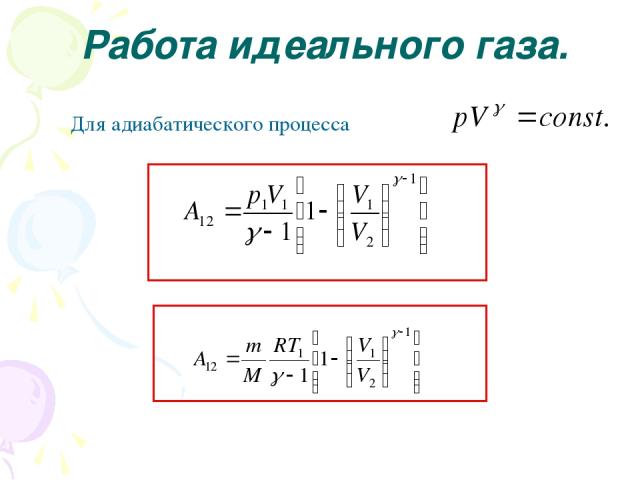
Работа идеального газа. Уравнение политропы идеального газа откуда , и работа При Используя Эта формула справедлива для любого политропического процесса, кроме процесса изотермического (n=1).

Работа идеального газа. Для адиабатического процесса

СТАТИСТИЧЕСКАЯ ФИЗИКА Сведения из теории вероятности Случайная величина может иметь значения: В результате измерений получили: - относительная частота.

Сведения из теории вероятности Теорема о сложении вероятностей: Пусть система характеризуется x и y вероятность которых, равна: - теорема об умножении вероятностей: вероятность одновременного появления статически независимых событий равна произведению вероятностей этих событий Среднее значение

Сведения из теории вероятности Непрерывная случайная величина характеризуется функцией распределения вероятности

Характер теплового движения В равновесии в газе молекулы движутся хаотически. Изменение скоростей при столкновениях происходит случайным образом. Скорость молекул газа не может быть больше некоторой Давление газа на стенку - число молекул в единице объёма, m - масса молекулы ‹v›- средняя скорость молекул ‹Ek› - средняя кинетическая энергия поступательного движения молекул Средняя энергия молекул

Характер теплового движения Так как Здесь учтена только энергия поступательного движения. Наряду с поступательным движением возможны также вращение молекулы и колебание атомов, входящих в состав молекулы. Числом степеней свободы механической системы называется число независимых величин, с помощью которых может быть задано положение системы.

Характер теплового движения Материальная точка задаётся 3-мя координатами; Твердое тело - 3-мя координатами и 2-мя углами и т.д. Закон равнораспределения – на каждую степень свободы молекулы приходится в среднем одинаковая кинетическая энергия, равная

Характер теплового движения Для идеального газа
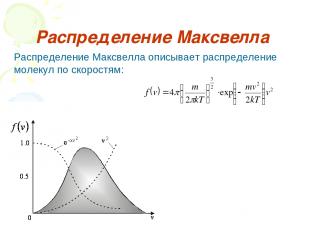
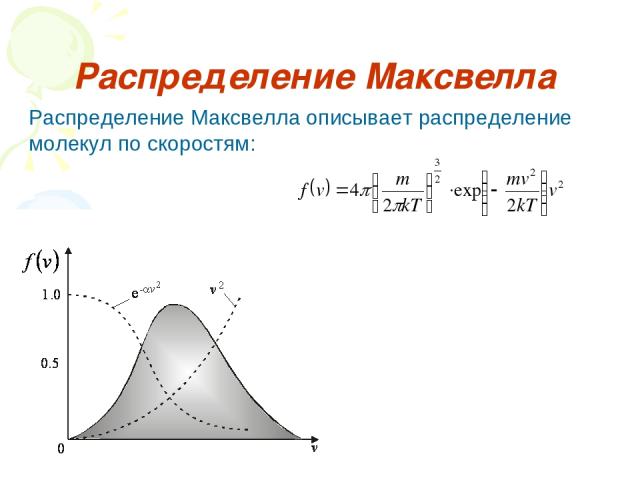
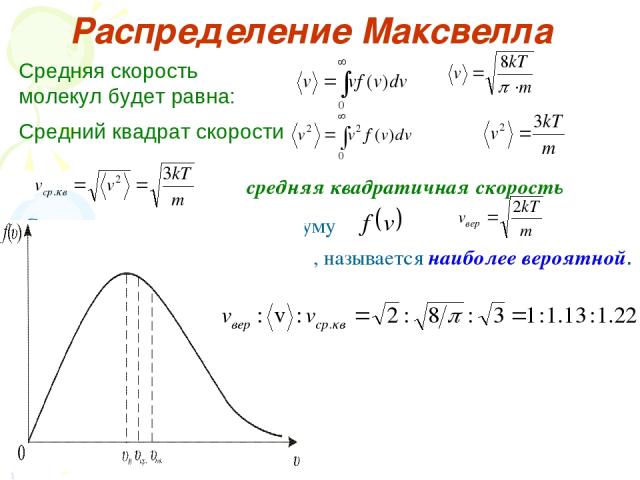
Распределение Максвелла Распределение Максвелла описывает распределение молекул по скоростям:
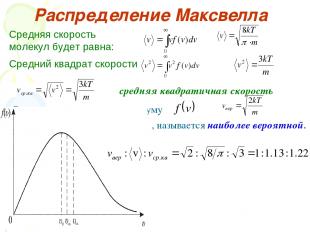
Распределение Максвелла Средняя скорость молекул будет равна: Средний квадрат скорости средняя квадратичная скорость Скорость, отвечающая максимуму , называется наиболее вероятной.
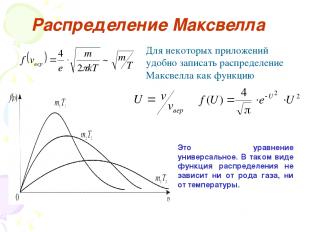
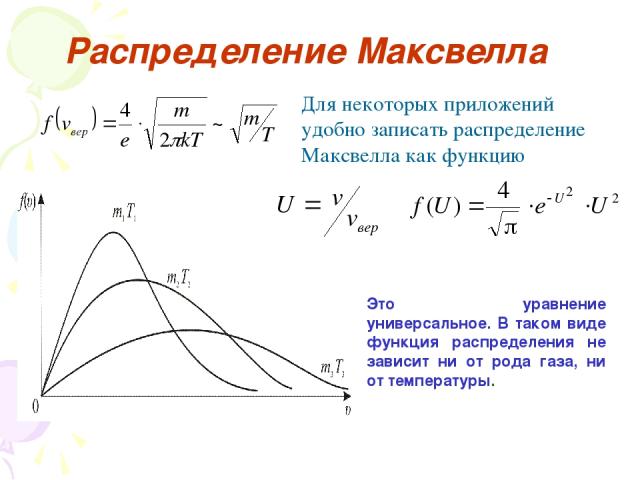
Распределение Максвелла Для некоторых приложений удобно записать распределение Максвелла как функцию Это уравнение универсальное. В таком виде функция распределения не зависит ни от рода газа, ни от температуры.

Распределение Максвелла Используя очевидное соотношение Таким образом распределение Максвелла – это распределение молекул по кинетической энергии.

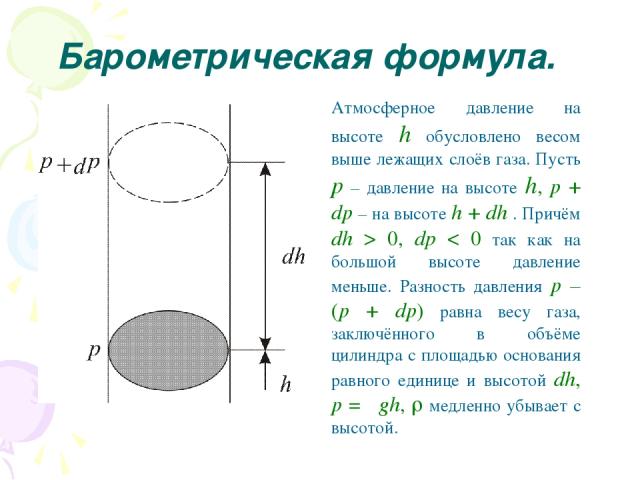
Барометрическая формула. Атмосферное давление на высоте h обусловлено весом выше лежащих слоёв газа. Пусть p – давление на высоте h, p + dp – на высоте h + dh . Причём dh > 0, dр < 0 так как на большой высоте давление меньше. Разность давления p – (p + dp) равна весу газа, заключённого в объёме цилиндра с площадью основания равного единице и высотой dh, p = ρgh, медленно убывает с высотой.
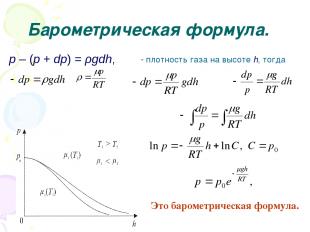
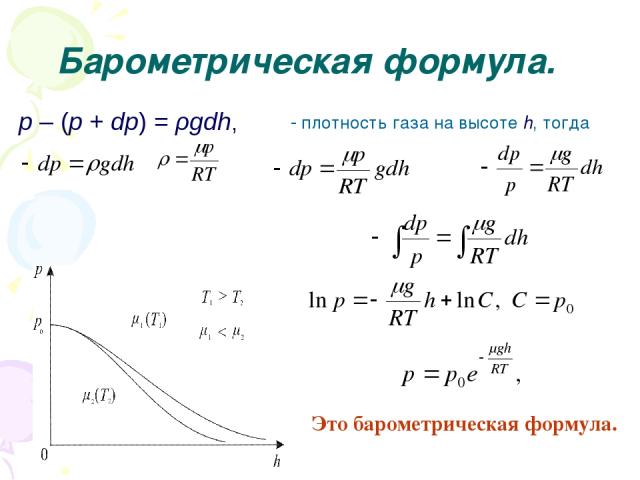
Барометрическая формула. p – (p + dp) = ρgdh, ρ плотность газа на высоте h, тогда Это барометрическая формула.

РАСПРЕДЕЛЕНИЕ БОЛЬЦМАНА . Плотность частиц равна В гравитационном поле Земли n0 – плотность молекул на уровне моря, p0 – давление уровне моря, h - высота. В центрифуге n0 и p0 плотность частиц и давление в центре центрифуги, r – расстояние от центра

РАСПРЕДЕЛЕНИЕ БОЛЬЦМАНА . Таким образом, молекулы располагаются с большей плотностью там, где меньше их потенциальная энергия Распределение Максвелла и Больцмана можно объединить в один закон Максвелла – Больцмана A – нормировочная константа, U – потенциальная mv2/2 – кинетическая, E = U + mv2/2 – полная энергия. N0 –полное число молекул

Распределение Бозе – Эйнштейна, Ферми – Дирака. Если у нас имеется термодинамическая система состояния из N частиц, энергии которых могут принимать дискретные значения (W1, W2 ... Wn), то говорят о системе квантовых чисел. Распределение Бозе – Эйнштейна: Распределение Ферми – Дирака: квантовые частицы с целым спином (собственный момент движения) - бозоны (например фотоны) квантовые частицы с полуцелым спином - фермионы, например: электроны, протоны, нейтроны
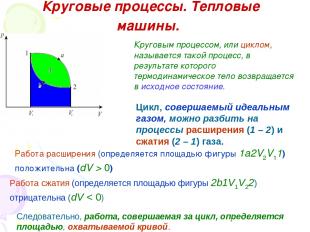
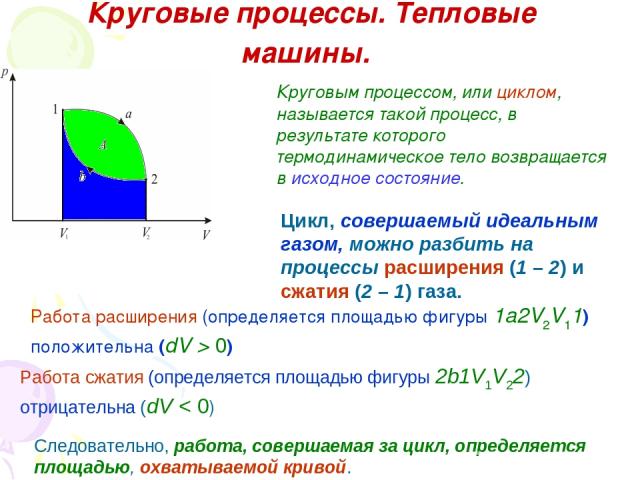
Круговые процессы. Тепловые машины. Круговым процессом, или циклом, называется такой процесс, в результате которого термодинамическое тело возвращается в исходное состояние. Цикл, совершаемый идеальным газом, можно разбить на процессы расширения (1 – 2) и сжатия (2 – 1) газа. Работа расширения (определяется площадью фигуры 1a2V2V11) положительна (dV > 0) Работа сжатия (определяется площадью фигуры 2b1V1V22) отрицательна (dV < 0) Следовательно, работа, совершаемая за цикл, определяется площадью, охватываемой кривой.

Круговые процессы. Тепловые машины. Если за цикл совершается положительная работа то он называется прямым Если за цикл совершается отрицательная работа он называется обратным

Круговые процессы. Тепловые машины. В результате кругового процесса система возвращается в исходное состояние, полное изменение внутренней энергии газа равно нулю. Первое начало термодинамики для кругового процесса Q = U + A = A работа, совершаемая за цикл, равна количеству полученной извне теплоты система может теплоту как получать, так и отдавать Q = Q1 – Q2 коэффициент полезного действия

Круговые процессы. Тепловые машины. Процесс называют обратимым, если он протекает таким образом, что после окончания процесса он может быть проведен в обратном направлении через все те же промежуточные состояния, что в прямом процесс. никаких изменений в среде, окружающей систему, не произойдет Процесс называется необратимым, если он протекает так, что после его окончания систему нельзя вернуть в начальное состояние через прежние промежуточные состояния Нельзя осуществить необратимый круговой процесс, чтобы нигде в окружающей среде не осталось никаких изменений. Максимальным КПД обладают машины у которых только обратимые процессы.
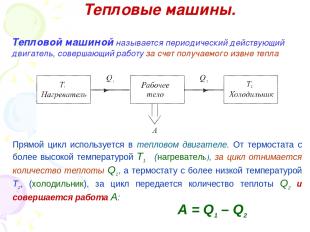
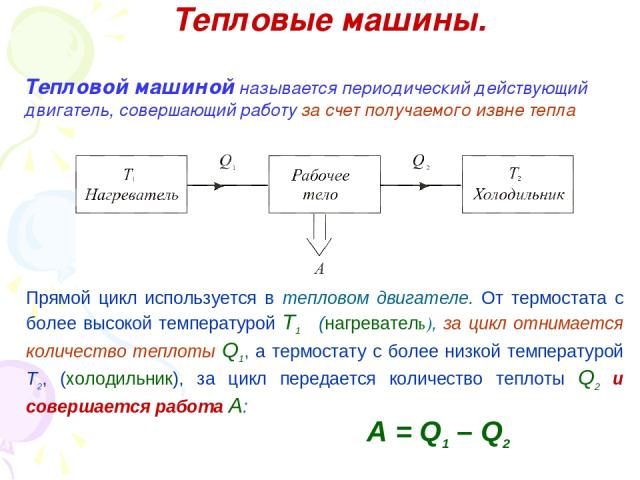
Тепловые машины. Тепловой машиной называется периодический действующий двигатель, совершающий работу за счет получаемого извне тепла Прямой цикл используется в тепловом двигателе. От термостата с более высокой температурой Т1 (нагреватель), за цикл отнимается количество теплоты Q1, а термостату с более низкой температурой Т2, (холодильник), за цикл передается количество теплоты Q2 и совершается работа A: A = Q1 – Q2
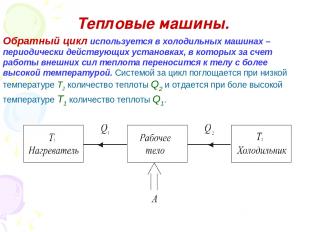
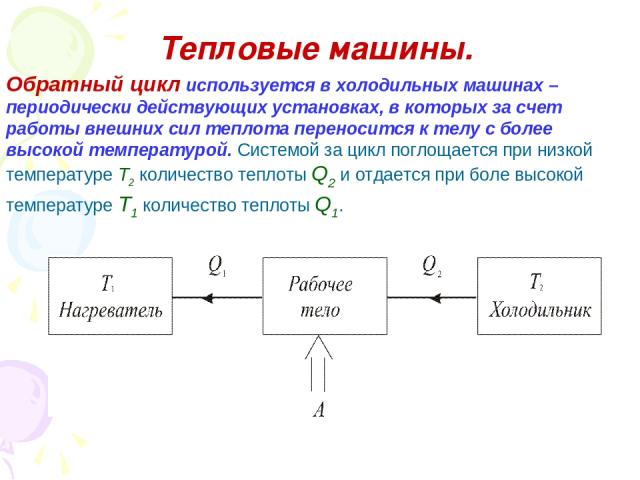
Тепловые машины. Обратный цикл используется в холодильных машинах – периодически действующих установках, в которых за счет работы внешних сил теплота переносится к телу с более высокой температурой. Системой за цикл поглощается при низкой температуре Т2 количество теплоты Q2 и отдается при боле высокой температуре Т1 количество теплоты Q1.
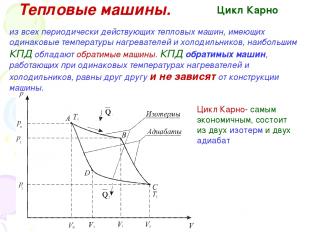
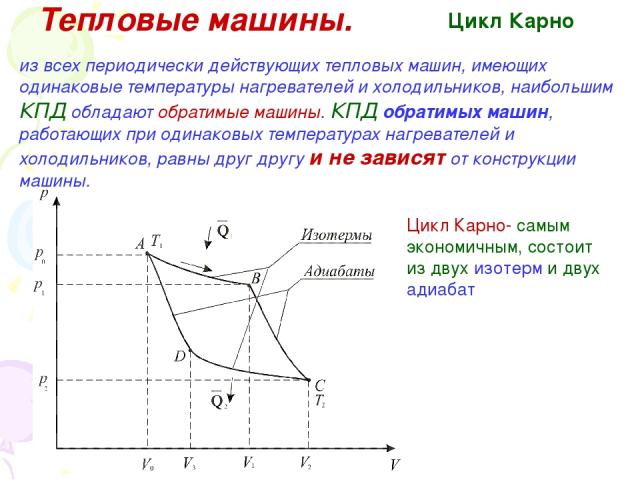
Тепловые машины. Цикл Карно из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей и холодильников, наибольшим КПД обладают обратимые машины. КПД обратимых машин, работающих при одинаковых температурах нагревателей и холодильников, равны друг другу и не зависят от конструкции машины. Цикл Карно- самым экономичным, состоит из двух изотерм и двух адиабат

Тепловые машины. Работа и КПД цикла Карно Процесс А-В. Положительная работа, совершенная газом при изотермическом расширении одного моля газа от V0 до V1. Тепло, полученное от нагревателя Q1, изотермически расширяется совершая при этом работу А1: Процесс В-С – адиабатическое расширение. Работа расширения А2 совершается за счет изменения внутренней энергии. Уравнение адиабаты: Полученная работа на этой стадии

Тепловые машины. Работа и КПД цикла Карно Процесс С-D – изотермическое сжатие. На третьем этапе газ изотермический сжимается V2 до V3. Теплота Q2, отданная газом холодильнику при изотермическом сжатии, равна работе сжатия А3 – это работа совершаемая над газом: Q2 – тепло, отданное холодильнику работа сжатия на последнем этапе:

Тепловые машины. Работа и КПД цикла Карно Значит работа совершаемая газом больше работы внешних сил: Работа равна площади ограниченной кривой АВСDА. Из равенств следует: полезная работа А = Q1 Q2. КПД η равен:

Тепловые машины. Необратимый цикл. Холодильная машина. Предположим, что необратимость цикла обусловлена тем, что теплообмен между рабочим телом и источником теплоты (холодильник - “источник”, отрицательной температуры) происходит при конечных разностях температур, т.е. нагреватель, отдавая тепло, охлаждается на ∆T, а холодильник нагревается на ΔТ. Для необратимого цикла ηобр > ηнеобр
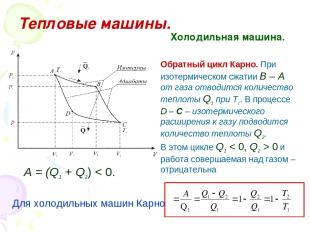
Тепловые машины. Холодильная машина. Обратный цикл Карно. При изотермическом сжатии В – А от газа отводится количество теплоты Q1 при Т1. В процессе D – С – изотермического расширения к газу подводится количество теплоты Q2. В этом цикле Q1 < 0, Q2 > 0 и работа совершаемая над газом – отрицательна А = (Q1 + Q2) < 0. Для холодильных машин Карно

ЭНТРОПИЯ. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. Из цикла Карно видно, что равны между собой отношения теплот к температурам, при которых они были получены или отданы: в изотермическом процессе Отношение теплоты Q1, в изометрическом процессе, к температуре, при которой происходила передача теплоты, называется приведенной теплотой Q*. в обратном цикле Карно имеем: Этот результат справедлив для любого обратимого процесса.

ЭНТРОПИЯ. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. Из равенства нулю интеграла взятого по замкнутому контуру, следует, что полный дифференциал некоторой функции, которая определяется только состоянием системы и зависит от пути, каким система пришла в это состояние. Функция состояния, дифференциал которой , называется – энтропией. Энтропия обозначается S – это отношение полученной или отданной теплоты к температуре при которой произошла эта отдача. Для обратимых процессов изменение энтропии равенство Клаузиуса

ЭНТРОПИЯ. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. Если система совершает равновесный переход из состояния 1 в состояние 2, то изменение энтропии: Последняя формула определяет энтропию лишь с точностью до аддитивной постоянной, т.е. начало энтропии произвольно.

ЭНТРОПИЯ. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. найдем изменения энтропии в процессах идеального газа используя

ЭНТРОПИЯ. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. изменение энтропии S1 2 идеального газа при переходе его из состояния 1 в состояние 2 зависит от вида перехода 1 2. изохорического процесса: изобарического процесса: p1 = p2 изотермического процесса: Т1 = Т2 адиабатного процесса: то S = const, адиабатный процесс по другому называют – изоэнтропийным процессом

Изменения энтропии при обратимых и необратимых процессах . Обратимый цикл Карно. Энтропия (S) – величина аддитивная, т.е. она равна сумме всех тел входящих в систему. так как газ возвращается в исходное состояние так как

Изменения энтропии при обратимых и необратимых процессах . Необратимый цикл. ηобр > ηнеобр, т.е. При любом необратимом процессе в замкнутой системе энтропия возрастает dS > 0. Таким образом для произвольного процесса где «=» – для обратимого; «>» для необратимого, и для замкнутой системы

Изменения энтропии при обратимых и необратимых процессах . ЭНТРОПИЯ. Второе начало термодинамики. Второе начало термодинамики. A = Q1 – Q2. Работа теплового двигателя. Чтобы кпд теплового двигателя был = 1, должно быть выполнено условие Q2 = 0 вечный двигатель Второго рода Невозможно создание вечного двигателя Второго рода подтверждается вторым началом термодинамики: М. Карно доказал, что для работы теплового двигателя необходимо не менее двух источников теплоты с различными температурами.

Изменения энтропии при обратимых и необратимых процессах . Невозможен процесс, единственным результатом которого является превращение всей теплоты, полученной от нагревателя в эквивалентной ей работе (формулировка Кельвина). Невозможен двигатель Второго рода (Томсон-Планк). Невозможен процесс, единственным результатом которого является передача энергии в форме теплоты от холодного тела к горячему (Клаузиус). Второе начало термодинамики. dS 0

Изменения энтропии при обратимых и необратимых процессах . Второе начало термодинамики. При обратном процессе Клаузиус доказал, что при необратимом процессе изменение энтропии больше приведенной теплоты, тогда dQ < TdS можно объединить, тогда тогда первое и второе начала термодинамики в объединенной форме будут иметь вид: dS > dQ

Изменения энтропии при обратимых и необратимых процессах . Свободная и связанная энергии в обратимом процессе: F – разность двух функций состояния, а поэтому и сама является функцией состояния. Ее назвали свободной энергией. Если тело совершает обратный изометрический процесс, то dT = 0,

Изменения энтропии при обратимых и необратимых процессах . Аизот = F1 – F2 - свободная энергия есть работа, которая могло бы совершить тело в обратном изотермическом процессе или, Свободная и связанная энергии свободная энергия – есть максимальная возможная работа, которую может совершить система, запасом внутренней энергии: U = F + TS Внутренняя энергия системы равна сумме свободной (F) и связанной энергии (TS). Связанная энергия – часть внутренней энергии, которая не может быть превращена в работу

Изменения энтропии при обратимых и необратимых процессах . При одной и той же температуре, связанная энергия тем больше, чем больше энтропия. Свободная и связанная энергии При необратимом процессе энтропия увеличивается, до того пока не прекратятся какие-либо процессы (F = 0). Это произойдет, при достижении замкнутой системы равновесного состояния. Вывести систему из этого равновесного состояния можно затратив энергию из вне. В термодинамике есть еще понятие – энергетическая потеря в изолированной системе Tmin температура окружающей среды.

Статистический смысл энтропии. Макросостояние – это состояние вещества характеризующее его термодинамические параметры. Состояние же системы, характеризуемое состоянием каждой входящей в систему молекулы называют – микросостояниями. Термодинамической вероятностью или статистическим весом макросостояния W называется число микросостояний, которым она может быть осуществлена Термодинамическая вероятность W максимальна, когда система находится в равновесном состоянии. В состоянии равновесия энтропия максимальна

Статистический смысл энтропии. S – аддитивная величина. где S энтропия системы; сумма энтропий тел, входящих в систему. Вероятность сложного события где W1 – первое состояние; W2 – второе состояние. Поэтому аддитивной величиной является логарифм W: Поэтому Больцман предложил

Статистический смысл энтропии. Связь между S и W позволяет несколько иначе сформулировать второе начало термодинамики: Наиболее вероятным изменением энтропии является ее возрастание. Энтропия – вероятностная статистическая величина. Энтропия системы – максимальна, при достижении системы (замкнутой) равновесного состояния.

Третье начало термодинамики . Энтропия любой равновесной системы при абсолютном нуле температуры равна нулю. Отсюда следует, что при T 0 сходится на нижнем пределе S(0) = const или S(0) = 0, равенство нулю рассматривается как наиболее вероятное теорема Нернста

Третье начало термодинамики . Третье начало термодинамики иногда формулируют следующим способом: при абсолютном нуле температуры любые изменения термодинамической системы происходят без изменения энтропии ST = 0 =0. Принцип Нернста бал развит Планком, предложившим при абсолютном нуле температуры энергия системы минимальна ST = 0 = 0, Следствием Третьего начала является, то что невозможно охладить тело до абсолютного нуля (принцип недостижимости абсолютного нуля температуры).

Термодинамические потенциалы. Термодинамические потенциалы – функции состояния. Внутренняя энергия Свободная энергия: Энтальпия: Термодинамический потенциал Гиббса: ,