Презентация на тему: Строение ядра атома

СОДЕРЖАНИЕ 1 модуль 1. Строение атома. Опыты Резерфорда. 2. Модель атома Резерфорда. 3. Радиоактивное превращение атомных ядер. 4. Состав атомного ядра. 5. Деление ядер урана. 6. Ядерный реактор. 7. Использование атомной энергии. 2 модуль 1. и распад. 2. Закон сохранения массового и зарядового числа. 3. Изотопы. 4. Термоядерная реакция. 2 - 4 5 7 - 9 6 13 - 15 10 -12 16 18 17 19 20 900igr.net

1896 г. Анри Беккерель (франц.) открыл явление радиоактивности. Радиоактивность – способность атомов к самопроизвольному излучению. 1899 г. Эрнест Резерфорд обнаружил, что это излучение неоднородно.

Опыты Резерфорда 1. В толстостенный свинцовый сосуд положили крупицу радия. Излучение радия обнаружили с помощью фотопластинки. 2. Вокруг цилиндра создали сильное магнитное поле. Излучение разделилось на три потока. Следовательно, излучение состоит из потоков положительных частиц, отрицательных и нейтральных. Положительные назвали альфа-частицами ( - частицы); Отрицательные – бета-частицы ( - частицы); Нейтральные – гамма-частицы ( - частицы) или - квантами или фотонами. N S
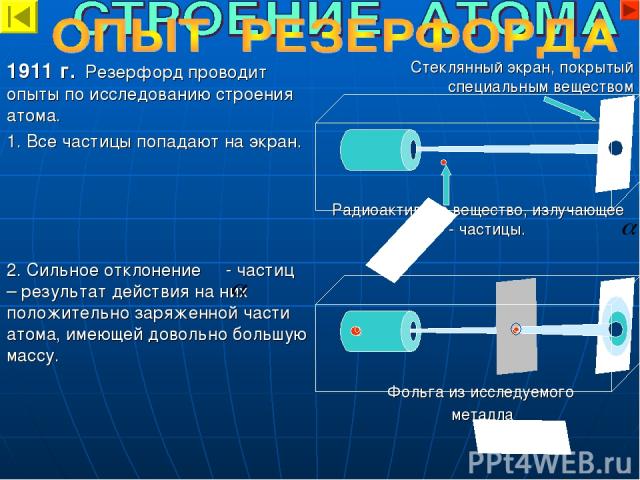
Стеклянный экран, покрытый специальным веществом Радиоактивное вещество, излучающее - частицы. Фольга из исследуемого металла 1911 г. Резерфорд проводит опыты по исследованию строения атома. 1. Все частицы попадают на экран. 2. Сильное отклонение - частиц – результат действия на них положительно заряженной части атома, имеющей довольно большую массу.

- частицы ядро По Резерфорду атом имеет планетарное строение. В центре находится положительно заряженное ядро. Вокруг ядра движутся электроны. Атом нейтрален, т.к. заряд ядра равен общему заряду электронов. Такое строение атома объясняет поведение - частиц

1903 г. Эрнест Резерфорд и Фредерик Содди обнаружили, что при - распаде происходит превращение одного химического элемента в другой. Реакция - распада: + В дальнейшем было установлено, что превращение происходит и при - распаде. + + Ядро - частица - излучение электрон - излучение ВЫВОД Ядра атомов состоят из более мелких частиц.

1919 г. Резерфорд исследовал взаимодействие - частиц с ядрами атомов азота. При этом, из ядра атома азота вылетала частица, которую он назвал протоном (первый). Позднее с помощью камеры Вильсона было доказано, что это действительно положительно заряженная элементарная частица, которая является ядром атома водорода. Кроме того, образовалось ядро атома кислорода. + + - ядро атома водорода или протон. Обозначается - , имеет массу ≈ 1а.е.м. и заряд равный заряду электрона.

1920 г. Резерфорд предполагает существование в ядре нейтральной частицы с массой равной массе протона. В 30-х гг. при бомбардировке ядер бериллия - частицами было обнаружено новое излучение, которое назвали бериллиевым. 1932 г. Джеймс Чедвиг (англ.) доказал, что бериллиевое излучение - это поток электрически нейтральных частиц с массой равной массе протона. Эти частицы назвали нейтронами.

N – число нейтронов 1932 г. Д.Д.Иваненко (рус.), В.Гейзенберг (нем.) предложили протонно-нейтронную модель строения ядра: ядро состоит из протонов и нейтронов – нуклонов. ПРИМЕР. А = 56, Z = 26, N = 30 Общее число нуклонов в ядре называется массовым числом и обозначается А Число протонов в ядре называется зарядовым числом и обозначается Z X A Z A = Z+N Число протонов для данного элемента постоянное. Число нейтронов может быть больше числа протонов, оно может меняться(получаем ИЗОТОПЫ вещества)

1939 г. Отто Ган и Фриц Штрассман (нем.) открыли деление ядер урана. Ядра урана бомбардируют нейтронами. Если нейтрон попадает в нестабильное ядро, то оно делится на два более стабильных ядра, которые разлетаются с огромной скоростью. При этом они испускают 2-3 нейтрона. Осколки ядра тормозятся и при этом передают свою энергию окружающей среде


ФАКТОРЫ, ВЛИЯЮЩИЕ НА ПРОТЕКАНИЕ ЦЕПНОЙ РЕАКЦИИ 1. МАССА УРАНА. 2. НАЛИЧИЕ ОТРАЖАЮЩЕЙ ОБОЛОЧКИ (бериллий). 3. НАЛИЧИЕ ПРИМЕСЕЙ. 4. НАЛИЧИЕ ЗАМЕДЛИТЕЛЯ НЕЙТРОНОВ – графит, вода, тяжелая вода. Наименьшая масса урана, при которой возможно протекание цепной реакции, называется критической массой
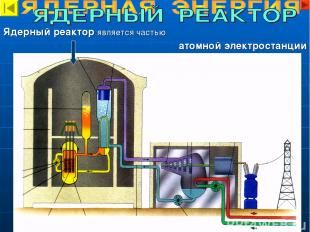
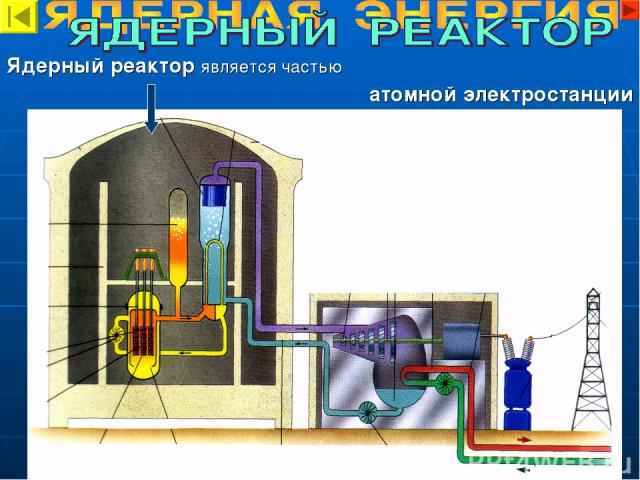
Ядерный реактор является частью атомной электростанции
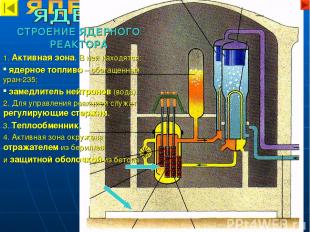
СТРОЕНИЕ ЯДЕРНОГО РЕАКТОРА 1. Активная зона. В ней находятся: ядерное топливо – обогащенный уран-235; замедлитель нейтронов (вода). 2. Для управления реакцией служат регулирующие стержни. 3. Теплообменник. 4. Активная зона окружена отражателем из бериллия и защитной оболочкой из бетона

ПРИНЦИП ДЕЙСТВИЯ ЯДЕРНОГО РЕАКТОРА 1. В активной зоне происходит управляемая ядерная реакция, в результате которой выделяется энергия. 2. Энергия передается воде. 3. Горячая вода поступает в теплообменник, где нагревает воду, превращая ее в пар. 4. Вода остывает и возвращается в активную зону. Это первый замкнутый контур. 5. Пар вращает турбину (отдает ей свою энергию) и конденсируется. 6. Насос перекачивает воду в теплообменник. Это второй замкнутый контур.

1. АТОМНЫЕ ЭЛЕКТРОСТАНЦИИ. 1942 г. Под руководством Э.Ферми в США был построен первый ядерный реактор. 1946 г. Под руководством И.В.Курчатова был создан первый ядерный реактор в СССР. 1954 г. В СССР была введена в действие первая в мире атомная станция. 2. Техника. 1. Космические корабли. 2. Атомные ледоколы. 3. Атомные подводные лодки. 3. Ядерное оружие.

ПРАВИЛО СМЕЩЕНИЯ ДЛЯ - РАСПАДА При - распаде химического элемента образуется элемент, расположенный в таблице Д.И.Менделеева на 2 клетки ближе к ее началу. При - распаде ядро радиоактивного элемента излучает - частицу и образуется ядро другого химического элемента, зарядовое число которого на 2 единицы меньше, чем у исходного. При - распаде ядро радиоактивного элемента излучает электрон ( - частицу) и нейтральную частицу – антинейтрино. В результате число протонов в ядре увеличивается на единицу, т.е. увеличивается зарядовое число, образуется новый химический элемент. - распад - распад 222 226 88 4 2 86 40 -1 20 19 40 0 0 0 ПРАВИЛО СМЕЩЕНИЯ ДЛЯ - РАСПАДА При - распаде химического элемента образуется элемент, расположенный в таблице Д.И.Менделеева на 1 клетку ближе к ее концу. Rn Ra + He e K Ca + +

Массовые числа химических элементов. Зарядовые числа химических элементов. 222 226 88 4 2 86 Rn Ra + He ЗАКОН СОХРАНЕНИЯ МАССОВОГО ЧИСЛА И ЗАРЯДА. В процессе радиоактивного распада массовое число и заряд распадающегося ядра атома равны суммам массовых чисел и зарядов образовавшихся в результате распада веществ.

ИЗОТОПЫ –разновидности химического элемента, различающиеся по массе атомных ядер. 234 92 U 235 92 U 236 92 U 1 1 H 2 1 H 3 1 H ПРИМЕРЫ: 1. Изотопы урана 2. Изотопы водорода - протий - дейтерий - тритий Все химические элементы имеют одинаковое зарядовое число, т.е. одинаковое число протонов, но разное массовое число, т.е. разное число нейтронов. Существование у химических элементов изотопов – причина того, что массовые числа многих элементов числа дробные. ПРИМЕР: 40,078 20 Ca

ПРИМЕР. При слиянии изотопов водорода образуется гелий и излучается нейтрон. При этом выделяется энергия. Для прохождения реакции необходима температура в несколько сотен миллионов градусов (температура в центре Солнца) ТЕРМОЯДЕРНОЙ называется реакция слияния легких ядер (водород, гелий и др.), происходящая при очень высоких температурах. 2 1 Н + Hе 3 1 Н 2 4 n 0 1 +