Презентация на тему: Строение атомов

Общая химия Лектор – Голушкова Евгения Борисовна Лекция 2 – Строение атомов

План лекции План лекции 1. Экспериментальная основа теории 2. Корпускулярно-волновое описание электрона 3. Квантовые числа 4. Принципы построения и способы изображения электронных структур 5. Строение атома и периодическая система элементов

Атом Устойчивая микросистема элементарных частиц, состоящая из положительно заряженного ядра и электронов, движущихся в околоядерном пространстве

Ядро атома состоит из протонов и нейтронов Ядро атома состоит из протонов и нейтронов Число протонов в ядре равно атомному номеру элемента и числу электронов в атоме Атом - электронейтрален
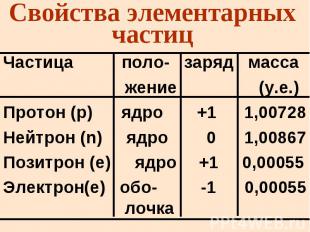
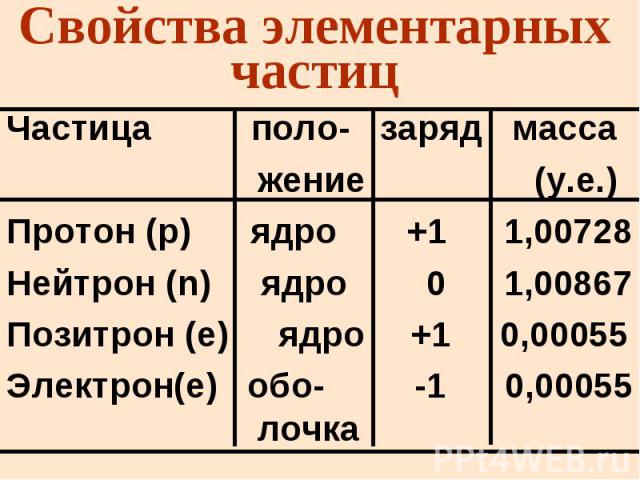
Свойства элементарных частиц Частица поло- заряд масса жение (у.е.) Протон (p) ядро +1 1,00728 Нейтрон (n) ядро 0 1,00867 Позитрон (е) ядро +1 0,00055 Электрон(е) обо- -1 0,00055 лочка

A = Z + N A – массовое число атома Z – заряд ядра (число протонов) N – число нейтронов Э

ИЗОТОПЫ ХЛОРА

Cамостоятельно: Cамостоятельно: Радиоактивные превращения химических элементов Н.С.Ахметов «Общая и неорг. химия» стр.9 - 16

Экспериментальные основы Спектральный анализ, спектры (Г. Кирхгоф, 1859; Дж.Бальмер, 1885, И.Ридберг) Периодический закон (Д.Менделеев 1869) Фотоэффект (А. Столетов, 1888) Катодные лучи (Ж. Перрен, 1895) Рентгеновские лучи (В.Рентген 1895) Радиоактивность (А. Беккерель, 1896) Открытие электрона (Дж. Томпсон, 1897)
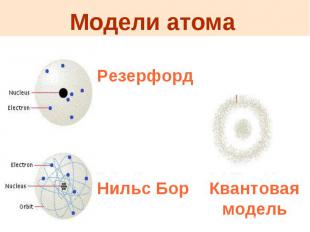
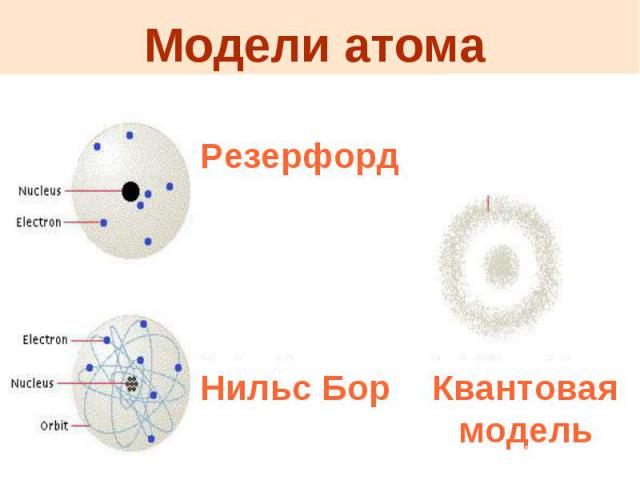
Модели атома
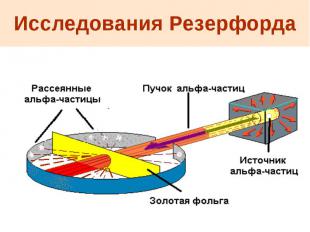
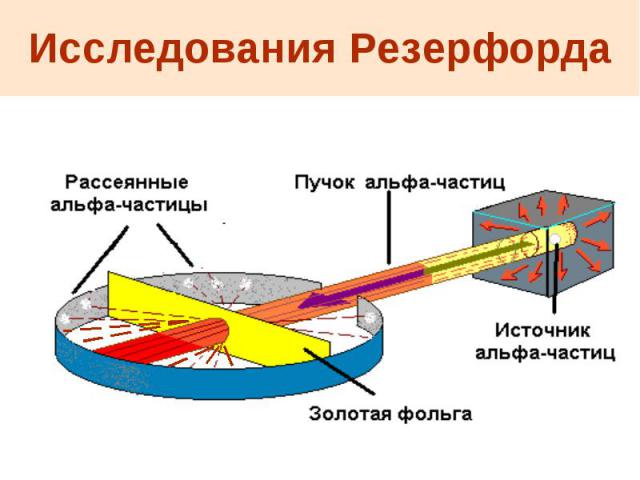
Исследования Резерфорда

Принцип квантования (М. Планк, 1900) атомы излучают энергию порциями, кратными некоторой минимальной величине - кванту, фотону - h h = 6,626•10-34(Дж•c)–пост. Планка

Принцип корпускулярно-волнового дуализма При движении электронов проявляются их волновые свойства При взаимодействии с веществом – корпускулярные волновые и корпускулярные свойства присущи электронам одновременно (Л.Де-Бройль)

Принцип неопределенности (В. Гейзенберг, 1925) Движение электрона в атоме не может быть описано определённой траекторией Положение и скорость движения электрона в атоме можно найти лишь с определенной долей точности

Волновое движение электрона Для струны: Ψ = А·Sin n(π/a)x n – квантовое число а – длинна струны х – координата точки на струне А – максимальная амплитуда колебаний

Квантовые представления Положение электрона характеризуется вероятностью пребывания частицы в конкретной области пространства Область наиболее вероятного пребывания электрона в атоме называют атомной орбиталью - АО Вероятность обнаружения электрона определяется квадратом волновой функцией - 2



Уравнение Шредингера - уравнение трехмерной волны НΨ = Е·Ψ В волновой теории движение эл-на представ-ся в виде стоячей волны, для которой характерен набор колебаний с длинами волн: , /2, /3, ....... /n; т.е. движение характеризуется квант. числом - n

Квантовые числа Уравнение Шредингера - трехмерно. Соответственно - три набора квантовых чисел. Каждой координате свое квантовое число. Размер, энергия, форма и ориентация электронного облака изменяются в атоме скачками (квантами)

Главное квантовое число(n) n - 1, 2, 3,… , определяет энергию электрона в атоме Энергетический уровень - состояние электронов в атоме с тем или иным значением n Основное состояние атома - min энергия электронов Возбужденное состояние – более высокие значения энергии электронов

Орбитальное квантовое число (l) харак-ет форму электронного облака Орбитальное квантовое число (l) харак-ет форму электронного облака l = 0, 1, 2, 3….n-1 Подуровень: s, p, d, f, g, h Т.е. энерг-кий уровень (n) содержит совокупность энерг-ких подуровней, отличающихся по энергиям (в многоэлектронном атоме)
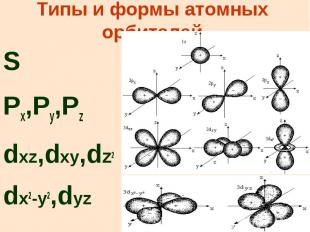
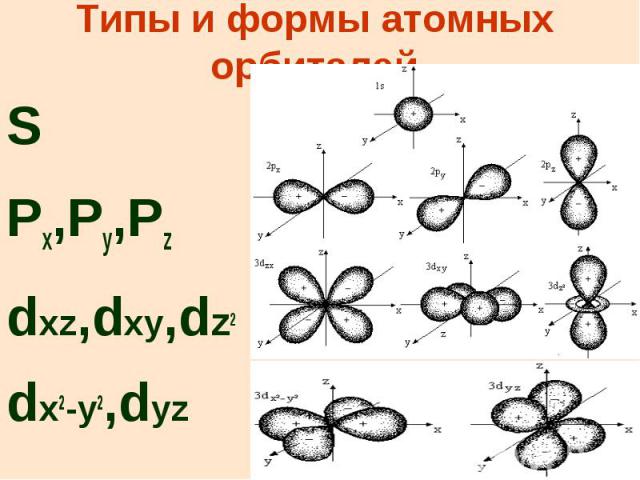
Типы и формы атомных орбиталей S Px,Py,Pz dxz,dxy,dz2 dx2-y2,dyz

Магнитное квантовое число (ml) характеризует ориентацию электронных облаков в пространстве Магнитное квантовое число (ml) характеризует ориентацию электронных облаков в пространстве ml меняется от –l до +l, а всего = 2l + 1 значений Например: l = 0 (s); ml = 0 l = 1 (p); ml = 0, +1, -1

Спиновое квантовое число (ms) характеризует собственный магнитный момент электрона, который или совпадает с ориентацией орбитального момента, или направлен в противоположную сторону. Спиновое квантовое число (ms) характеризует собственный магнитный момент электрона, который или совпадает с ориентацией орбитального момента, или направлен в противоположную сторону. ms имеет значения: +1/2 или -1/2

Атомная орбиталь (АО) это состояние электрона в атоме, которое описывается волновой функцией с набором из трех квантовых чисел n, l, ml Условное изображение АО АО обозначают с помощью кв. чисел Например: 1s (n = 1, l = 0, ml = 0) 2p (n = 2, l = 1, ml = -1, 0, +1)

Закономерности формирования электронных структур Принцип наименьшей энергии: электрон размещается на АО c min энергией Принцип Паули: в атоме не может быть двух электронов с одинаковым набором 4-х кв.чисел Правила Гунда: (1) на одном подуровне сумма спинов электронов максимальна, (2) сумма магнитных кв-х чисел максимальна.

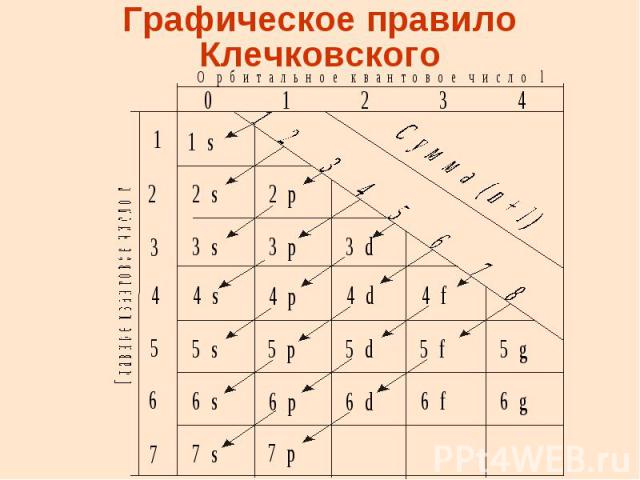
Правила Клечковского Ниже по энергии находится та орбиталь для которой сумма (n + l) минимальна Если сумма (n + l) для двух подуровней одинакова , то сначала эл-ны заполняют АО с меньшим n

Графическое правило Клечковского

Последовательность заполнения АО по правилам Клечковского 1sι 2s2pι 3s3pι 4s3d4pι 5s4d5pι 6s4f5d6pι 7s5f6d7p

Способы изображения электронных структур Электронная формула Графическая структура Энергетическая диаграмма

Примеры электронных структур Полная электронная формула Se - 1s22s22p63s23p64s23d104p4 Краткая формула Se - 4s24p4 Электроно-графическая формула

Энергетическая диаграмма ванадия Е

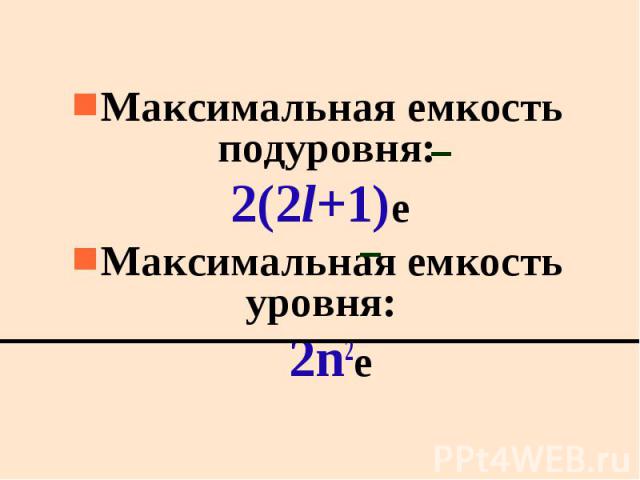
Maксимальная емкость подуровня: Maксимальная емкость подуровня: 2(2l+1)e Максимальная емкость уровня: 2n2е

Проскок электрона Пример: z = 24; Cr Ожидаемая: 1s22s22p63s23p64s23d4 Действительная: 1s22s22p63s23p64s13d5
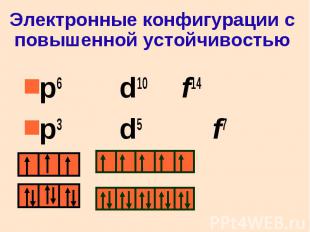
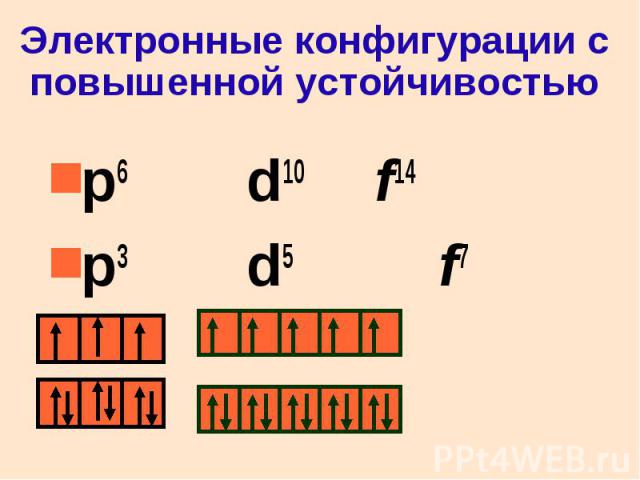
Электронные конфигурации с повышенной устойчивостью p6 d10 f14 p3 d5 f7

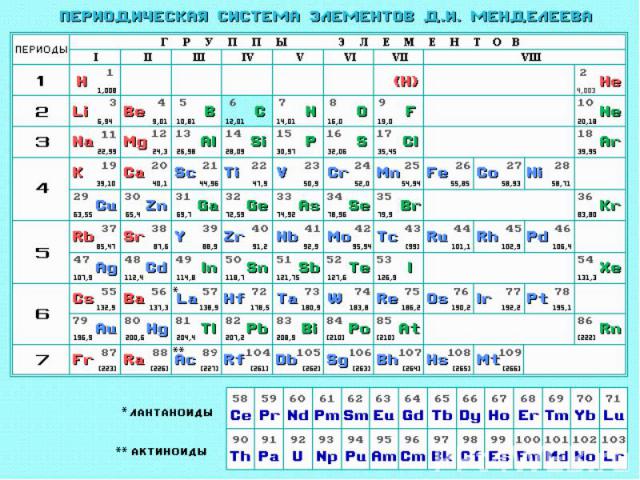
Периодическая система элементов Д.И. Менделеева (1869г.) Свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от их атомных весов

Неясные моменты В чем причина периодичности? Почему элементы одной группы имеют одинаковую валентность и образуют одинаковые соединения? Почему число элементов в периодах не одинаковое? Почему в ПС расположение элементов не всегда соответствует возрастанию атомной массы (Аr – К, Co – Ni, Te – I)?

Периодический закон Свойства элементов, а также формы и свойства их соединений находятся в периодической зависимости от заряда ядер их атомов

Причина периодичности Определенная последовательность формирования электронных оболочек (принципы и правила Паули, Хунда, Клечковского) Периодическое повторение сходных электронных слоёв и их усложнение при увеличении гл. кв. числа: периоды начинаются s-элементами, а заканчиваются р-элементами

Короткие периоды 1 период (n=1): (2n2) 2 элемента (1s2) 2 период (n=2): (2n2) 8 элементов (2s22p6) 3 период (n=3): (2n2 – 2*5) 8 элементов (3s23p6)

Длинные периоды 4 период (n=4): (2n2 -2*7) 18 элементов (4s23d104p6) 5 период (n=5): (2n2 -2(7 + 9) ) 18 элементов (5s24d105p6) 6 период (n=6): (2n2 -2(9 + 11) ) 32 элемента (6s24f145d106p6) 7 период (n=7): (2n2 -2(9 + 11 + 13) ) 32 элемента (7s25f146d107p6), незавершенный

Период - горизонтальная последовательность эл-тов, атомы которых имеют равное число энергетических уровней, частично или полностью заполненных электронами Период - горизонтальная последовательность эл-тов, атомы которых имеют равное число энергетических уровней, частично или полностью заполненных электронами

Группа - вертикальная последовательность элементов с однотипной электроной конфигурацией атомов, равным числом внешних эл-нов, одинаковой max валентностью и похожими химическими свойствами Группа - вертикальная последовательность элементов с однотипной электроной конфигурацией атомов, равным числом внешних эл-нов, одинаковой max валентностью и похожими химическими свойствами


Периодичность свойств элементов атомные и ионные радиусы энергия ионизации сродство к электрону электроотрицательность валентность элементов

Периодичность свойств простых веществ и соединений температура плавления и кипения длина химической связи энергия химической связи электродные потенциалы стандартные энтальпии образования веществ энтропии веществ и т.д.

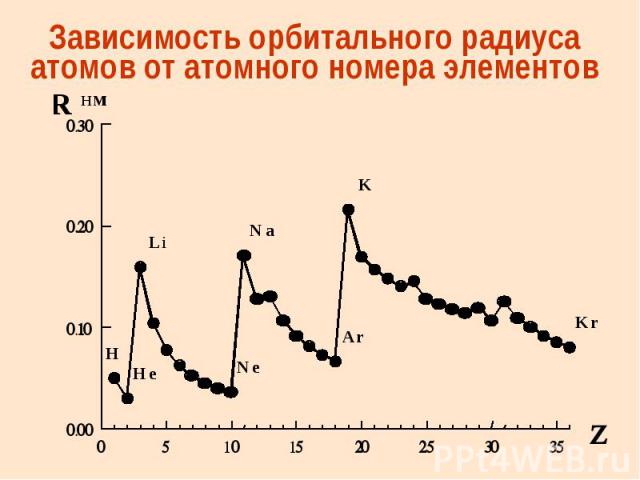
Атомные и ионные радиусы химических элементов Орбитальный радиус атома (иона) – это расстояние от ядра до максимума электронной плотности наиболее удаленной орбитали этого атома


Радиусы катионов и анионов Превращение атома в катион - резкое ум-ие орбитального радиуса Превращение атома в анион почти не изменяет орбитального радиуса Rкат < Rат < Rан Cl+ < Cl < Cl– 0,099 0,181нм
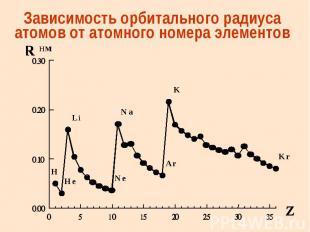
Зависимость орбитального радиуса атомов от атомного номера элементов
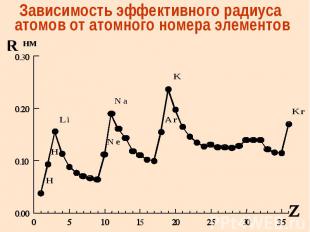
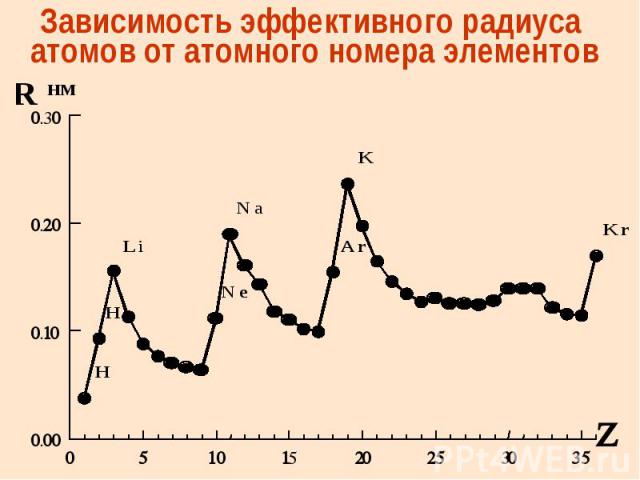
Зависимость эффективного радиуса атомов от атомного номера элементов

Эффективные радиусы Эффективные радиусы атомов и ионов определяют по межъядерным расст-ям в молекулах и кристаллах, предполагая, что атомы – несжимаемые шары

Ковалентные радиусы - это эффективные радиусы, определяемые по межъядерным расстояниям в ковалентных молекулах Ковалентные радиусы - это эффективные радиусы, определяемые по межъядерным расстояниям в ковалентных молекулах Металлические радиусы - это эффективные радиусы в металлах Ионные радиусы – это эффективные радиусы в ионах

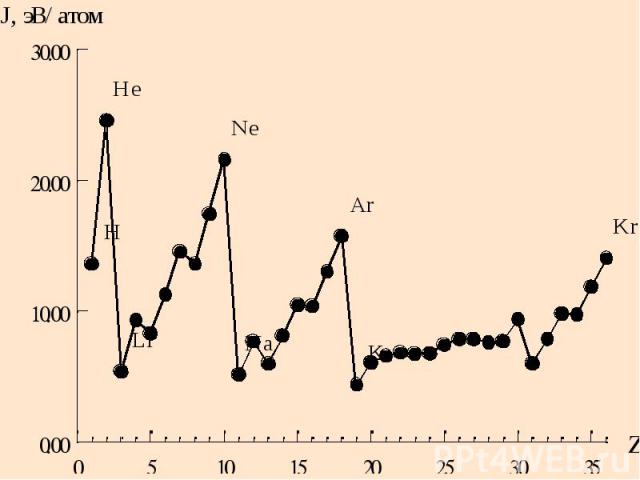
Энергия и потенциал ионизации атомов Энергия ионизации – это энергия, необходимая для отрыва электрона от атома и превращение атома в положительно заряженный ион Э – е = Э+, Еион [кДж/моль] Ионизационный потенциал – это разность потенциалов, при которой происходит ионизация J [эВ/атом]; Еион= 96,5•J

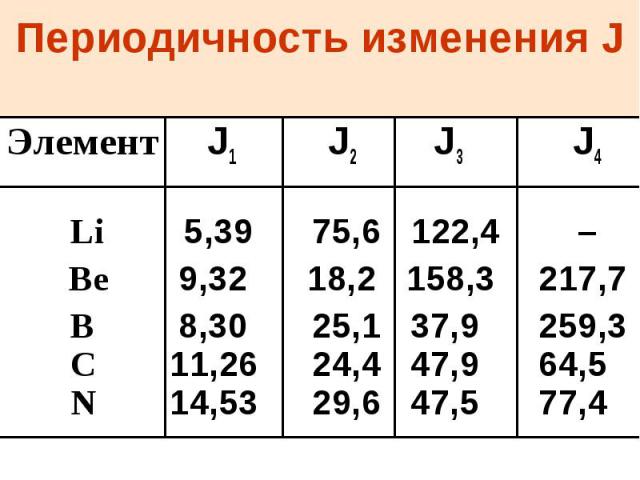
1-й, 2-й, ….i потенциал ионизации Энергия отрыва каждого последующего электрона больше, чем предыдущего J1 < J2<J3<J4…… Резкое увеличение J происходит тогда, когда заканчивается отрыв внешних электронов и следующий электрон находится на предвнешнем энергетическом уровне
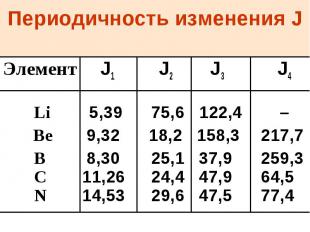
Периодичность изменения J Элемент J1 J2 J3 J4 Li 5,39 75,6 122,4 – Be 9,32 18,2 158,3 217,7 B 8,30 25,1 37,9 259,3 C 11,26 24,4 47,9 64,5 N 14,53 29,6 47,5 77,4
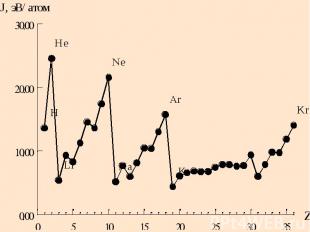

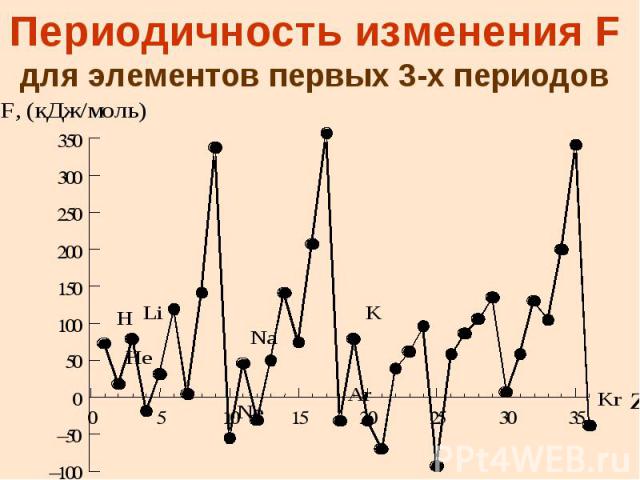
Сродство к электрону это энергия, выделяющаяся или поглощающаяся при захвате электрона атомом или энергия, необходимая для присоединения электрона к атому: Э + е = Э- , F [кДж/моль]
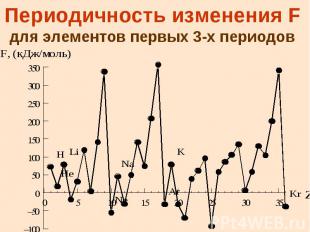
Периодичность изменения F для элементов первых 3-х периодов

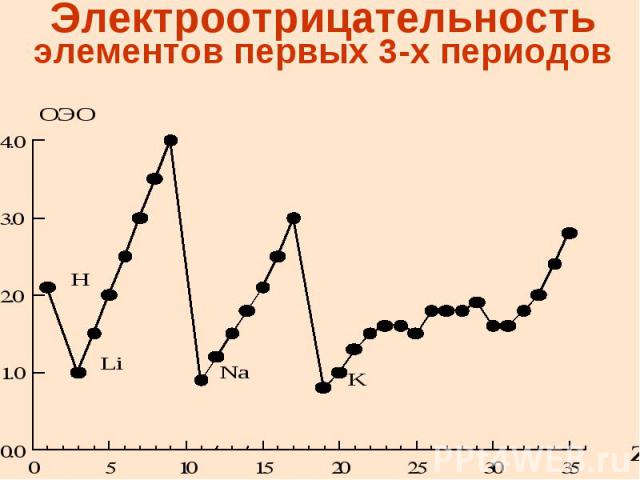
Электроотрицательность - свойство атома притягивать электроны от других атомов, с которыми он образует химическую связь в соединениях Электроотрицательность определяли Полинг, Малликен и др. ученые Электроотрицательность выражается в относительных условных единицах
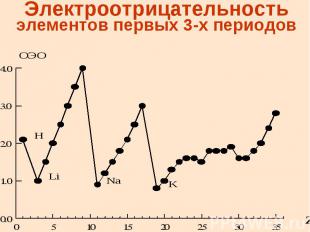
Электроотрицательность элементов первых 3-х периодов

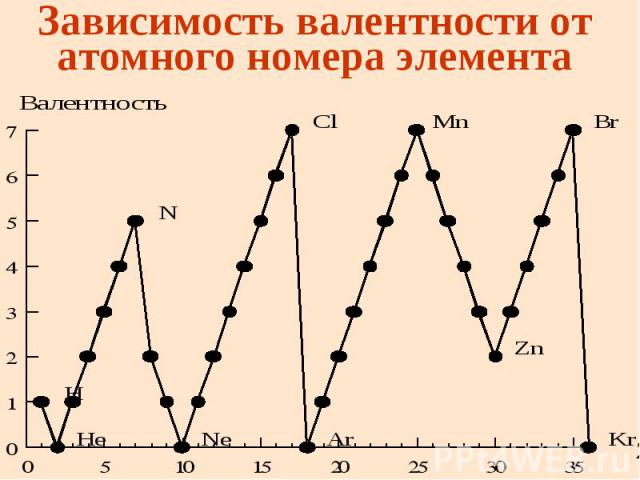
Валентность Валентность определяется электронами внешнего уровня, поэтому высшая валентность элементов главных подгрупп равна номеру группы
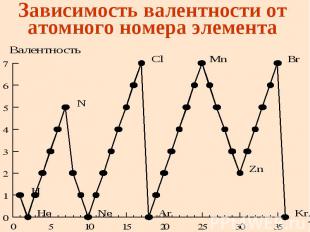
Зависимость валентности от атомного номера элемента

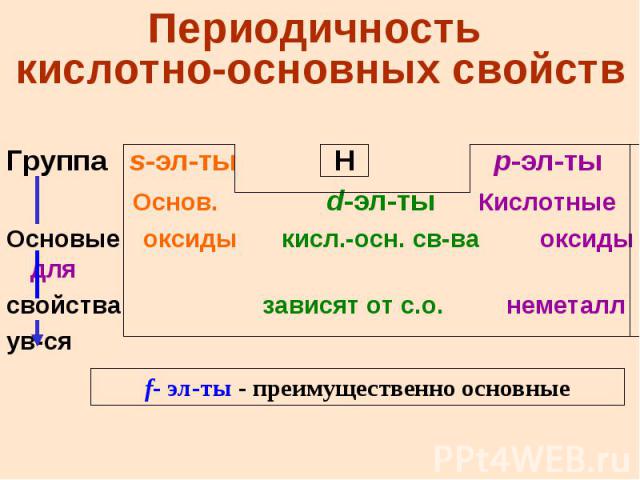
Периодические свойства соединений основно-кислотные свойства оксидов и гидроксидов: в периодах ум-ся основные свойства, но ув-ся кислотные свойства этих соединений в группах основные свойства ув-ся, а кислотные ум-ся
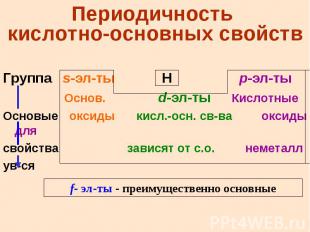
Периодичность кислотно-основных свойств Группа s-эл-ты H p-эл-ты Основ. d-эл-ты Кислотные Основые оксиды кисл.-осн. св-ва оксиды для свойства зависят от с.о. неметалл ув-ся

Кислотно-основные свойства с. о. кислотные свойства MnO Mn2O3 MnO2 MnO3 Mn2O7 осн. слабо осн. амфот. кисл. кисл.

По периоду: По периоду: (-) значения Gрo кислотные св-ва оксидов Na2O + Al2O3 = 2NaAlO2 Goр= -175 kJ Na2O + SiO2 = Na2SiO3 Goр= -197 kJ Na2O + 1/3P2O5 = 2/3Na3PO4 Goр= -371 kJ Na2O + SO3 = Na2SO4 Goр= -522 kJ Na2O + Cl2O7 = 2NaClO4 Goр= -587kJ

Окислительная способность простых веществ и однотипных соединений: Окислительная способность простых веществ и однотипных соединений: в периодах увеличивается в группах уменьшается

термическая устойчивость однотипных солей термическая устойчивость однотипных солей в периодах уменьшается и возрастает их склонность к гидролизу в группах увеличивается
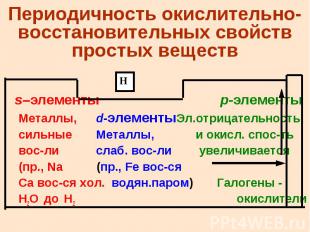
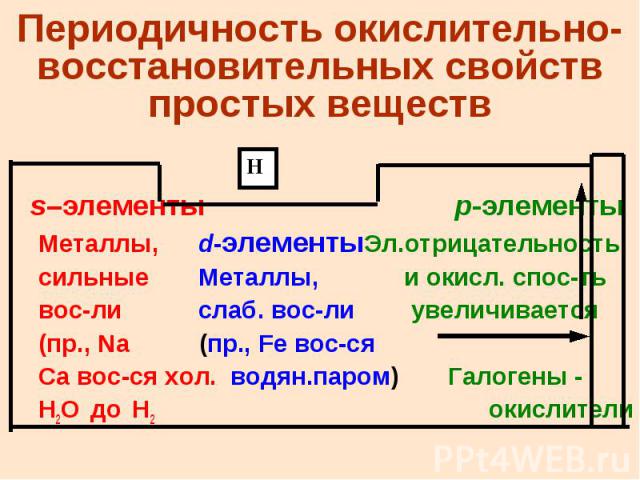
Периодичность окислительно-восстановительных свойств простых веществ s–элементы p-элементы Металлы, d-элементыЭл.отрицательность сильные Металлы, и окисл. спос-ть вос-ли слаб. вос-ли увеличивается (пр., Na (пр., Fe вос-ся Ca вос-ся хол. водян.паром) Галогены - H2O до H2 окислители

Периодическими являются многие другие свойства соединений: энергия хим. связи, энтальпия, энергия Гиббса образования и др. Периодическими являются многие другие свойства соединений: энергия хим. связи, энтальпия, энергия Гиббса образования и др. Место химического элемента в ПС определяет его свойства и свойства его многих соединений













































![Энергия и потенциал ионизации атомов Энергия ионизации – это энергия, необходимая для отрыва электрона от атома и превращение атома в положительно заряженный ион Э – е = Э+, Еион [кДж/моль] Ионизационный потенциал – это разность потенциалов, при кот… Энергия и потенциал ионизации атомов Энергия ионизации – это энергия, необходимая для отрыва электрона от атома и превращение атома в положительно заряженный ион Э – е = Э+, Еион [кДж/моль] Ионизационный потенциал – это разность потенциалов, при кот…](https://fs1.ppt4web.ru/images/95241/153167/640/img54.jpg)

![Сродство к электрону это энергия, выделяющаяся или поглощающаяся при захвате электрона атомом или энергия, необходимая для присоединения электрона к атому: Э + е = Э- , F [кДж/моль] Сродство к электрону это энергия, выделяющаяся или поглощающаяся при захвате электрона атомом или энергия, необходимая для присоединения электрона к атому: Э + е = Э- , F [кДж/моль]](https://fs1.ppt4web.ru/images/95241/153167/640/img58.jpg)