Презентация на тему: Основные сведения о строении атомов

Основные сведения о строении атомов


Понятие атом возникло ещё в античном мире для обозначения частиц вещества.

Ученые древности о строении вещества Древнегреческий ученый Демокрит 2500 лет назад считал, что любое вещество состоит из мельчайших частиц, которые впоследствии были названы «атомами», что в переводе на русский язык означает «неделимый»Долгое время считалось, что атом является неделимой частицей.

Ирландский физик СТОНИ на основании опытов пришёл к выводу, что электричество переносится мельчайшими частицами, существующими в атомах всех химических элементов В 1891 предложил название «электрон», что по-гречески означает «янтарь» для элементарного СТОНЕИ (Стони) Джордж Джонстон (Stoney George Johnstone) (15.II.1826 – 5.VII.1911) — ирландский физик и математик, член Ирландского королевского об-ва (1861), его секретарь на протяжении 20 лет.

История открытия строения атома. В 1879 году открыл катодные лучи.Уильям Крукс

Джозеф Томсон Жан ПерренДжозеф Томсон и Жан Перрен доказали, что электроны несут на себе отрицательный заряд
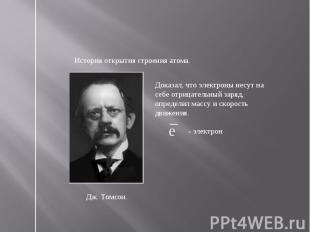
История открытия строения атома.Доказал, что электроны несут на себе отрицательный заряд, определил массу и скорость движения.Дж. Томсон.


Открытие радиоактивности Анри БеккерельРасщепление радиоактивного излучения

Эрнест Резерфорд В 1910 г. Эрнест Резерфорд со своими учениками и коллегами изучал рассеивание альфа-частиц, проходящих через тонкую золотую фольгу и попадавших на экран.

Э. РезерфордДоказал, что атом имеет плотное ядро. Предложил планетарную теорию строения атома.


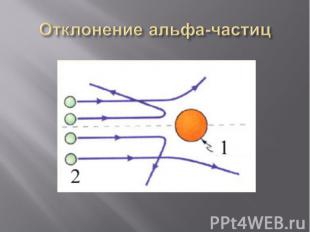
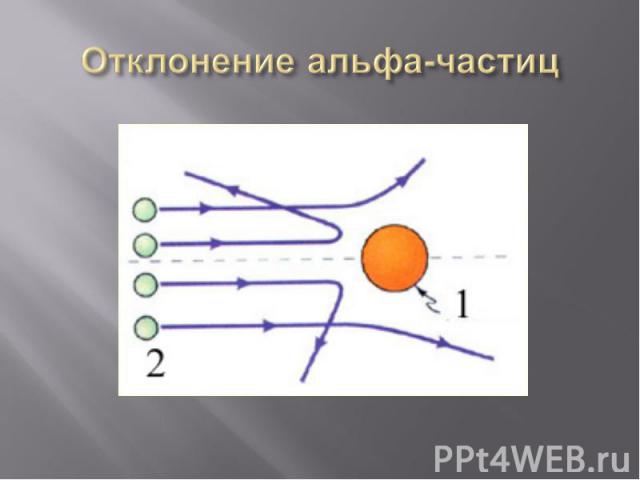
Отклонение альфа-частиц

Структура атома

В 1911 г. английский ученый Э. Резерфорд доказал ,что в центре атома имеется положительно заряженное ядро.

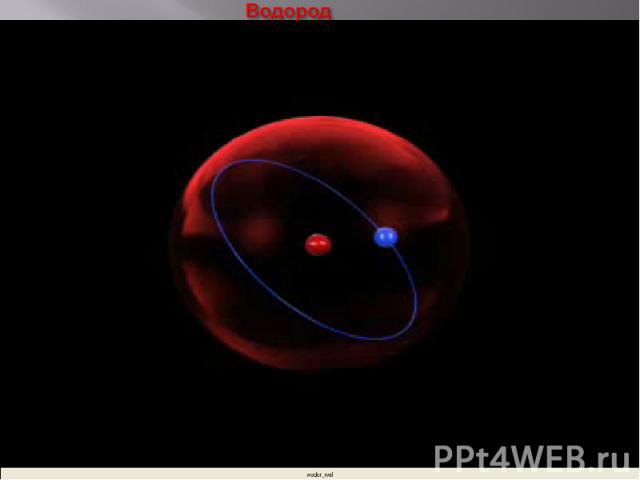
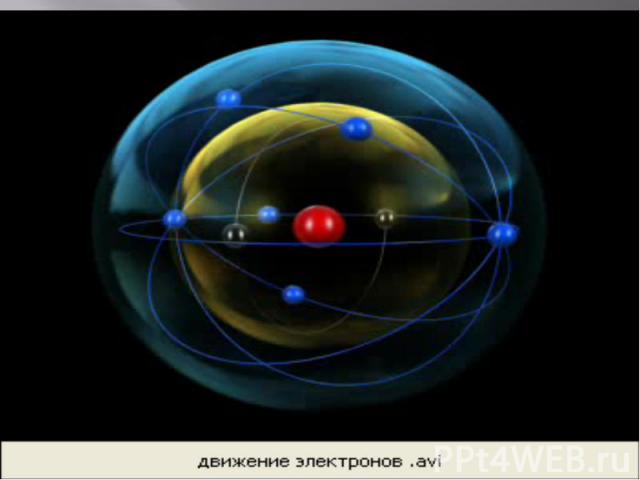
Планетарная модель строения атома Резерфорд предположил, что атом устроен подобно планетарной системе. Суть модели строения атома по Резерфорду заключается в следующем: в центре атома находится положительно заряженное ядро, в котором сосредоточена вся масса, вокруг ядра по круговым орбитам на больших расстояниях вращаются электроны (как планеты вокруг Солнца). Заряд ядра совпадает с номером химического элемента в таблице Менделеева.
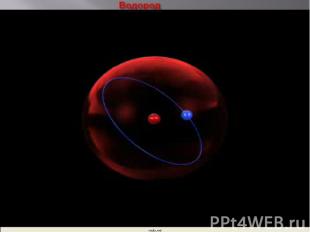
Водород
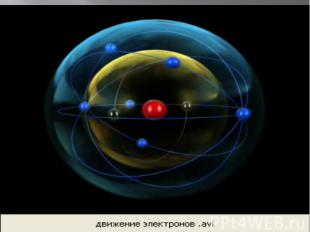

Характеристики элементарных частиц

СТРОЕНИЕ АТОМА

Число протонов в атоме равно порядковому номеру.Число электронов в атоме равно числу протонов.Число нейтронов рассчитывается по формуле: N = A – Z , где N – количество нейтроновA – массовое числоZ – заряд ядра

Изменение в составе ядер атомов химических элементов.Ядерные реакции. Изотопы

I. Ядерные реакции – это процессы приводящие к изменению структуры атома.


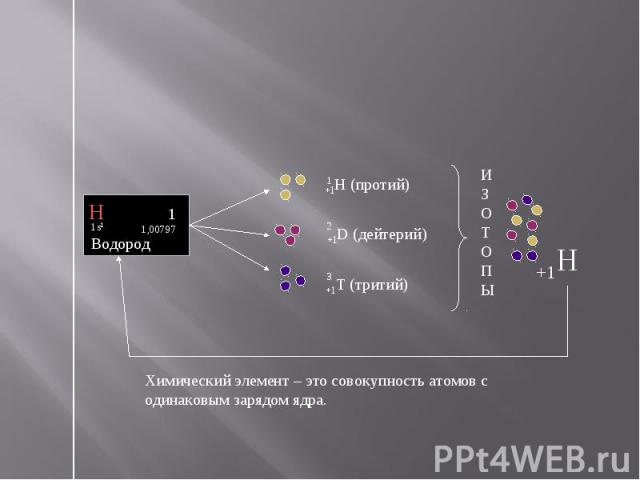
Химический элемент – это совокупность атомов с одинаковым зарядом ядра.
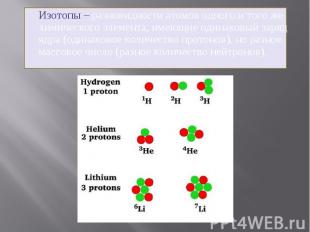
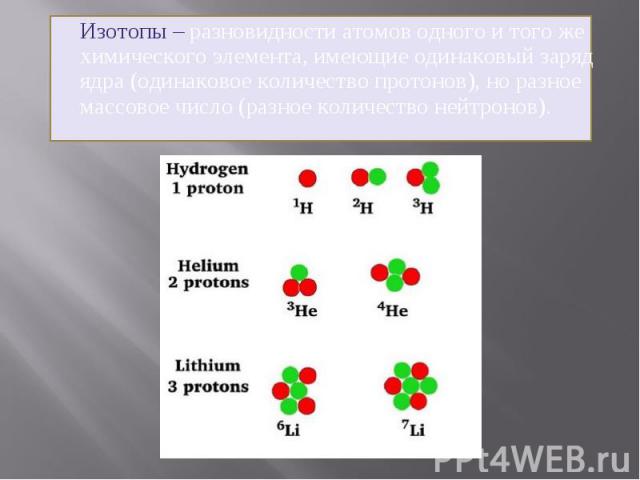
Изотопы – разновидности атомов одного и того же химического элемента, имеющие одинаковый заряд ядра (одинаковое количество протонов), но разное массовое число (разное количество нейтронов).