Презентация на тему: Гибридизация атомных орбиталей

Гибридизация атомных орбиталей

Лайнус Карл Полинг

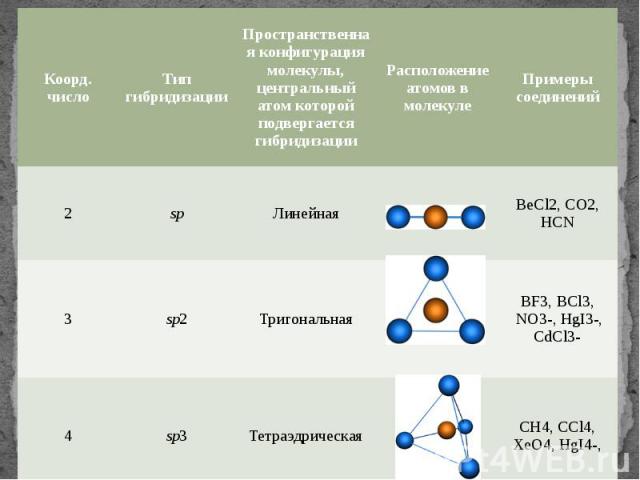
Гибридизация атомных орбиталей – изменение формы и энергии орбиталей атома при образовании ковалентной связи для достижения более эффективного перекрывания орбиталей.

Различные орбитали, несильно отличающиеся энергиями, образуют соответствующее число гибридных орбиталей. Число гибридных орбиталей равно числу атомных орбиталей, участвующих в гибридизации. Гибридные орбитали одинаковы по форме электронного облака и по энергии.

В гибридизации участвуют не только связывающие электроны, но и неподеленные электронные пары.

По сравнению с атомными орбиталями гибридные более вытянуты в направлении образования химических связей и поэтому обуславливают лучшее перекрывание электронных облаков.

Гибридная орбиталь больше вытянута по одну сторону ядра, чем по другую.
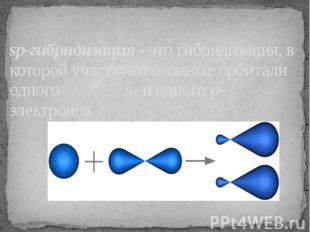
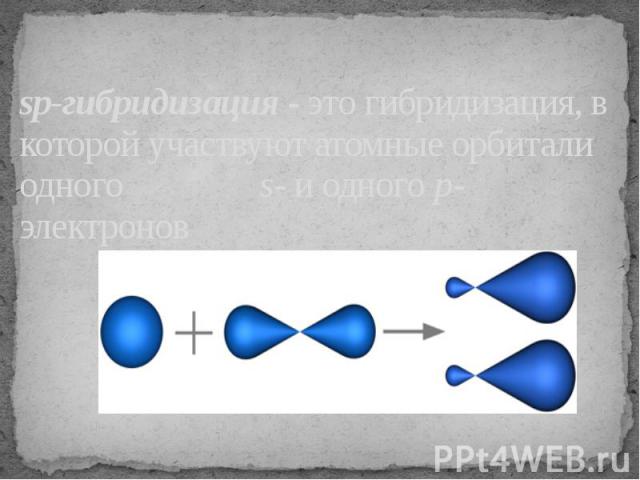
sp-гибридизация - это гибридизация, в которой участвуют атомные орбитали одного s- и одного p-электронов

В процессе гибридизации образуются 2 гибридные орбитали, которые ориентируются друг к другу под углом 180°

Представление о sp-гибридизации орбиталей можно применить для объяснения линейной формы молекулы BeH2, в которой атом бериллия образован гибридными sp-орбиталями.

Образование молекулы фторида бериллия . Каждый атом фтора, входящий в состав этой молекулы, обладает одним неспаренным электроном,который и участвует в образовании ковалентной связи.
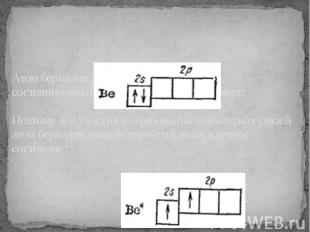
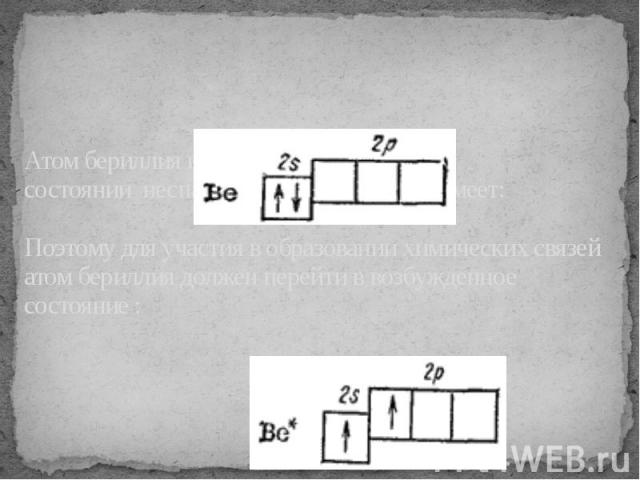
Атом бериллия в невозбужденном состоянии неспаренных электронов не имеет:Поэтому для участия в образовании химических связей атом бериллия должен перейти в возбужденное состояние :

при затрате некоторой энергии вместо исходных s- и р-орбиталей атома бериллия могут образоваться две равноценные гибридные орбитали (sp-орбитали).

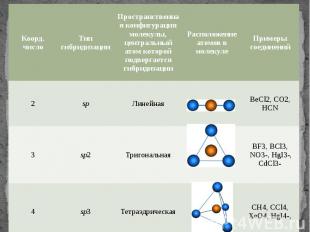
Примеры химических соединений, для которых характерна sp-гибридизация: BeCl2, BeH2,CO, CO2, HCN, карбин, ацетиленовые углеводороды (алкины).
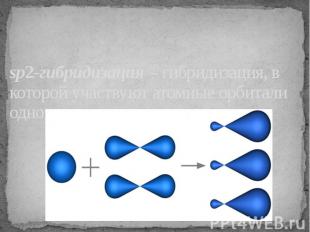
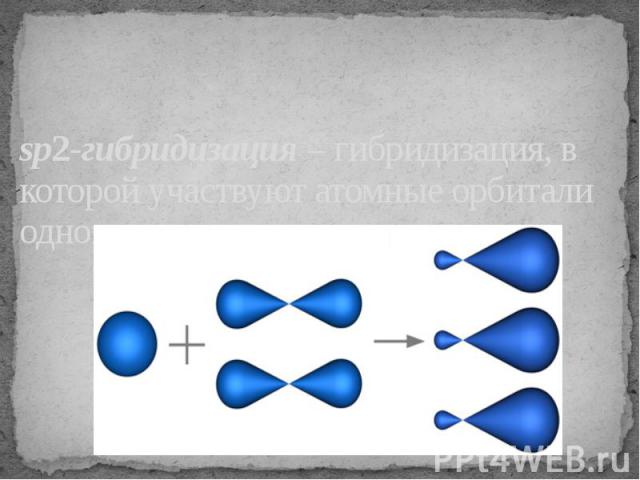
sp2-гибридизация – гибридизация, в которой участвуют атомные орбитали одного s- и двух p-электронов

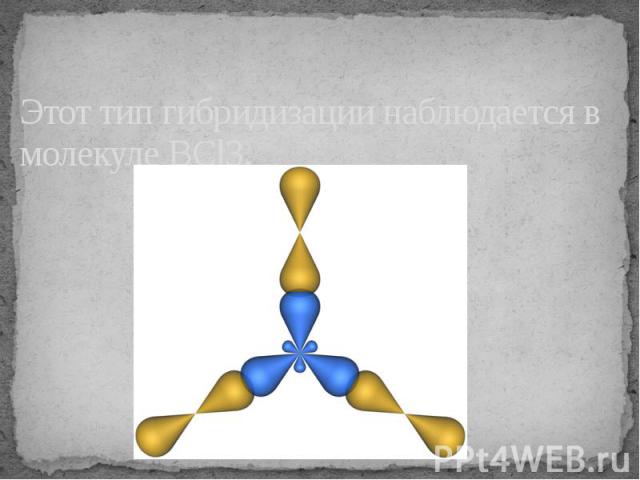
В результате гибридизации образуются три гибридные sp2 орбитали, расположенные в одной плоскости под углом 120° друг к другу
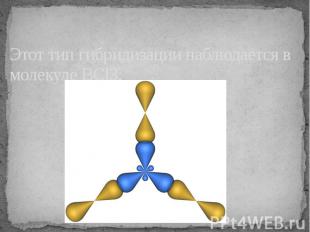
Этот тип гибридизации наблюдается в молекуле BCl3.
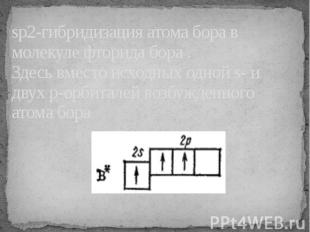
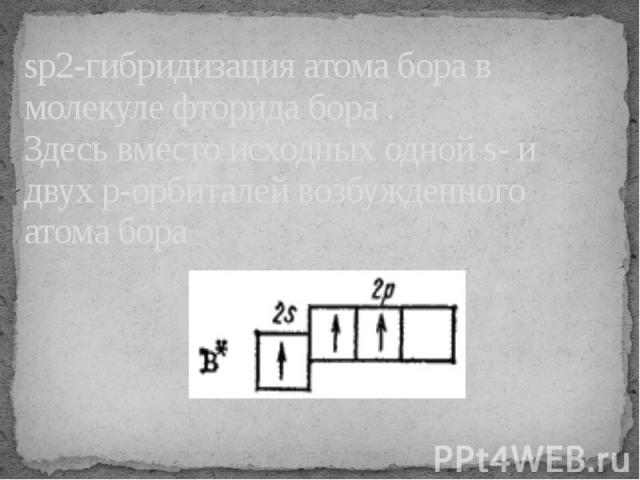
sp2-гибридизация атома бора в молекуле фторида бора . Здесь вместо исходных одной s- и двух р-орбиталей возбужденного атома бора

образуются три равноценные sp2-орбитали. Поэтому молекула построена в форме правильного треугольника, в центре которого расположен атом бора, а в вершинах—атомы фтора.

Примеры соединений, в которых наблюдается sp2-гибридизация: SO3, BCl3, BF3, AlCl3, CO32-, NO3-, графит, этиленовые углеводороды (алкены), карбоновые кислоты и ароматические углеводороды (арены).

sp3-гибридизация – гибридизация, в которой участвуют атомные орбитали одного s- и трех p-электронов

Четыре sp3-гибридные орбитали симметрично ориентированны в пространстве под углом 109°28'

не всегда пространственная конфигурация молекулы соответствует тетраэдру, это зависит от числа атомов в молекуле.Примером тому служат молекул воды и аммиакаNH3.

Валентность атома азота – III, его пять электронов внешнего уровня занимают четыре орбитали, значит, тип гибридизации – sp3, но только три орбитали принимают участие в образовании химической связи. Тетраэдр без одной вершины превращается в пирамиду. Поэтому у молекулы аммиака форма молекулы пирамидальная, угол связи искажается до 107°30′.

кислород в молекуле воды находится в sp3 гибридном состоянии, а форма молекулы - угловая, угол связи составляет 104°27′.

Примеры соединений, для которых характерна sp3-гибридизация: H2O, NH3, POCl3, SO2F2, SOBr2, NH4+, H3O+, алмаз, предельные углеводороды (алканы, циклоалканы).