Презентация на тему: Гибридизация Атома Углерода

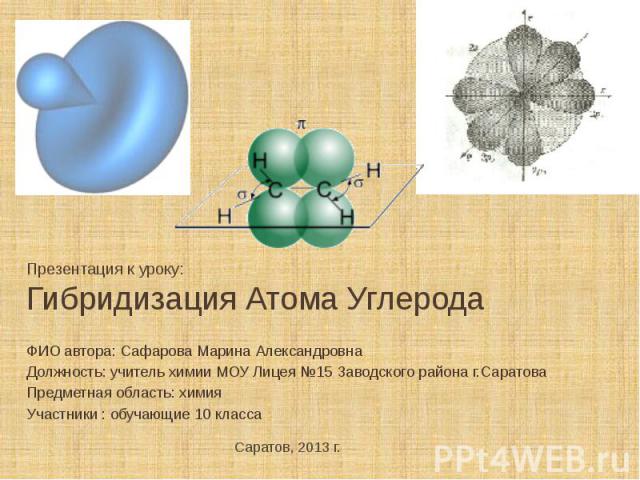
Презентация к уроку: Гибридизация Атома Углерода ФИО автора: Сафарова Марина АлександровнаДолжность: учитель химии МОУ Лицея №15 Заводского района г.СаратоваПредметная область: химияУчастники : обучающие 10 класса
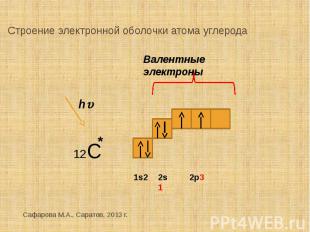
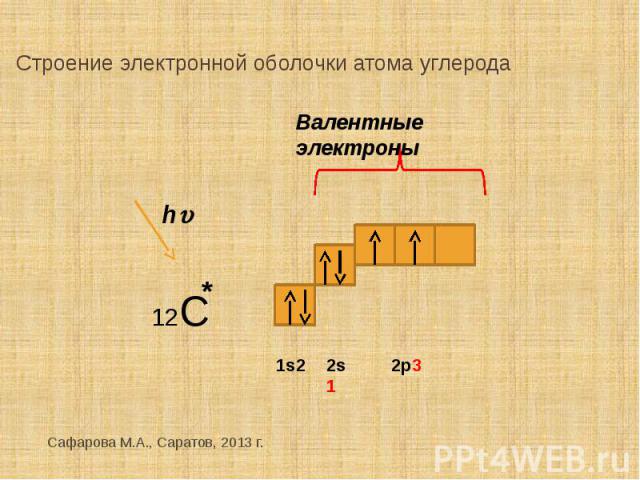
Строение электронной оболочки атома углерода Валентные электроны

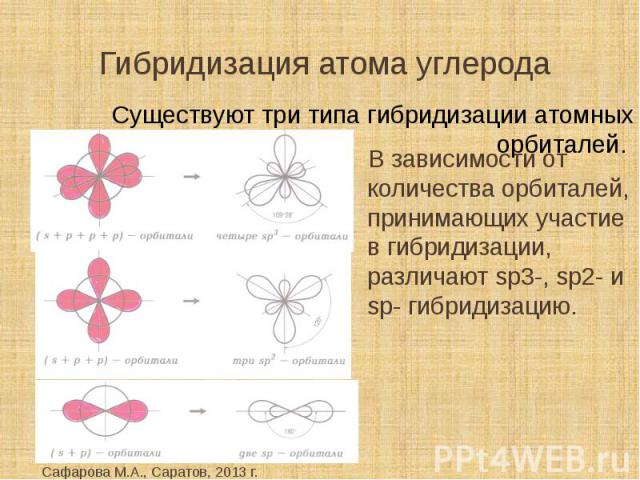
Гибридизация атома углерода Существуют три типа гибридизации атомных орбиталей. В зависимости от количества орбиталей, принимающих участие в гибридизации, различают sp3-, sp2- и sp- гибридизацию.
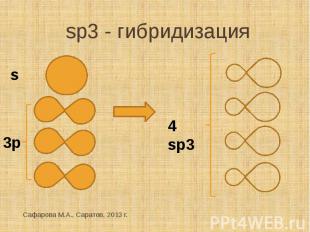
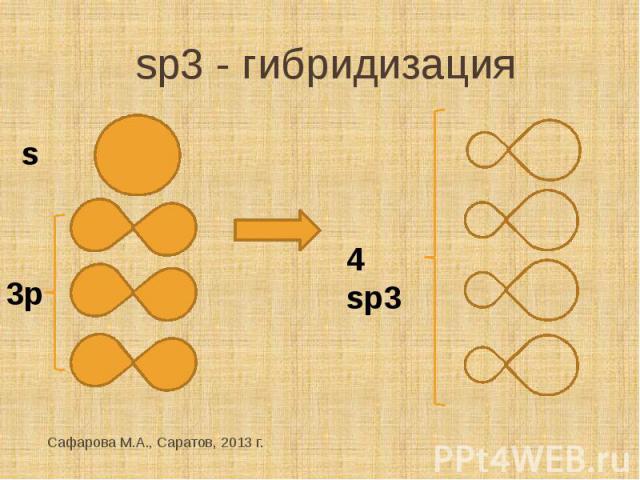
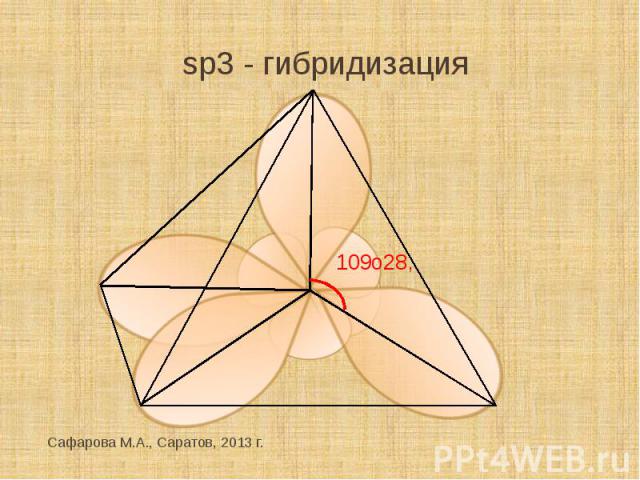
sp3 - гибридизация
sp3 - гибридизация
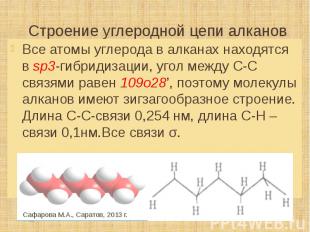
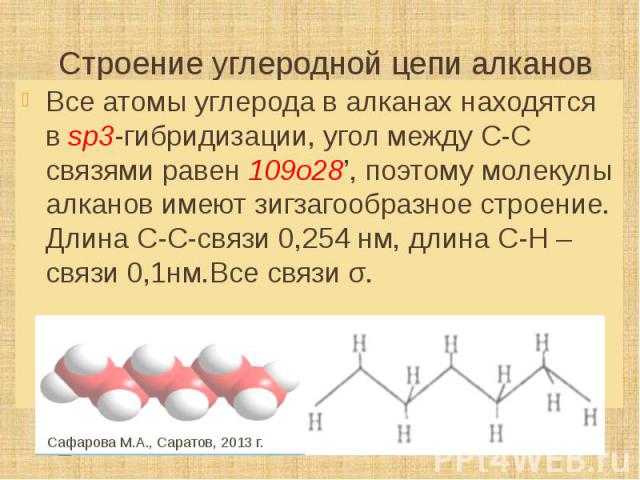
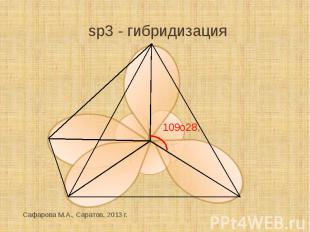
Строение углеродной цепи алканов Все атомы углерода в алканах находятся в sp3-гибридизации, угол между С-С связями равен 109о28’, поэтому молекулы алканов имеют зигзагообразное строение. Длина С-С-связи 0,254 нм, длина С-Н – связи 0,1нм.Все связи σ.

В алмазе атомы углерода находятся в sp3 – гибридизации.
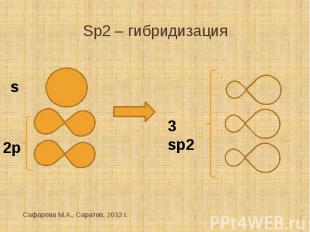
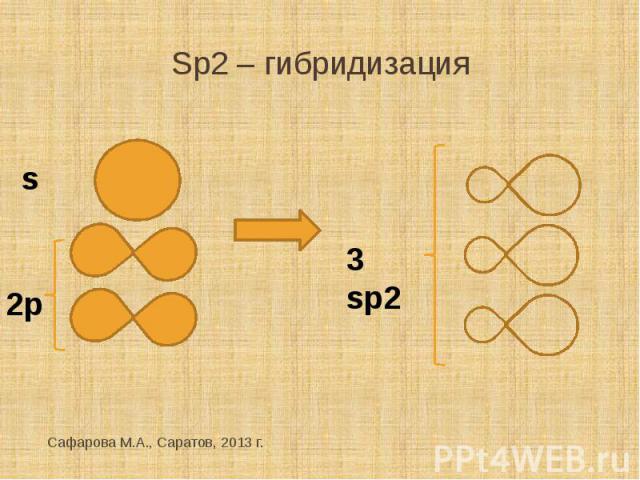
Sp2 – гибридизация
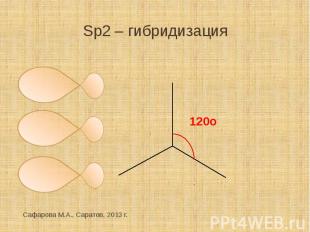
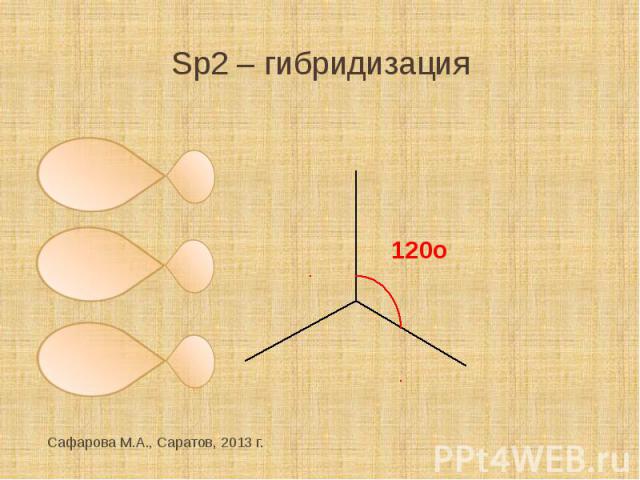
Sp2 – гибридизация
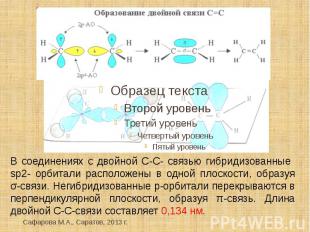
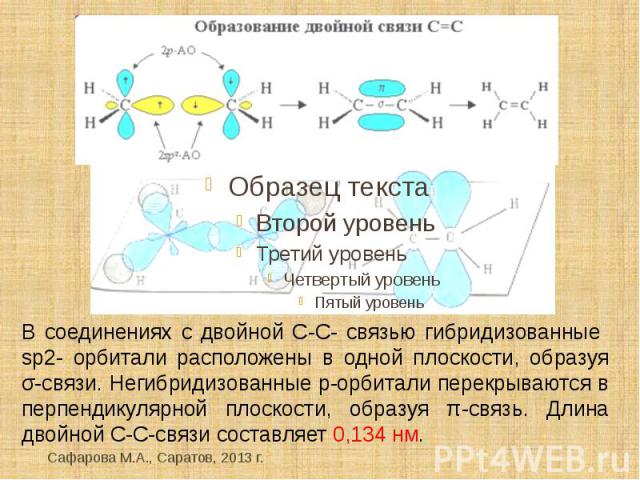
В соединениях с двойной C-C- связью гибридизованные sp2- орбитали расположены в одной плоскости, образуя σ-связи. Негибридизованные р-орбитали перекрываются в перпендикулярной плоскости, образуя π-связь. Длина двойной С-С-связи составляет 0,134 нм.
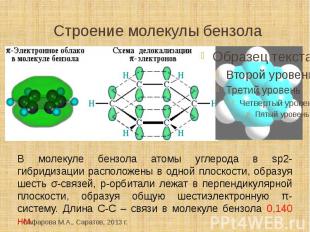
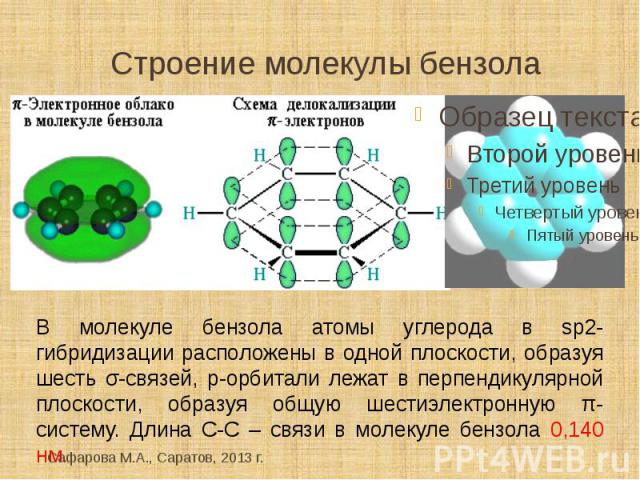
Строение молекулы бензола В молекуле бензола атомы углерода в sp2- гибридизации расположены в одной плоскости, образуя шесть σ-связей, р-орбитали лежат в перпендикулярной плоскости, образуя общую шестиэлектронную π-систему. Длина С-С – связи в молекуле бензола 0,140 нм.
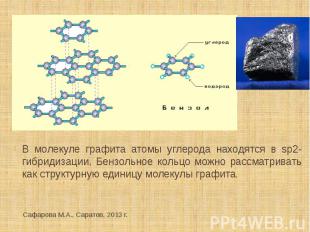
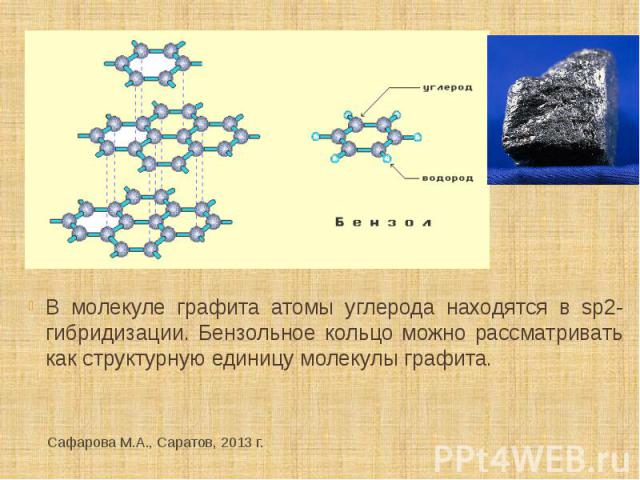
В молекуле графита атомы углерода находятся в sp2- гибридизации. Бензольное кольцо можно рассматривать как структурную единицу молекулы графита.
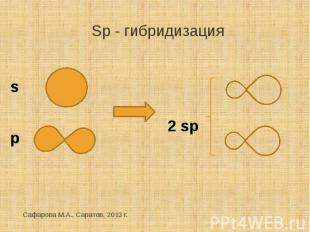
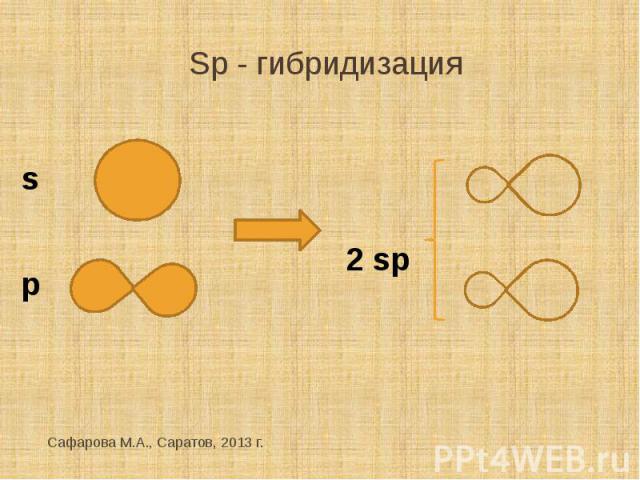
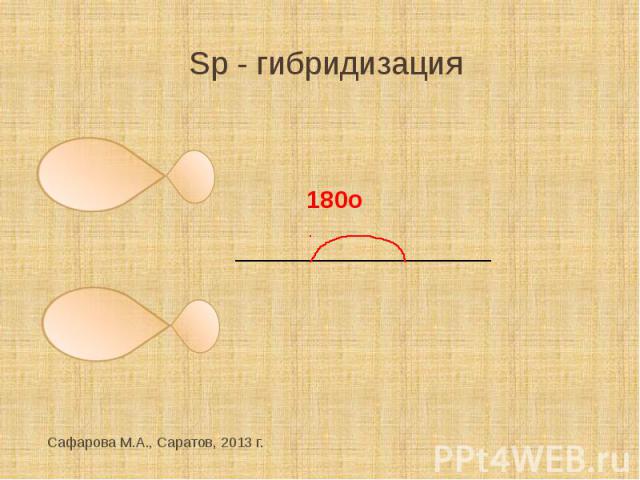
Sp - гибридизация
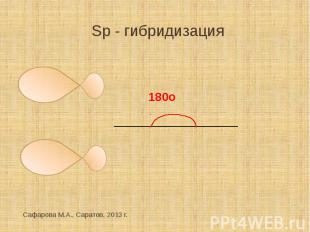
Sp - гибридизация
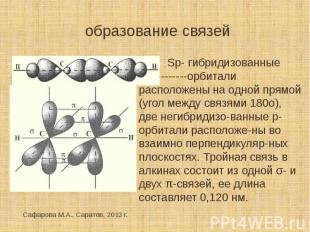
образование связей Sp- гибридизованные --------орбитали расположены на одной прямой (угол между связями 180о), две негибридизо-ванные р- орбитали расположе-ны во взаимно перпендикуляр-ных плоскостях. Тройная связь в алкинах состоит из одной σ- и двух π-связей, ее длина составляет 0,120 нм.
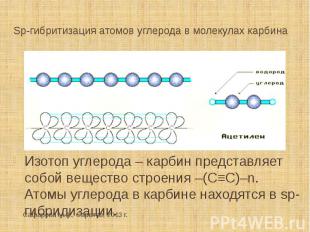
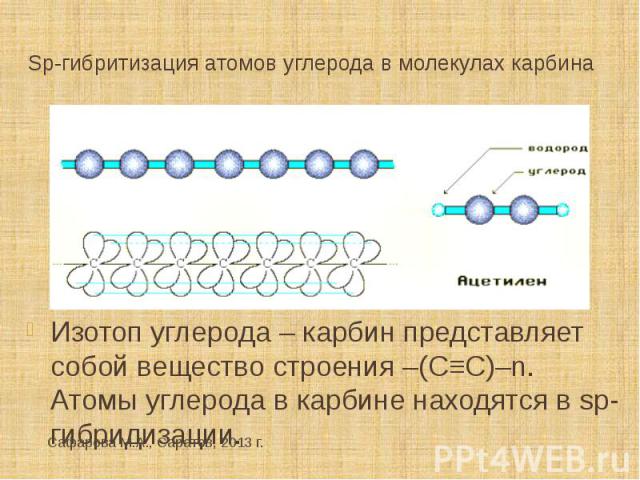
Sp-гибритизация атомов углерода в молекулах карбина Изотоп углерода – карбин представляет собой вещество строения –(С≡С)–n. Атомы углерода в карбине находятся в sp-гибридизации.

Геометрические конфигурации молекул