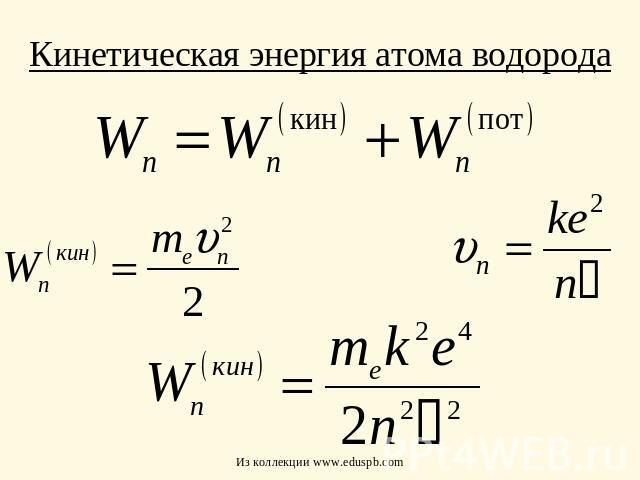Презентация на тему: Атом водорода по Бору. Квантовые постулаты

Атом водорода по Бору. Квантовые постулаты © В.Е. Фрадкин, А.М.Иконников, 2004

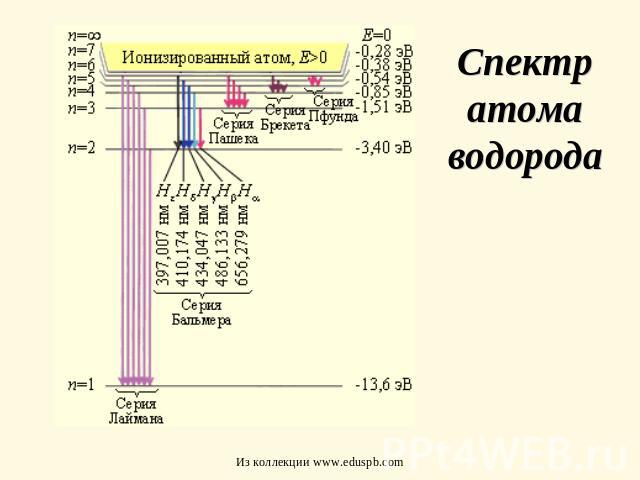
Спектр водорода

И. Бальмер (1885г.) Экспериментальные данные п=3, 4, 5 и т.д., R= 3,21015 Гц R - "постоянная Ридберга"

Ф. Пашен Экспериментальные данные п= 4, 5 и т.д.

Т. Лайман Экспериментальные данные п= 2, 3, 4, 5 и т.д.

Первый постулат Бора (постулат стационарных состояний) Атомная система может находится только в особых стационарных или квантовых состояниях, каждому из которых соответствует определенная энергия Wn. В стационарных состояниях атом не излучает.
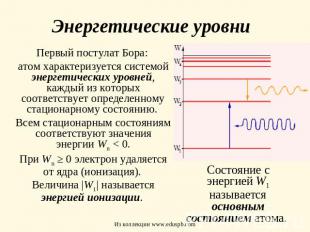
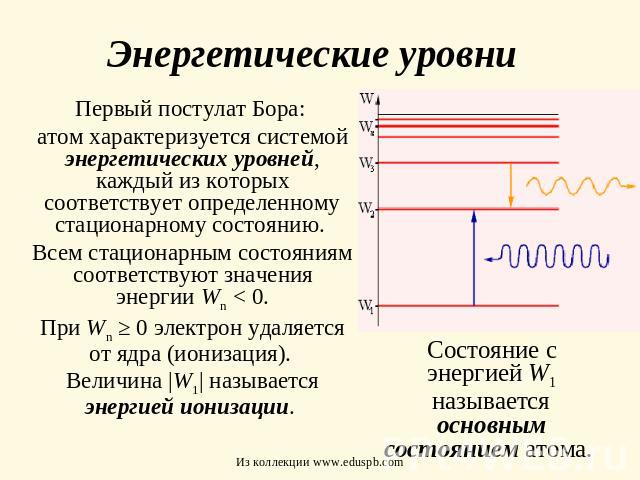
Энергетические уровни Первый постулат Бора: атом характеризуется системой энергетических уровней, каждый из которых соответствует определенному стационарному состоянию. Всем стационарным состояниям соответствуют значения энергии Wn < 0.При Wn ≥ 0 электрон удаляется от ядра (ионизация). Величина |W1| называется энергией ионизации. Состояние с энергией W1 называется основным состоянием атома.

Второй постулат Бора (правило частот): при переходе атома из одного стационарного состояния с энергией Wn в другое стационарное состояние с энергией Wk излучается или поглощается квант, энергия которого равна разности энергий стационарных состояний:

Правило квантования (отбора орбит) Момент импульса Постоянная Планка Момент импульса электрона, вращающегося вокруг ядра, может принимать только дискретные значения, кратные постоянной Планка. Для круговых орбит:

Атом водорода по Н.Бору По правилу квантования:

Расчет спектра атома водорода
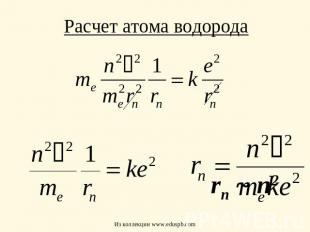
Расчет атома водорода
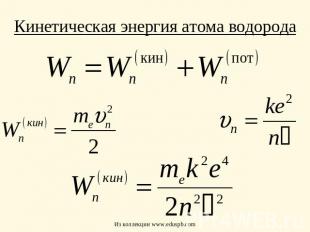
Кинетическая энергия атома водорода

Потенциальная энергия атома водорода

Энергия атома водорода

Формула И.Ридберга (1890) Для серии Бальмера m = 2, n = 3, 4, 5, ... . Для ультрафиолетовой серии Лаймана m = 1, n = 2, 3, 4, ... .

Постоянная Ридберга
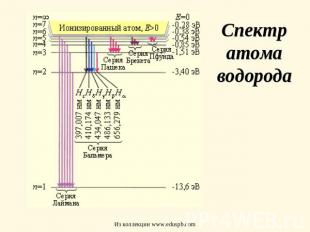
Спектр атома водорода