Презентация на тему: Строение атома. Урок в 8 классе


Маленькая точка, сделанная карандашом, состоит из огромного количества атомов, большего, чем количество жителей на Земле !

Демокрит В основе философии Демокрита лежит учение об атомах и пустоте как двух принципах, порождающих многообразие космоса. Атом есть мельчайшее «неделимое» тело, не подверженное никаким изменениям. Неделимость атома аналогична неделимости «бытия».

М.В. Ломоносов (1711-1765 гг.) Материя состоит из мельчайших первичных частиц, или атомов. Атомы неделимы и не могут создаваться и разрушаться. Атомы характеризуются определенным размером и массой. Молекулы состоят из атомов, как из одинаковых, так и различных. При физических явлениях молекулы сохраняются, при химических – разрушаются. Химические реакции заключаются в образовании новых молекул из тех же самых атомов, из которых состояли исходные вещества. атомно- молекулярная теория Джон Дальтон (1766-1844 гг.)
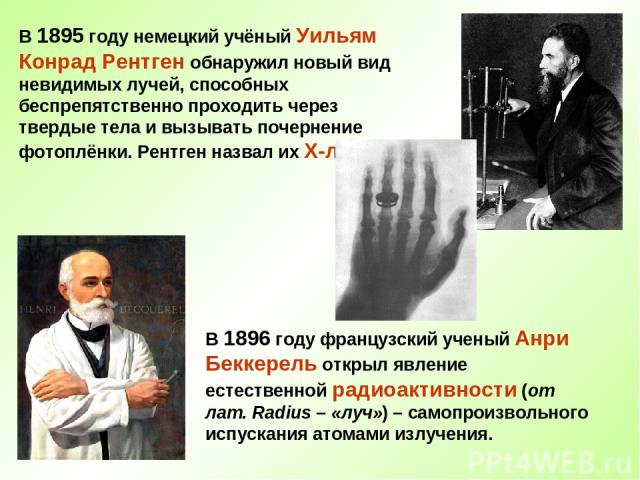
В 1895 году немецкий учёный Уильям Конрад Рентген обнаружил новый вид невидимых лучей, способных беспрепятственно проходить через твердые тела и вызывать почернение фотоплёнки. Рентген назвал их Х-лучами. В 1896 году французский ученый Анри Беккерель открыл явление естественной радиоактивности (от лат. Radius – «луч») – самопроизвольного испускания атомами излучения.

В 1898 году Пьер Кюри и Мария Склодовская – Кюри, изучавшие явление радиоактивности, открыли новые элементы – полоний и радий.

Английский физик Эрнест Резерфорд в 1909 г. открыл ядро атома Опыт Резерфорда: поток ά-частиц, излучаемый радиоактивным источником, через узкую щель направлялся на тонкую золотую фольгу; при помощи флюоресцирующего экрана проводилась регистрация ά-частиц, которые в отсутствии фольги двигались узким пучком, вызывая на экране яркую вспышку
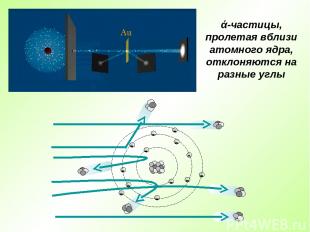
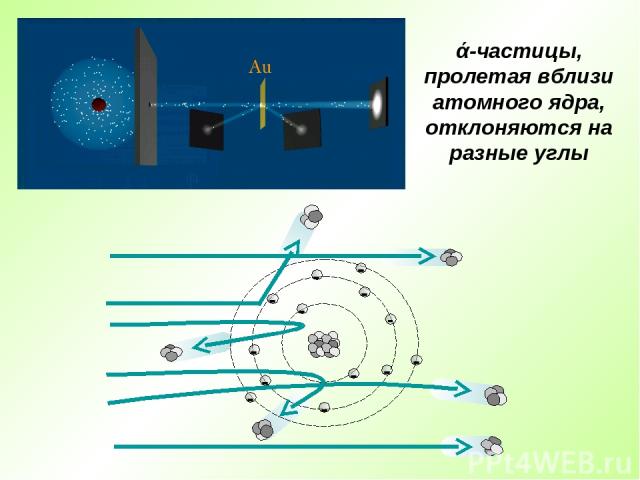
ά-частицы, пролетая вблизи атомного ядра, отклоняются на разные углы
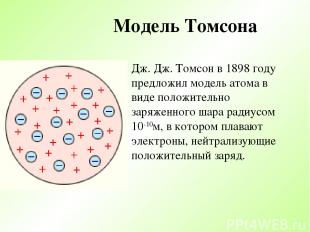
Модель Томсона Дж. Дж. Томсон в 1898 году предложил модель атома в виде положительно заряженного шара радиусом 10-10м, в котором плавают электроны, нейтрализующие положительный заряд.

Э. Резерфорд предложил планетарную модель атома: в центре находится положительно заряженное ядро, которое имеет достаточно малые размеры, но в нём заключена почти вся масса атома; вокруг ядра по круговым орбитам движутся отрицательно заряженные электроны, подобно движению планет вокруг солнца.
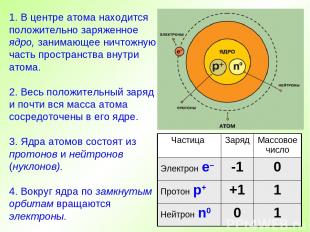
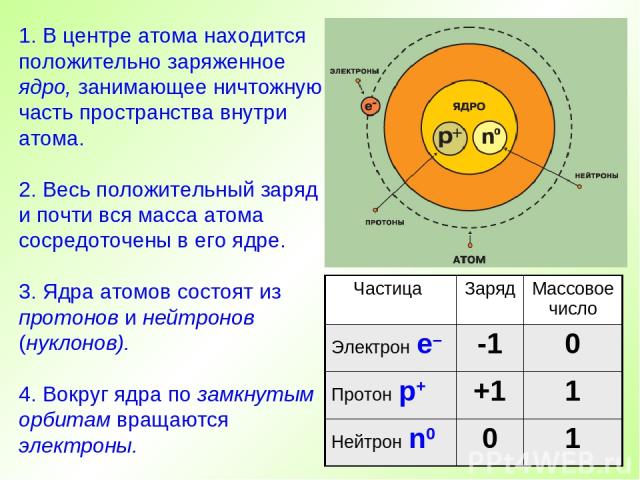
1. В центре атома находится положительно заряженное ядро, занимающее ничтожную часть пространства внутри атома. 2. Весь положительный заряд и почти вся масса атома сосредоточены в его ядре. 3. Ядра атомов состоят из протонов и нейтронов (нуклонов). 4. Вокруг ядра по замкнутым орбитам вращаются электроны. Частица Заряд Массовое число Электрон е– -1 0 Протон р+ +1 1 Нейтрон n0 0 1
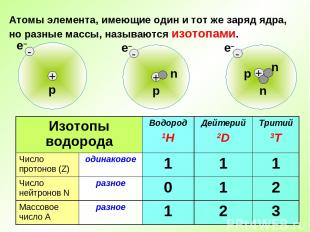
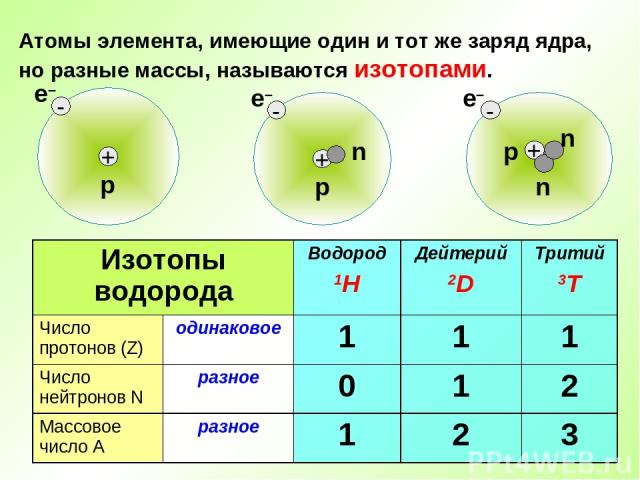
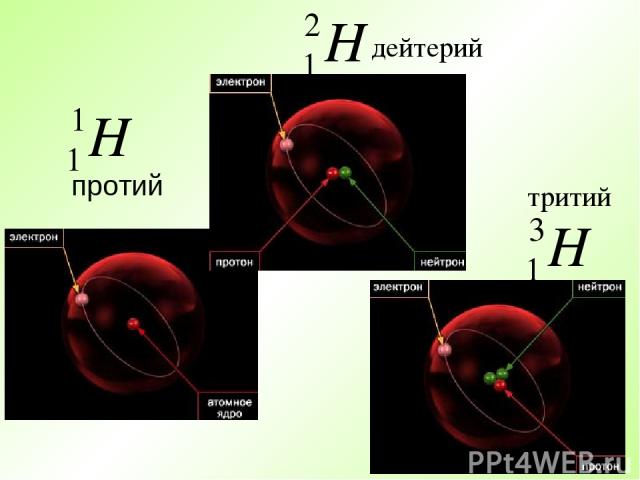
Атомы элемента, имеющие один и тот же заряд ядра, но разные массы, называются изотопами. Изотопы водорода Водород 1H Дейтерий 2D Тритий 3T Число протонов (Z) одинаковое 1 1 1 Число нейтронов N разное 0 1 2 Массовое число А разное 1 2 3
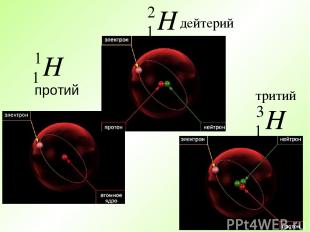
протий дейтерий тритий
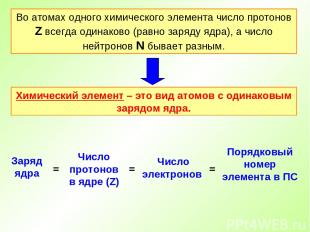
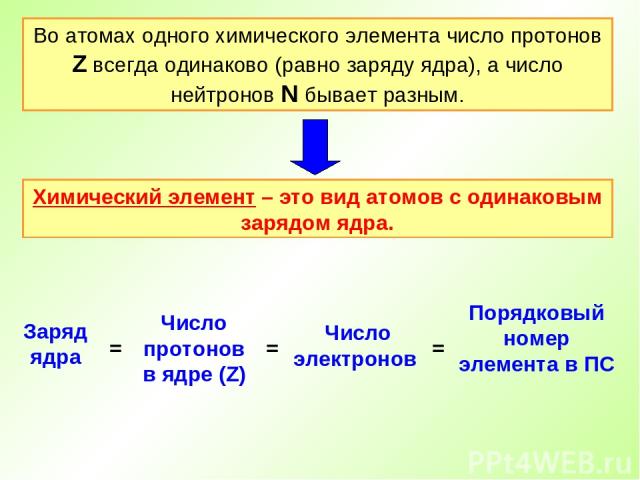
Во атомах одного химического элемента число протонов Z всегда одинаково (равно заряду ядра), а число нейтронов N бывает разным. Химический элемент – это вид атомов с одинаковым зарядом ядра.
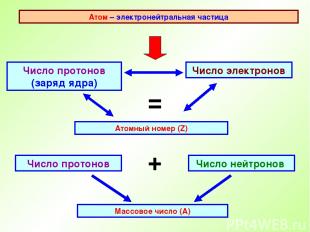
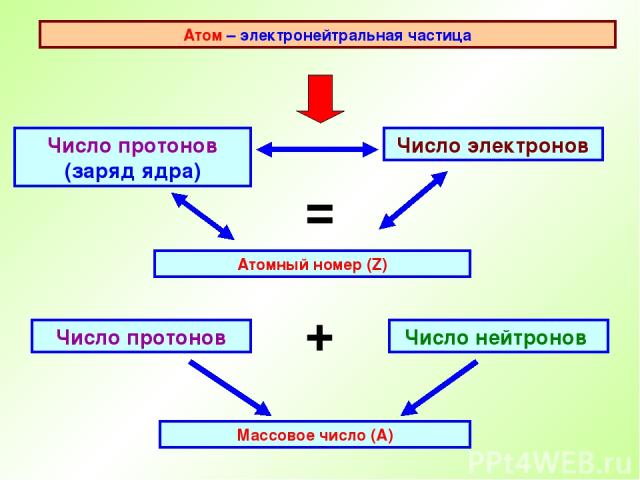
Атом – электронейтральная частица Число протонов (заряд ядра) Атомный номер (Z) Число электронов = Число нейтронов Число протонов + Массовое число (А)
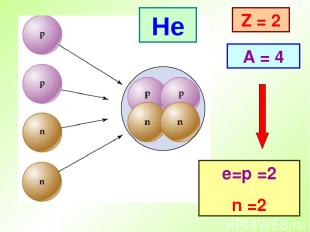
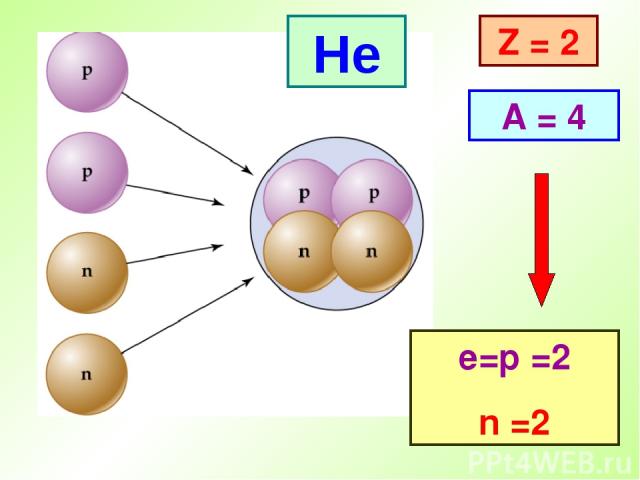
He Z = 2 A = 4 е=p =2 n =2
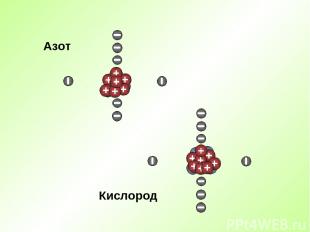
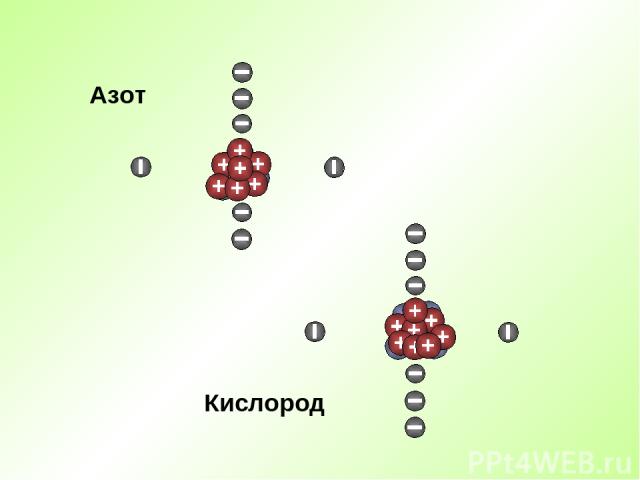
Кислород Азот
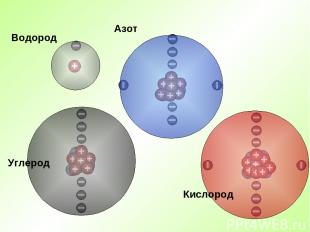
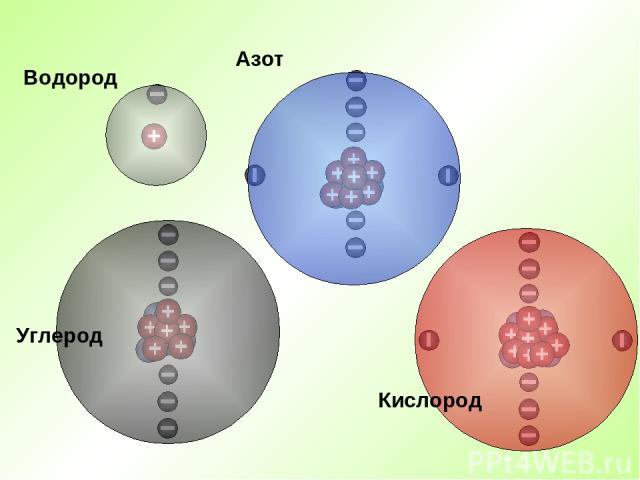
Водород Азот Кислород Углерод
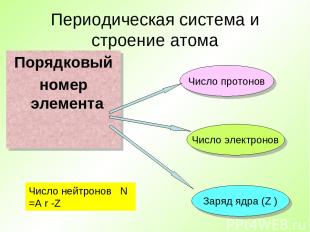
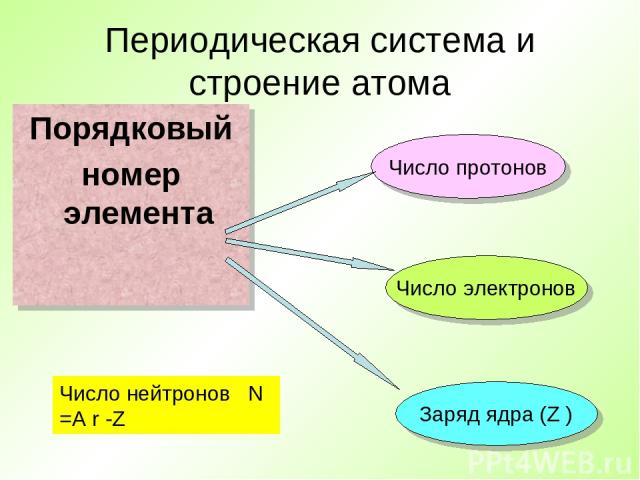
Периодическая система и строение атома Порядковый номер элемента Число протонов Число электронов Заряд ядра (Z ) Число нейтронов N =A r -Z
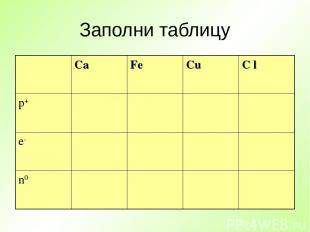
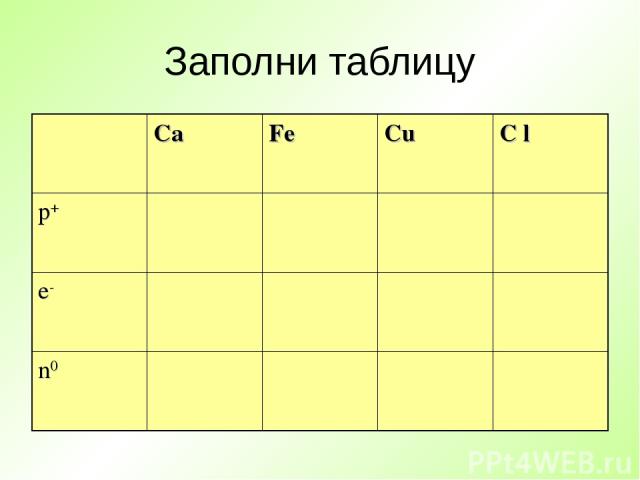
Заполни таблицу Ca Fe Cu C l p+ e- n0
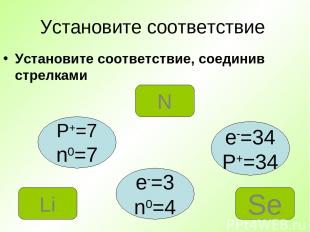
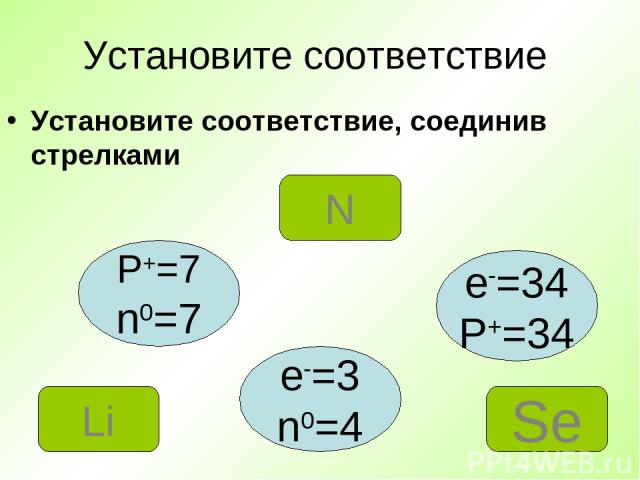
Установите соответствие Установите соответствие, соединив стрелками P+=7 n0=7 e-=34 P+=34 e-=3 n0=4 N Se Li

Свойства химических элементов, а также образованных ими веществ находятся в периодической зависимости от зарядов атомных ядер Современная формулировка Периодического закона

Тестовые задания Заряд ядра атома азота равен : а) 7 б) 13 в) 4 г) 29 д) 11 Число протонов в ядре атома криптона : а ) 36 б) 17 в) 4 г) 31 д) 6 Число нейтронов в ядре атома цинка : а) 8 б) 35 в)11 г)30 д)4 Число электронов в атоме железа : а) 11 б)8 в)56 г)26 д)30 Изотопы водорода отличаются друг от друга : а)числом e- б)числом n в) химическим знаком г) числом p д)массовым числом

Тестовые задания Заряд ядра атома азота равен : а) 7 б) 13 в) 4 г) 29 д) 11 Число протонов в ядре атома криптона : а ) 36 б) 17 в) 4 г) 31 д) 6 Число нейтронов в ядре атома цинка : а) 8 б) 35 в)11 г)30 д)4 Число электронов в атоме железа : а) 11 б)8 в)56 г)26 д)30 Изотопы водорода отличаются друг от друга : а)числом электронов б)числом нейтронов в) химическим знаком г) числом p д)массовым числом МОЛОДЦЫ ! ЭТО ВАМ УДАЛОСЬ !!!

МОЛОДЦЫ !!! Вы справились. Желаю дальнейших успехов в изучении химии!