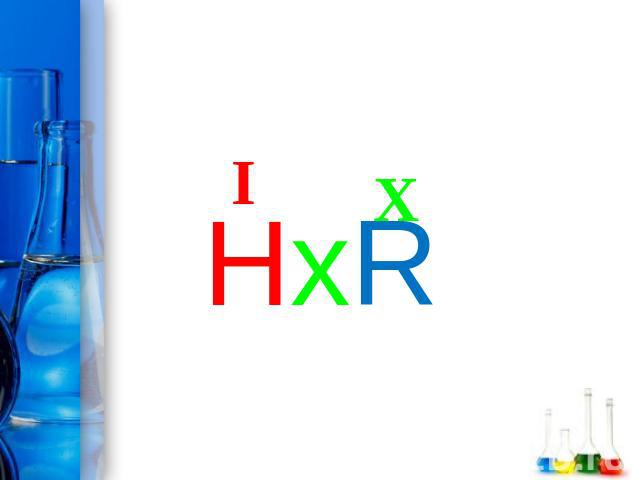Презентация на тему: Классификация неорганических веществ
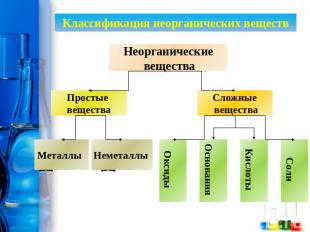
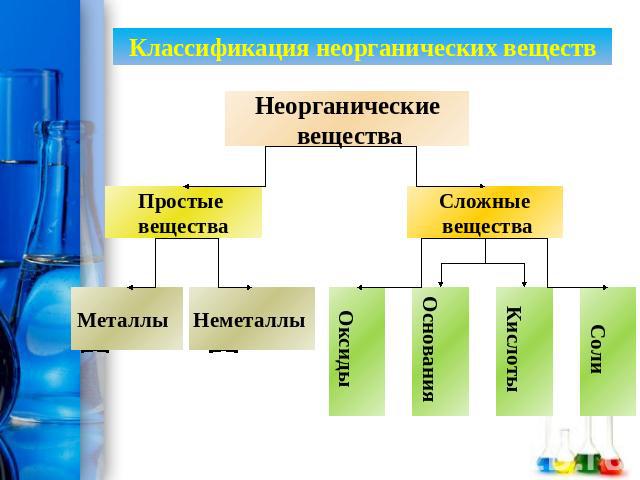
Классификация неорганических веществНеорганические вещества

Задание: Определите тип каждой из реакций, уравнения которых записаны в таблице

Задание: Из букв правильных ответов определите название класса веществ

КИСЛОТЫОрлова В.Н.Учитель химии и биологии МАОУ «Гимназия Тарасовка»

Цели урокаСформировать понятие о кислотах.Рассмотреть состав, название, классификацию кислот.Познакомиться с представителями неорганических кислот.Изучить химические свойства кислот

Кислоты вокруг нас

Кислоты вокруг нас

Кислоты вокруг нас

Кислоты вокруг нас

Кислоты в организме человека
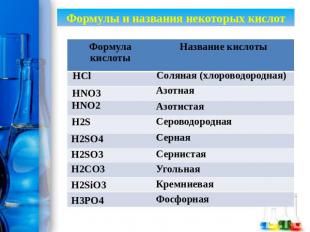
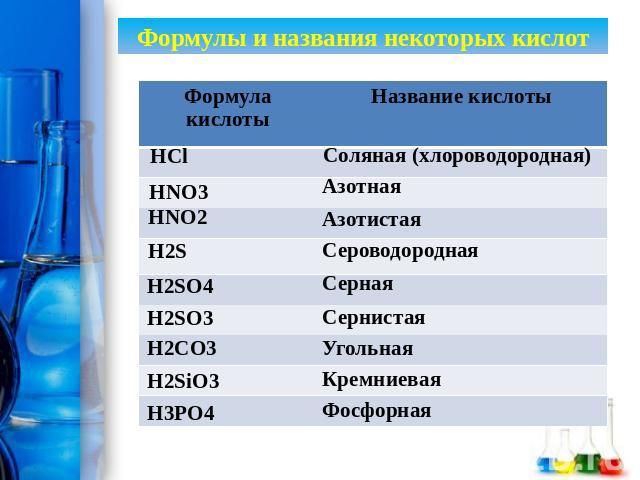
Формулы и названия некоторых кислот

Кислоты - это сложные вещества, состоящие из одного или нескольких атомов водорода и кислотного остатка
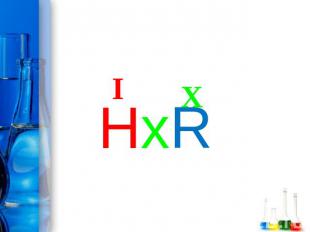
XI

Подчеркните кислотный остаток в молекулах кислотH2SO4; H2CO3; HNO3; H2SiO3; H3PO4

Определите валентность кислотных остатковH2SO4; H2CO3; HNO3; H2SiO3; H3PO4

Составьте формулы кислот по известным кислотным остаткамCl(I) → S(II)→ PO4(III)→SiO3(II)→ ClO4(I) →MnO4(II) → NO2(I)→

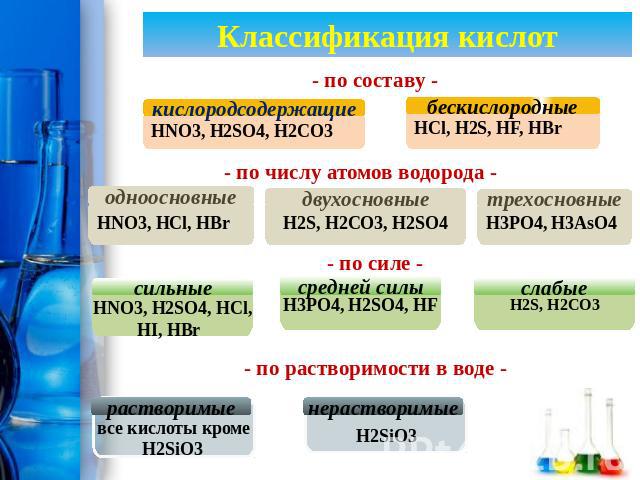
Классификация кислотПо какому признаку кислоты разделены на группы

Классификация кислот

Классификация кислотПо какому признаку кислоты разделены на группы?фтороводороднаяHCl - хлороводородная HBr - бромоводороднаяHI - йодоводороднаяHNO3 - азотнаяHNO2 - азотистаяHClO4 - хлорная

Классификация кислот
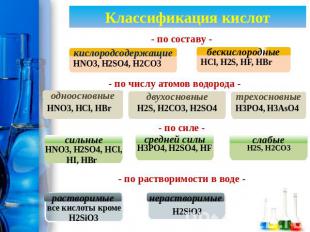
Классификация кислот

Общие химические свойства кислотОпыт №2. Взаимодействие кислот с основаниямиДанная реакция является универсальной, т.к. протекает между любыми кислотами и основаниями.

Общие химические свойства кислотОпыт №3. Взаимодействие кислот с оксидами металловУсловия протекания данной реакции:В ряду напряжений металл должен стоять до водорода.В результате реакции должна получиться растворимая соль.Нерастворимые кислоты (кремниевая) с металлами не взаимодействуют).Концентрированный раствор серной кислоты и раствор азотной кислоты взаимодействуют иначе, поэтому уравнения реакций этих кислот с металлами записывают по другой схеме.

Общие химические свойства кислотОпыт №4. Взаимодействие кислот с солямиУсловия протекания данной реакции:В результате реакции должен выделяться газВ результате реакции новая кислота или новая соль должны выпадать в осадок

Это интересно!

Закрепление!1. Найдите группу формул кислот:2. Выберите формулу «третьего лишнего» вещества в каждом ряду:

Закрепление!Расположите их в таком порядке, чтобы внизу получилось название индикатора.

Домашнее задание:§ 32 упр. 2, 7 ,8 подготовиться к химическому диктанту

Список литературыРудзитис Г.Е. Химия. 8 класс: учеб. для общеобразоват. учреждений /Г.Е. Рудзитис, Ф.Г. Фельдман. – 13-е изд. - М.: Просвещение, 2009.Настольная книга учителя химии / авт.-сост. Н.Н. Гара, Р.Г. Иванова, А.А. Каверина. – М.АСТ,2002. – 190 с.Обучение химии в 8 классе: метод. Пособие / Т.А. Боровских. – М.: АСТ, 2002. – 237 с. Ил. – (Библиотека учителя химии)