Презентация на тему: Медико-генетическое консультирование

Медико-генетическое консультирование

- отрасль профилактической медицины, главной целью которой является снижение количества генетически обусловленных болезней и врожденных пороков развития. - отрасль профилактической медицины, главной целью которой является снижение количества генетически обусловленных болезней и врожденных пороков развития. Цель генетической консультации - установление степени генетического риска в обследуемой семье и разъяснение супругам в доступной форме медико-генетического заключения.

Что такое медико-генетическое консультирование? «… коммуникативный процесс, связанный с решением проблем относительно появления или риска появления генетических болезней в семье. Этот процесс заключается в попытке одного или более квалифицированных специалистов помочь пациенту или его семье в следующих вопросах: понять медицинские факты, включающие диагноз, возможное течение болезни и доступное лечение оценить пути наследования болезни и риск ее повторения определить возможность принятия решения исходя из величины повторного риска выбрать ряд действий в соответствии с этим решением, принимая во внимание риск и семейные цели помочь консультирующимся лучше адаптироваться к болезни и риску повторения этой болезни в семье …»

Задачи медико-генетического консультирования: ретро- и проспективное консультирование семей и больных с наследственной или врожденной патологией; пренатальная диагностика врожденных и наследственных заболеваний; помощь врачам различных специальностей в постановке диагноза заболевания, если для этого требуются специальные генетические методы исследования; доведение пациенту и его семье в доступной форме информации о степени риска иметь больных детей и оказание им помощи в принятии решения; ведение территориального регистра семей и больных с наследственной и врожденной патологией и их диспансерное наблюдение; пропаганда медико-генетических знаний среди населения.

Иначе говоря, задачей генетической консультации является составление генетического прогноза в семье индивидуума с аномалией физического, психического либо полового развития и выбор профилактических мероприятий по предупреждению рождения больного ребенка. Иначе говоря, задачей генетической консультации является составление генетического прогноза в семье индивидуума с аномалией физического, психического либо полового развития и выбор профилактических мероприятий по предупреждению рождения больного ребенка.

Составление генетического прогноза включает три этапа 1 этап. Определение степени генетического риска. Под генетическим риском понимается вероятность (от 0 до 100%) возникновения определенной аномалии у самого пациента (пробанда) или его родственников. Общий риск проявления генетически обусловленной аномалии для популяций европейцев составляет 3-5% (генетический груз), поэтому риск, который не превышает 5%, расценивается как низкий. Генетический риск до 10% называется повышенным в легкой степени, до 20% - повышенным в средней степени и свыше 20% - высоким.

Расчеты генетического риска Существуют два способа расчета генетического риска: теоретические расчеты, основанные на генетических закономерностях, и эмпирические данные. Для менделирующих заболеваний теоретические основы оценки риска сводятся к идентификации и вероятностной оценке определенного дискретного генотипа, лежащего в основе заболевания. При сложно наследующихся заболеваниях нет специфического дискретного генотипа, ответственного за развитие болезни, поэтому консультирование часто основывается на чистом эмпиризме, на методе «черного ящика»

2 этап. Оценка тяжести медицинских и социальных последствий предполагаемой аномалии. Степень генетического риска далеко не всегда соответствует степени тяжести ожидаемой патологии. Например, полидактилия (аутосомно-доминантный тип наследования, высокая степень генетического риска - не менее 50%) может быть легко устранена соответствующей корригирующей операцией, и человек может вести нормальный образ жизни, в то время как фенилкетонурия, риск возникновения которой у детей гетерозиготных родителей составляет 25%, - это тяжелое заболевание, плохо поддающееся лечению. Во втором случае степень страдания с медицинской точки зрения и социальных последствий для больного и его семьи расценивается как тяжелая. 2 этап. Оценка тяжести медицинских и социальных последствий предполагаемой аномалии. Степень генетического риска далеко не всегда соответствует степени тяжести ожидаемой патологии. Например, полидактилия (аутосомно-доминантный тип наследования, высокая степень генетического риска - не менее 50%) может быть легко устранена соответствующей корригирующей операцией, и человек может вести нормальный образ жизни, в то время как фенилкетонурия, риск возникновения которой у детей гетерозиготных родителей составляет 25%, - это тяжелое заболевание, плохо поддающееся лечению. Во втором случае степень страдания с медицинской точки зрения и социальных последствий для больного и его семьи расценивается как тяжелая.

3 этап - врач-генетик должен оценить перспективы применения и эффективность методов пренатальной диагностики. Достижения в этой области позволяют планировать деторождение в семьях с высоким риском наследования тяжелой патологии (болезнь Дауна, мукополисахаридоз, гемофилия, муковисцидоз и др.), так как эти заболевания могут быть выявлены методами пренатальной диагностики. 3 этап - врач-генетик должен оценить перспективы применения и эффективность методов пренатальной диагностики. Достижения в этой области позволяют планировать деторождение в семьях с высоким риском наследования тяжелой патологии (болезнь Дауна, мукополисахаридоз, гемофилия, муковисцидоз и др.), так как эти заболевания могут быть выявлены методами пренатальной диагностики.

Правильное составление медико-генетического прогноза зависит от следующих факторов: Правильное составление медико-генетического прогноза зависит от следующих факторов: точности диагноза, адекватности применения методов расчета генетического риска, знакомства с новейшими данными литературы,

Показания для направления семьи в медико-генетическую консультацию: наличие сходных заболеваний у нескольких членов семьи; первичное бесплодие супругов; привычное невынашивание беременности; отставание ребенка в умственном и физическом развитии; рождение ребенка с врожденными пороками развития; первичная аменорея, особенно с недоразвитием вторичных половых признаков; кровное родство между супругами.

Группы населения, обращающиеся в медико-генетическую консультацию

Структура обращений в медико-генетическую консультацию

Основные группы патологии в медико-генетической консультации
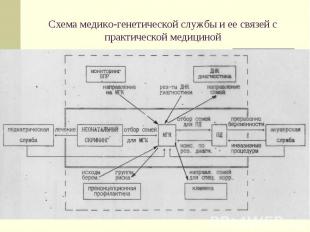
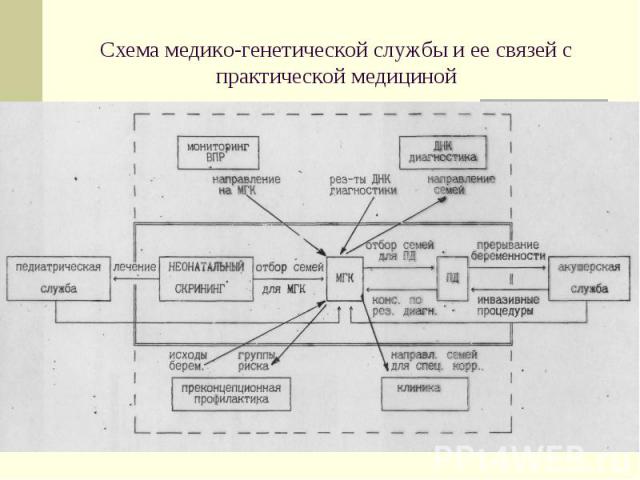
Схема медико-генетической службы и ее связей с практической медициной

Уровни медико-генетической помощи населению

Морально-этические проблемы При медико-генетическом консультировании существует ряд трудностей морально-этического характера: вмешательство в семейную тайну (возникает при сборе данных для построения родословных, при выявлении носителей патологического гена, при несовпадении паспортного и биологического отцовства и др.; проблема разрешается корректным отношением врача к пациенту); ответственность врача-генетика в случае совета консультирующимся на основании вероятностного прогноза (необходимо, чтобы пациент правильно понял медико-генетическую информацию, консультант не должен давать категорических советов (окончательное решение принимают сами консультирующиеся).

Задача МГК с социальной точки зрения – помощь семье в принятии правильного решения Врач-генетик должен помочь консультирующимся понять медицинские факты, тип наследования заболевания, генетический риск его повторения в семье, лучше адаптироваться к несчастью и принять правильное решение относительно дальнейшего деторождения. Эффективность МГК напрямую зависит от грамотного выполнения этой коммуникативной функции врача-консультанта.
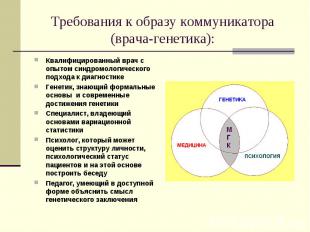
Требования к образу коммуникатора (врача-генетика): Квалифицированный врач с опытом синдромологического подхода к диагностике Генетик, знающий формальные основы и современные достижения генетики Специалист, владеющий основами вариационной статистики Психолог, который может оценить структуру личности, психологический статус пациентов и на этой основе построить беседу Педагог, умеющий в доступной форме объяснить смысл генетического заключения

Дородовая (пренатальная) диагностика наследственных заболеваний - предусматривает их своевременное выявление. Таким образом, пренатальная диагностика связана с решением ряда биологических и этических проблем до рождения ребенка, так как при этом речь идет не об излечении болезни, а о предупреждении рождения ребенка с патологией, не поддающейся лечению. Пренатальная диагностика позволяет перейти от вероятностного к однозначному прогнозированию исхода беременности.

Общие показания к проведению пренатальной диагностики Повышенный генетический риск рождения ребенка с наследственным или врожденным заболеванием. Тяжелый характер заболевания, оправдывающий прерывание беременности Отсутствие удовлетворительного способа лечения предполагаемого заболевания Наличие точного диагностического теста Согласие семьи на проведение пренатальной диагностики и прерывание беременности по показаниям

Методические подходы к пренатальной диагностике Требования к методам: Высокая точность метода Небольшая опасность осложнений Маленький срок беременности Минимальный срок получения результата

Методы пренатальной диагностики В настоящее время применяются непрямые и прямые методы пренатальной диагностики. При непрямых методах обследуют беременную (акушерско-гинекологические методы, сыворотка крови на альфа-фетопротеин и др.); при прямых - плод. К прямым неинвазивным (без хирургического вмешательства) методам относится ультрасонография; к прямым инвазивным (с нарушением целостности тканей) – фетоскопия, хорионбиопсия, плацентобиопсия, амниоцентез, кордоцентез.

Непрямые методы Наиболее широкое распространение получила триада методов: исследование уровня альфа-фетопротеина (АФП), содержания хорионического гонадотропина (ХГ) и свободного эстриола в крови женщин во 2-м триместре беременности. Содержание альфа-фетопротеина определяется также в амниотической жидкости, а свободный эстриол - в моче беременных. Отклонения плазматического уровня АФП, ХГ, свободного эстриола у беременной служат индикаторами высокого риска для плода.

Непрямые методы В частности, содержание альфа-фетопротеина в биологических жидкостях повышено при множественных пороках развития, спинномозговой грыже, гидроцефалии, анэнцефалии, пороках развития желудочно-кишечного тракта и др. дефектах. В случаях хромосомных болезней у плода (например, болезнь Дауна) или наличия у беременной сахарного диабета I типа, напротив, концентрация альфа-фетопротеина в крови беременных снижена.

Непрямые методы Хорионический гонадотропин, синтезируемый трофобластом плаценты, определяется уже на 8-9-й дни после зачатия. При исследовании крови женщины во 2-м триместре беременности повышение уровня ХГ и его свободных бета-субъединиц свидетельствует о задержке внутриутробного развития плода, высоком риске его антенатальной гибели. Содержание свободного эстриола в биологических жидкостях беременной женщины отражает фетоплацентарную активность и снижается при патологии плода и нарушении функции плаценты.

Прямые методы Фетоскопия - осмотр плода фиброоптическим эндоскопом, введенным в амниотическую полость через переднюю стенку матки. Метод позволяет осмотреть плод, пуповину, плаценту и произвести биопсию. Фетоскопия сопровождается высоким риском прерывания беременности (до 20%) и технически сложна, поэтому имеет ограниченное применение.
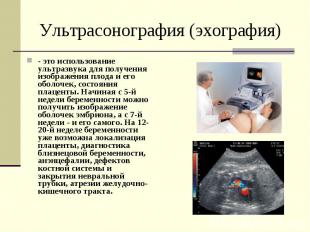
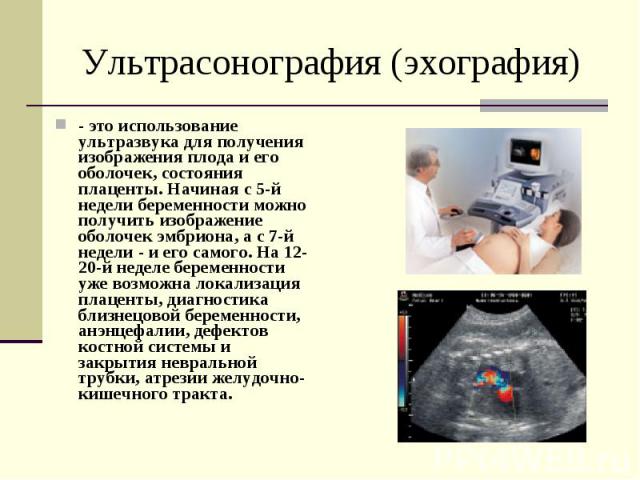
Ультрасонография (эхография) - это использование ультразвука для получения изображения плода и его оболочек, состояния плаценты. Начиная с 5-й недели беременности можно получить изображение оболочек эмбриона, а с 7-й недели - и его самого. На 12-20-й неделе беременности уже возможна локализация плаценты, диагностика близнецовой беременности, анэнцефалии, дефектов костной системы и закрытия невральной трубки, атрезии желудочно-кишечного тракта.

Ультрасонография (эхография) Ультразвуковое исследование позволяет получить данные о размерах плода (длина туловища, бедра, плеча, диаметр головы), о функции миокарда, об объеме амниотической жидкости и размерах плаценты. УЗИ позволяет обнаружить у плода ряд аномалий развития - анэнцефалию, гидроцефалию, поликистоз или агенезию почек, дисплазию конечностей, гипоплазию легких, множественные врожденные пороки, пороки сердца, водянку (отек) плода и плаценты. Выявляется около 70% всех состояний плода, сопровождающихся врожденными пороками развития, как изолированных, так и в составе хромосомных и наследственных синдромов.
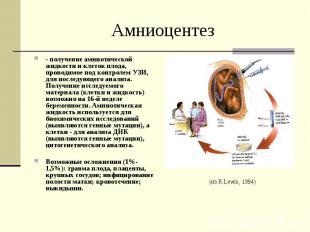
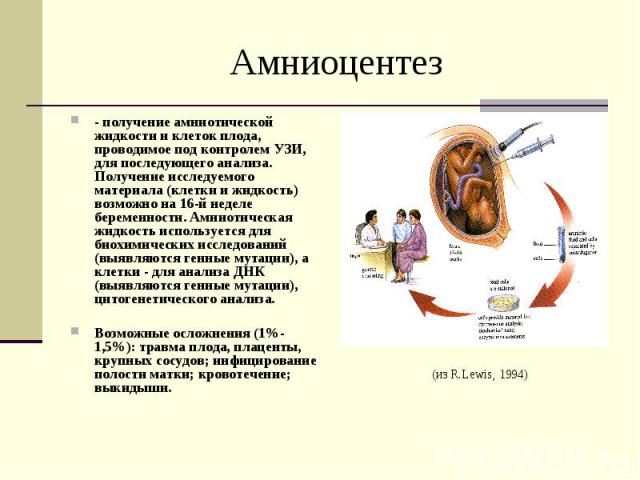
Амниоцентез - получение амниотической жидкости и клеток плода, проводимое под контролем УЗИ, для последующего анализа. Получение исследуемого материала (клетки и жидкость) возможно на 16-й неделе беременности. Амниотическая жидкость используется для биохимических исследований (выявляются генные мутации), а клетки - для анализа ДНК (выявляются генные мутации), цитогенетического анализа. Возможные осложнения (1%-1,5%): травма плода, плаценты, крупных сосудов; инфицирование полости матки; кровотечение; выкидыши.
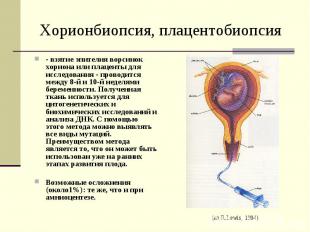
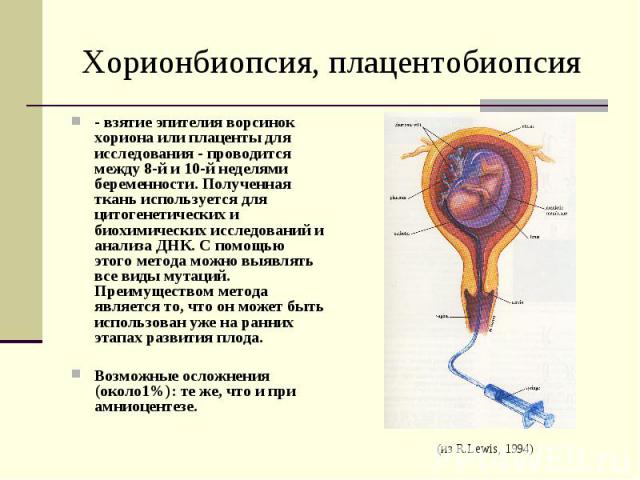
Хорионбиопсия, плацентобиопсия - взятие эпителия ворсинок хориона или плаценты для исследования - проводится между 8-й и 10-й неделями беременности. Полученная ткань используется для цитогенетических и биохимических исследований и анализа ДНК. С помощью этого метода можно выявлять все виды мутаций. Преимуществом метода является то, что он может быть использован уже на ранних этапах развития плода. Возможные осложнения (около1%): те же, что и при амниоцентезе.

Кордоцентез Оптимальные сроки: 16 – 20 недель беременности Акушерские подходы: пункция пуповины. Возможные осложнения минимальные (инфицирование, выкидыши). Диапазон диагностических возможностей: такой же, как и при амниоцентезе.

Современные технологии, помимо перечисленных выше методов, позволяют осуществлять биопсию кожи, мышц, печени плода для диагностики многих наследственных заболеваний. Риск прерывания беременности при применении инвазивных методов пренатальной диагностики составляет 1-2%. Современные технологии, помимо перечисленных выше методов, позволяют осуществлять биопсию кожи, мышц, печени плода для диагностики многих наследственных заболеваний. Риск прерывания беременности при применении инвазивных методов пренатальной диагностики составляет 1-2%. Дальнейшее развитие и распространение методов пренатальной диагностики наследственных заболеваний позволят значительно снизить частоту наследственной патологии новорожденных.