Презентация на тему: Жидкие вещества

Урок химии -8 класс Учитель химии МОУ « СОШ№9» Меркушева И.В 900igr.net

1. Однородная смесь – А) смесь, в которой границу раздела между веществами нельзя заметить невооруженным глазом Б) смесь, в которой границу раздела между веществами можно заметить невооруженным глазом 2. Неоднородная смесь – А) смесь, в которой границу раздела между веществами нельзя заметить невооруженным глазом Б) смесь, в которой границу раздела между веществами можно заметить невооруженным глазом 3. Агрегатное состояние однородной смеси: жидкое, твердое, газообразное; жидкое, твердое; жидкое.

4. Агрегатное состояние чистого вещества: жидкое, твердое, газообразное; жидкое, твердое; жидкое. 5. Смесью веществ является: водопроводная вода; углекислый газ; медь 6. Вещества, применяемые для очистки и обеззараживания питьевой воды: песок, уголь, гравий, хлор; песок, уголь, гравий; песок, уголь; песок 7. Способ разделения смеси из порошка железа и серы: растворение в воде; фильтрование; использование магнита;

Именно водная среда (Мировой океан) могла обеспечить все требования к возникновению и развитию жизни. Она стала тем “питательным бульоном”, в котором 3,5 млрд. лет назад зародилась жизнь на Земле. Живое вещество – это водный раствор, и почти все процессы, обеспечивающие его жизнедеятельность, сводятся к химическим реакциям в водном растворе.


В здоровом организме взрослого человека наблюдается состояние водного равновесия, или водного баланса. Общий объем воды, потребляемый человеком в сутки при питье и с пищей, составляет 2-2,5 л. Через почки и мочевыводящие пути удаляется около 50-60% воды. Потеря 10% воды может привести к необратимым изменениям в организме, а потеря 15-20% приводит к смерти, поскольку кровь настолько густеет, что с ее перекачкой не справляется сердце. В сутки сердце приходится перекачивать около 10000 л. крови.

Массовая доля и молярная концентрация растворённого вещества ?

Массовая доля w растворенного вещества - это отношение его массы mр.в к массе раствора m(р-ра): w = mр.в /m(р-ра), где m(р-ра) = mр.в + m(Н2О).

«Подобное растворяется в подобном”
Растворитель Растворимое вещество Раствор + =
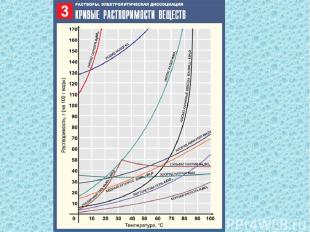

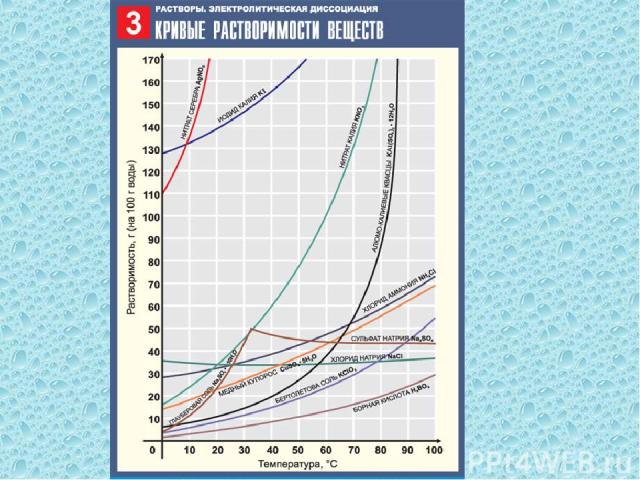
Вещества можно разделить на: Хорошо растворимые (S20 C > 1 г) Малорастворимые (S20 C = 0.01 – 1.0 г) Нерастворимые (S20 C < 0,01 г)

Растворы делятся на: Разбавленные Концентрированные Нассыщенные Ненасыщенные

Задача 1 Вычислите массы поваренной соли и воды, необходимые для приготовления 200 г физиологического раствора (0,9-процентный раствор поваренной соли).

Задача 2 Определите массу сухой соли, которая образуется в чашке после выпаривания 150 г раствора с массовой долей этой соли 15%.

Задача 4 Смешали 200грамм 25% раствора и 500 грамм 35% раствора уксусной кислоты. Определите концентрацию вновь полученного раствора?

Задача 3 Железнодорожная цистерна имеет грузоподъёмность 60 т. Какова масса перевозимой воды при транспортировке 65-процентной азотной кислоты пятидесятивагонным поездом.