Презентация на тему: Введение в аналитическую химию

Преподаватель Ельчищева Юлия Борисовна Преподаватель Ельчищева Юлия Борисовна
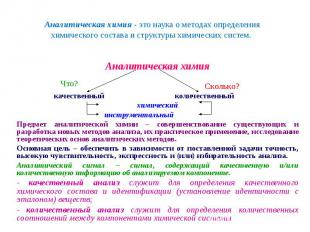

- элементный анализ – это установление наличия и количественного содержания химических элементов в веществе, то есть нахождение его элементного состава; - элементный анализ – это установление наличия и количественного содержания химических элементов в веществе, то есть нахождение его элементного состава; - функциональный анализ – это установление наличия и количественного содержания функциональных групп в молекулах органических соединений; - молекулярный анализ – это установление наличия и количественного содержания молекул индивидуальных химических соединений в веществе, смесях и материалах; - фазовый анализ – это анализ вещества на наличие в нем отдельных фаз, различающихся по своим химическим и физическим свойствам и отделенных друг от друга поверхностями раздела.
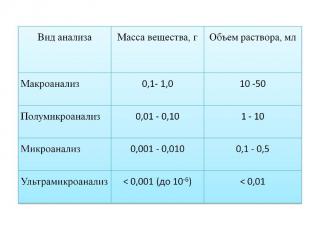


2. Пробоподготовка — совокупность действий над объектом анализа с целью превращения пробы в подходящую для последующего анализа форму, а также для концентрирования/разбавления аналита и избавления от мешающих анализу компонентов. 2. Пробоподготовка — совокупность действий над объектом анализа с целью превращения пробы в подходящую для последующего анализа форму, а также для концентрирования/разбавления аналита и избавления от мешающих анализу компонентов. Основная задача пробоподготовки — подготовка вещества для определнного вида анализа В каком агрегатном состоянии должна быть проба для анализа? Нужно ли отделение мешающих компонентов? Необходимо ли концентрирование/разбавление? Нужно ли перевести анализируемый компонент в определенную форму? 3.Методы разделения и концентрирования: дистилляция, выпаривание, осаждение, экстракция, сорбция, хроматография

4. Проведение химического анализа 4. Проведение химического анализа Титриметрические (волюметрические) методы - измерение объема раствора реактива известной концентрации, расходуемого для реакции с определяемым веществом. Гравиметрические методы - измерение массы определяемого компонента, выделенного в виде веществ определённого состава. Электроаналитические методы - основаны на электрохимических явлениях, происходящих в исследуемой среде или на границе раздела фаз. Спектральные методы - основаны на взаимодействии анализируемого вещества с электромагнитным излучением. Методы разделения основаны на разделении с последующим определением (хроматография, электрофорез) Прочие методы 5. Обработка полученных результатов анализа, используя методы математической статистики.

Химические реакции, при проведении которых наблюдается аналитический эффект (сигнал) называются аналитическими химическими реакциями. Они осуществляются с помощью аналитических реагентов (реактивов) Химические реакции, при проведении которых наблюдается аналитический эффект (сигнал) называются аналитическими химическими реакциями. Они осуществляются с помощью аналитических реагентов (реактивов) Аналитическая реакция - должна протекать достаточно быстро быть практически необратимой. Аналитические реакции делятся на реакции разделения (отделения) и обнаружения (открытия). Реакции разделения служат для практически полного отделения одних веществ (ионов) от других. Реакции обнаружения, которые сопровождаются внешним эффектом (образование осадка, изменение окраски, выделение газообразных продуктов), служат для доказательства наличия в растворе молекул веществ, ионов, функциональных групп в составе органических соединений и т. д. Каждая аналитическая реакция характеризуется чувствительностью или пределом обнаружения (ПО). Для большинства аналитических реакций концентрационный ПО – Сmin = 10-4 – 10-5 г/мл

Способ выполнения Способ выполнения Пробирочный Микрокристаллоскопический Капельный В «замкнутой камере» Пути выполнения «Мокрый» ( реакции, происходящие в растворах) «Сухой» (используемое вещество подвергается обработке (нагреванию, растиранию) в твердом виде (окрашивание пламени, получение цветных стекол).

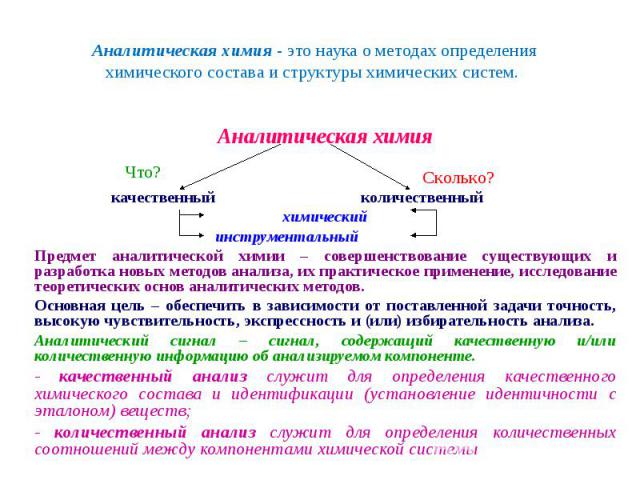
1. Специфические – реакции, характерные только для одного иона или соединения 1. Специфические – реакции, характерные только для одного иона или соединения 3FeСl2 + 2K3[Fe(CN)6] → Fe3[Fe(CN)6]2↓+6KCl (синий, «турнбулева синь») 4FeCl3 + 3K4[Fe(CN)6] → Fe4[Fe(CN)6]3↓+12KCl (синий, «берлинская лазурь») NH4Cl + 2K2[HgI4] + 4KOH → [O(Hg)2NH2]I↓ +KCl +7KI + 3H2O (реакция в «газовой камере») NH4Cl+ NaOH → NH3↑ + H2O (запах аммиака) 2КСl + Na2Pb[CuNO2)6] → K2Pb[Cu(NO2)6]↓ + 2NaCl (микрокристаллоскопическая реакция – черные или темно-коричневые кристаллы кубической формы) CoCl2 + 4NH4CNS → (NH4)2[Co(CNS)4] + 2NH4Cl (капельный метод – розовое окрашивание, при подсушивании – синее)

2. Избирательные (селективные) – реакции, которые дают одинаковый или сходный эффект с несколькими ионами. 2. Избирательные (селективные) – реакции, которые дают одинаковый или сходный эффект с несколькими ионами. (NH4)2C2O4 + Ca2+(Sr2+, Ba2+) → CaC2O4↓ + 2NH4+ (белый осадок) 3. Реакции тождества - основаны на индивидуальных свойствах уже образовавшихся продуктов, например, на способности осадков растворяться в кислотах, щелочах . Для повышения селективности: Методы удаления мешающих ионов или их “маскировка”. Используют реакции осаждения, окисления-восстановления и комплексообразования. Использование методов разделения, т.е. избирательного распределения компонентов анализируемой системы между двумя разделяющимися фазами. Наибольшее значение в практике анализа имеют осаждение, экстракция, хроматография и ионный обмен.









![1. Специфические – реакции, характерные только для одного иона или соединения 1. Специфические – реакции, характерные только для одного иона или соединения 3FeСl2 + 2K3[Fe(CN)6] → Fe3[Fe(CN)6]2↓+6KCl (синий, «турнбулева синь») 4FeCl3 + 3K4[Fe(CN)6] … 1. Специфические – реакции, характерные только для одного иона или соединения 1. Специфические – реакции, характерные только для одного иона или соединения 3FeСl2 + 2K3[Fe(CN)6] → Fe3[Fe(CN)6]2↓+6KCl (синий, «турнбулева синь») 4FeCl3 + 3K4[Fe(CN)6] …](https://fs1.ppt4web.ru/images/95289/122867/640/img9.jpg)