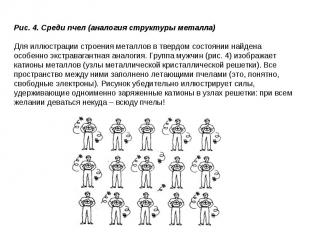
Презентация на тему: ВИДЫ КРИСТАЛЛИЧЕСКИХ РЕШЕТОК

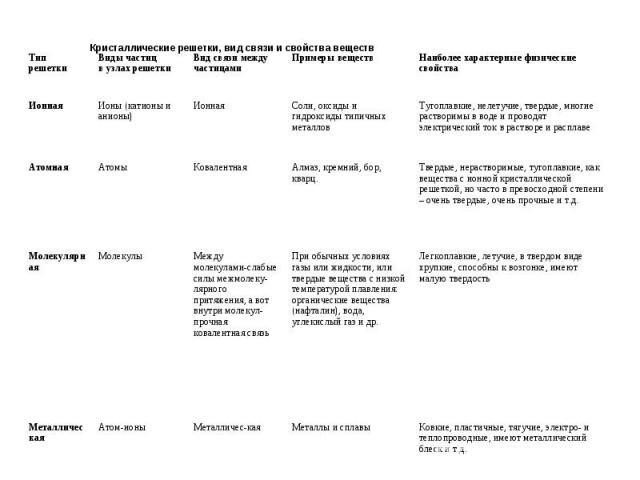
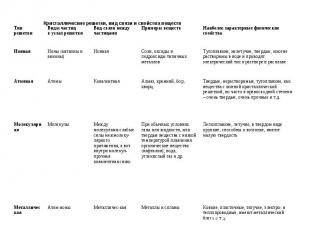
Характеристика Характеристика У веществ с молекулярным строением в узлах кристаллической решетки находятся молекулы с прочными ковалентными связями между атомами. В то же время отдельные молекулы взаимосвязаны гораздо слабее, что делает молекулярный кристалл довольно непрочным. Примеры


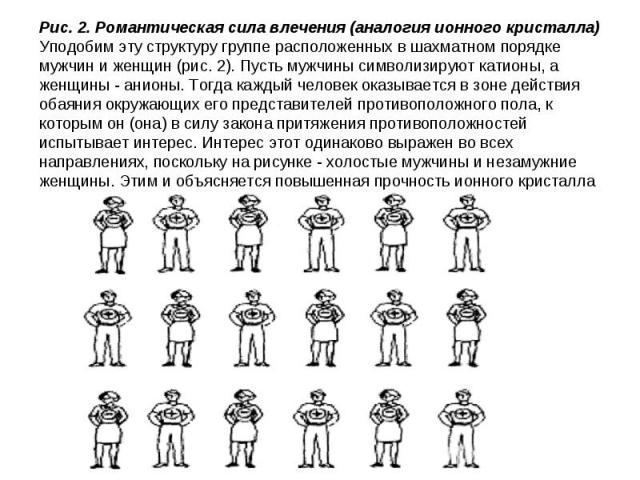
Характеристика Характеристика У веществ с ионной решеткой в узлах расположены разноименно заряженные ионы, удерживаемые силами электростатич. притяжения. Примеры


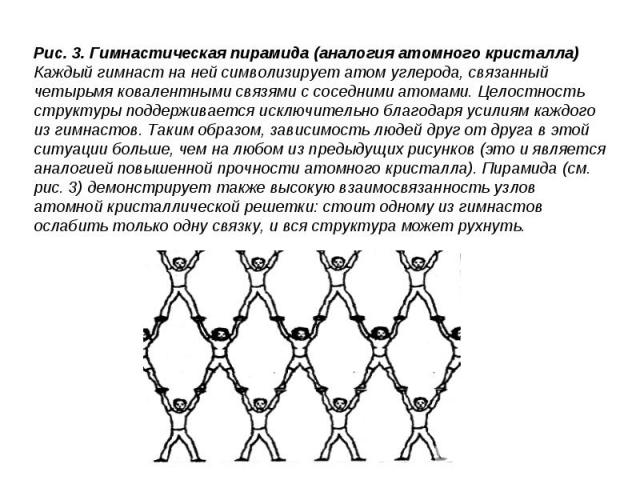
Характеристика Характеристика В узлах атомной кристаллической решетки находятся атомы, связанные прочными ковалентными связями в протяженную пространственную сеть. В этом случае структура отличается таким внутренним единством, что можно сказать, что весь кристалл представляет одну молекулу. Пример

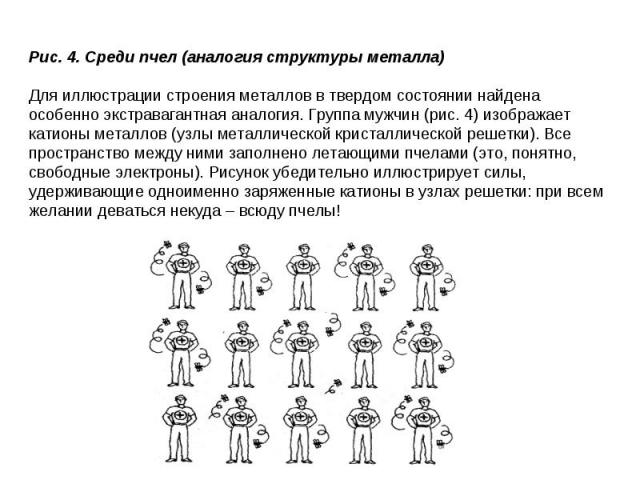
Характеристика Характеристика Этим типом кристаллической решетки обладают металлы с металлической химической связью. Примеры

а) ионы а) ионы в) молекулы б) атомы г) атом-ионы

а) металлическая а) металлическая в) ионная б) ковалентная г) сила межмолекул. взаимодействия

а) очень прочная а) очень прочная в) слабая б) прочная г) разной прочности

а) твердые а) твердые в) жидкие б) газы

а) кристаллические а) кристаллические б) аморфные

а) металлической а) металлической в) атомной б) молекулярной г) ионной

а) металлической а) металлической в) молекулярной б) ионной г) атомной

а) молекулярную а) молекулярную в) ионную б) атомную г) металлическую

а) молекулярную а) молекулярную в) ионную б) металлическую г) атомную

а) молекулярную а) молекулярную в) ионную б) атомную б) металлическую

1-а, 2-б, 3-в, 4-а, 5-б, 6-в, 7-а, 8-б, 9-в, 10-а. 1-а, 2-б, 3-в, 4-а, 5-б, 6-в, 7-а, 8-б, 9-в, 10-а. или абв-абв-абв-а