Презентация на тему: Растворы


Раствор – гомогенная система, переменного химического состава, состоящая из двух и более компонентов: растворитель и растворенное вещество (вещества). Раствор – гомогенная система, переменного химического состава, состоящая из двух и более компонентов: растворитель и растворенное вещество (вещества).


Коллоидные растворы - размер частиц Коллоидные растворы - размер частиц 10-5 - 10-7 см. Примером коллоидных ДС служат растворы клея и желатины. Коллоидные растворы отличаются тем, что их частицы сильно рассеивают проходящий через них свет и делают заметным путь пропущенного светового луча (эффект Тиндаля). Истинные растворы – размер частиц 10-7 - 10-8 см, это гомогенные, устойчивые ДС.

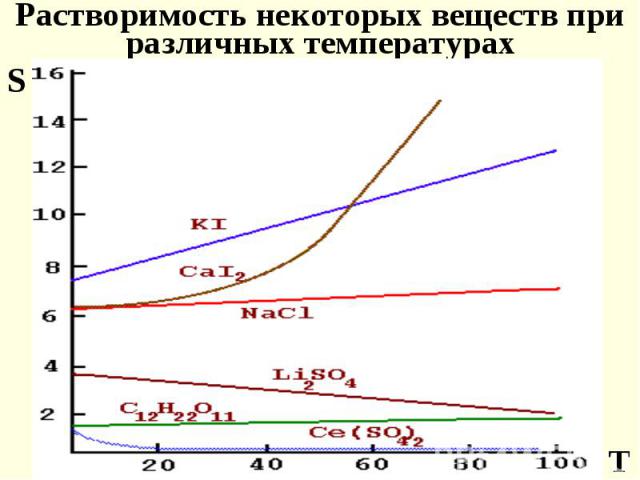
по отношению к равновесию (растворимое вещество – раствор) по отношению к равновесию (растворимое вещество – раствор) ( насыщенный, ненасыщенный, перенасыщенный) Насыщенный раствор – находится в равновесии с твердым не растворившемся веществом, т.е. скорость растворения равна скорости его кристаллизации. Концентрация насыщенного раствора наз. растворимостью с указанием температуры, при которой она определена.

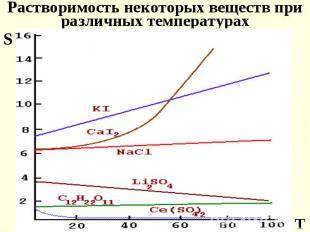
Растворимость - число моль растворенного Растворимость - число моль растворенного в-ва в одном литре раств-ля (в состоянии насыщения) Коэфф. растворимости - масса раств-го компонента в 100 г. раств-ля Ненасыщенный раствор - содержит раств-го в-ва меньше равновесного кол-ва, т.е. скорость растворения больше скорость кристаллизации. Перенасыщенный раствор - скорость кристаллизации больше скорость растворения.


Массовая доля ( ) - отношение массы раств-го в-ва к общей массе раствора: =
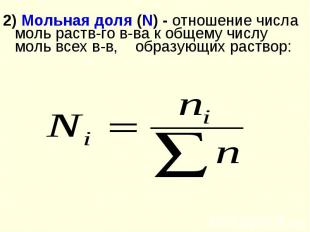
2) Мольная доля (N) - отношение числа моль раств-го в-ва к общему числу моль всех в-в, образующих раствор:

3) Моляльность(Сm) - отношение числа моль растворенного вещества к массе растворителя:

Молярная концентрация вещества (См) – отношение числа моль растворенного вещества к объему раствора

2)Молярная конц-ция эквивалентов в-ва (Сэ) – 2)Молярная конц-ция эквивалентов в-ва (Сэ) – кол-тво (моль) эквивалентов растворенного вещества в 1 л раствора.

3) Титр (Т) - масса (г) растворенного вещества в 1 мл р-ра

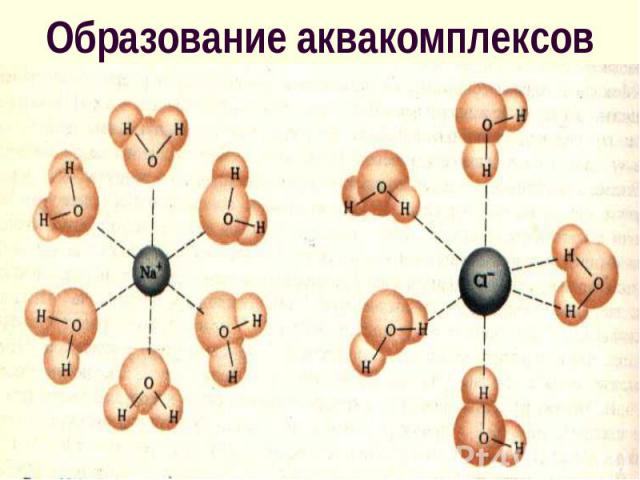
Физико-химическая теория растворов разработана Физико-химическая теория растворов разработана Д.И. Менделеевым, И.А. Каблуковым, В.А. Кистяковским и др. Основной принцип теории: между компонентами р-ров образуются хим. соединения определенного состава - сольваты (гидраты)

Между частицами внутри сольватов существует сильное взаимодействие и часто они образуют комплексы, в которых осуществляется донорно-акцепторное взаимодействие Между частицами внутри сольватов существует сильное взаимодействие и часто они образуют комплексы, в которых осуществляется донорно-акцепторное взаимодействие [Cu(H2O)6]Cl2 [Fe(H2O)6]Cl3 [Be(H2O)4]Cl2

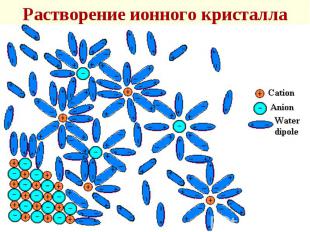
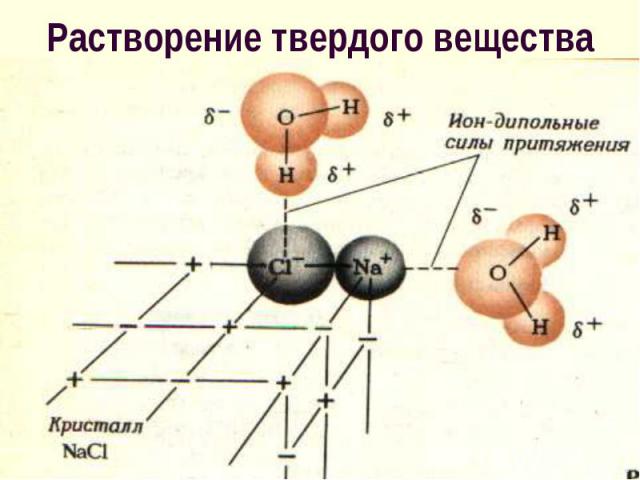
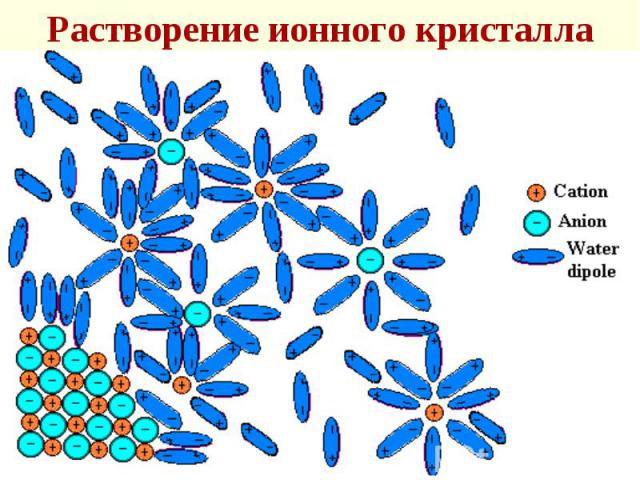
твердого вещества в жидкости состоит в том, что молекулы растворителя образуют с поверхностными молекулами (атомами, ионами) химические связи, при этом ослабляются связи этих молекул внутри твердого вещества твердого вещества в жидкости состоит в том, что молекулы растворителя образуют с поверхностными молекулами (атомами, ионами) химические связи, при этом ослабляются связи этих молекул внутри твердого вещества
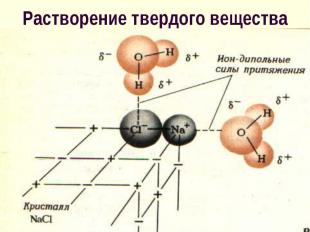

В итоге образовавшийся комплекс отрывается и диффундирует в р-р В итоге образовавшийся комплекс отрывается и диффундирует в р-р Этот процесс обратим и с увеличением концентрации в-ва скорость обратного процесса (кристаллизации) становится все больше, сравниваясь со скоростью растворения
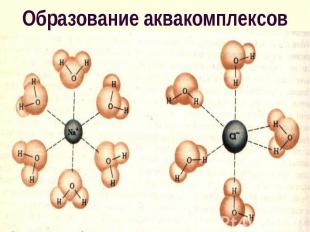

Растворение - это химическое взаимодействие, которое проявляется в изменении объема раствора и тепловом эффекте Растворение - это химическое взаимодействие, которое проявляется в изменении объема раствора и тепловом эффекте

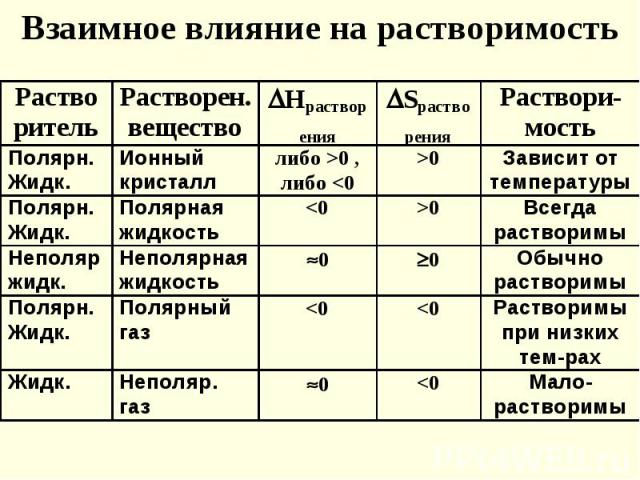
Если тип межмолекулярных связей в компонентах р-ра и между ними одинаков, то возможны любые соотношения между компонентами р-ра Если тип межмолекулярных связей в компонентах р-ра и между ними одинаков, то возможны любые соотношения между компонентами р-ра

Примеры: Примеры: бесконечная растворимость спирта в воде (водородные связи) орг. в-в в орг-ких жидкостях (ван-дер-ваальсовы силы) ограниченная раств-сть солей (ионная связь) в воде (водородная связь)

Раств-сть полярных в-в опр-ся природой раств-ля. Большое значение имеет его диэл-кая проницаемость ( ) : чем она больше, тем легче диссоциация на ионы, т.к. Раств-сть полярных в-в опр-ся природой раств-ля. Большое значение имеет его диэл-кая проницаемость ( ) : чем она больше, тем легче диссоциация на ионы, т.к. По этой причине многие соли лучше растворяются в воде ( = 80), чем в спирте ( = 25)

При растворении происходит три процесса: 1) перехода компонентов из индивидуального состояния в раствор (фазовый переход); При растворении происходит три процесса: 1) перехода компонентов из индивидуального состояния в раствор (фазовый переход); 2) гидратация; 3) диффузия Энтальпия растворения равна сумме энтальпий этих процессов: ΔНр-ния = ΔНф.п + ΔНгидр

Экзотермическое растворение - при растворении газа или жидкости энтальпия фазового перехода меньше энтальпии гидратации и растворение сопровождается выделением тепла. Экзотермическое растворение - при растворении газа или жидкости энтальпия фазового перехода меньше энтальпии гидратации и растворение сопровождается выделением тепла. Эндотермическое растворение – при растворении кристаллических веществ требуется значительная энергия (энергия кристаллической решетки) на их разрушение, которая больше энтальпии гидратации, и в этом случае процесс растворения сопровождается поглощением тепла.

При растворении газов энтропия уменьшается. При растворении газов энтропия уменьшается. При растворении твердых веществ увеличивается. Растворение жидкостей сопровождается также увеличением энтропии. Образование раствора происходит самопроизвольно, энергия Гиббса процесса растворения отрицательна: ΔGр-ния = ΔНр-ния – Т·ΔSр-ния < 0
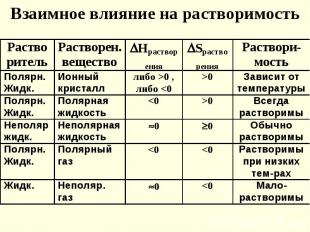

При условии ΔGр-ния< 0, раствор является ненасыщенным. При условии ΔGр-ния< 0, раствор является ненасыщенным. При увеличении концентрации раствора энтропия уменьшается, и энтропийный фактор становится равным энтальпийному. Наступает состояние равновесия, при котором ∆Gр-ния= 0. Такой раствор называется насыщенным. При охлаждении образуются пересыщенные растворы.

в жидкостях и тв. телах идет без разрушения крист. решетки в жидкостях и тв. телах идет без разрушения крист. решетки теплота растворения определяется теплотой гидратации, которая всегда Н 0 (при нагревании растворимость ум-ся) уменьшается объем газа при его поглощении ( V 0), что соответствует S 0 это приводит к уменьшению растворимости с ув-ем температуры

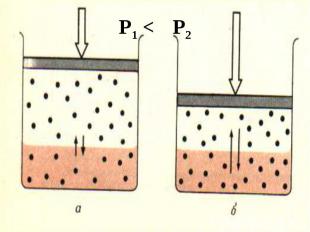
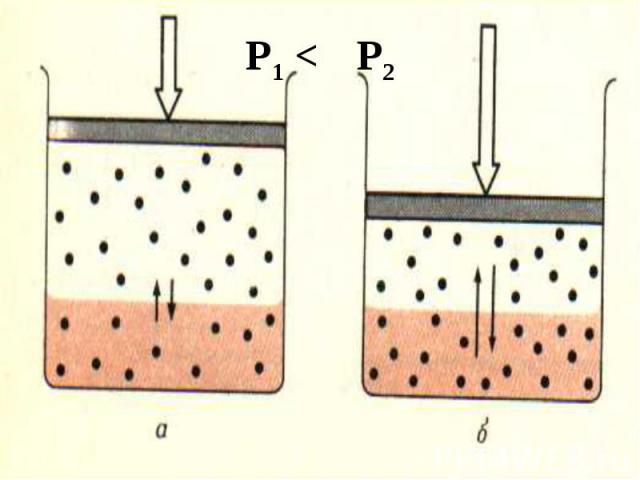
Закон Генри Закон Генри Растворимость газа в жидкостях (и в твердых веществах) при постоянной температуре пропорциональна его давлению: Si = K•Pi Для смеси газов их раств-сти пропорциональны парциальным давлениям

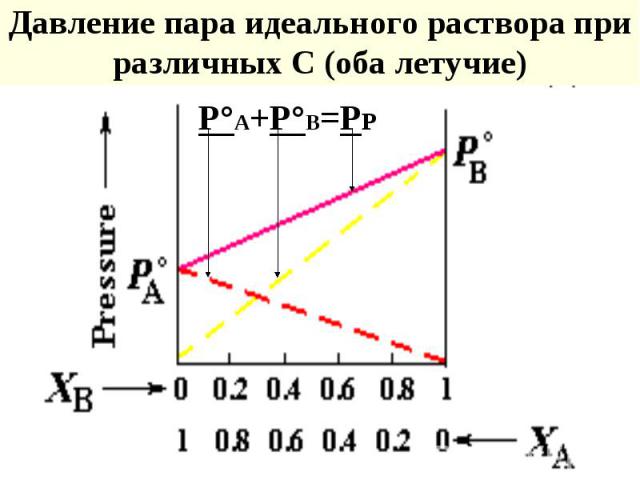
Р-ры неэлектролитов по свойствам приближаются к идеальным газам Р-ры неэлектролитов по свойствам приближаются к идеальным газам Их свойства пропорциональны конц-циям компонентов, они аддитивны (обусловлены коллективом частиц), поэтому их называют коллигативными св-вами

Коллигативные свойства Коллигативные свойства давление пара раств-ля над раствором температура кипения температура замерзания осмотическое давление

Обозначения: Растворенное вещество - нелетучее Р1 давление пара растворителя над раствором P10 - давление пара над чистым растворителем N1 и N2 мольные доли растворителя и раств-го в-ва
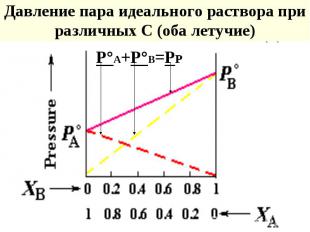

Если одно из веществ нелетучее Если одно из веществ нелетучее Для чистого растворителя: N1 = 1 ; P1 = P10 = K Для р-ра : P1 = P10 . N1 т. к. N1 = 1 - N2 , то P1 = P10 (1 - N2 ) P1 - P10 = P10 N2 Р = P10 N2 Понижение давления насыщ.пара растворителя над раствором пропорционально мольной доле раствор-го в-ва

Повышение температуры кипения и понижение температуры замерзания р-ров пропорциональны моляльной концентрации растворенного вещества Повышение температуры кипения и понижение температуры замерзания р-ров пропорциональны моляльной концентрации растворенного вещества Tk = E•Cm Е - эбулиоскопическая константа; Сm - моляльная концентрация, моль/кг Tз = K•Cm К - криоскопическая константа

Осмос - явление односторонней диффузии через полупроницаемую перегородку Осмос - явление односторонней диффузии через полупроницаемую перегородку Осмотическое давление равно тому давлению, которое имело бы раств-ное вещество, будучи в газообразном состоянии в объеме раствора

Растворы имеющие одинаковые осмотические давления наз изотоническими. Растворы имеющие одинаковые осмотические давления наз изотоническими. Гипертонический раствор – имеет большее осмотическое давление, чем раствор сравнения. Гипотонический р-р - имеет меньшее осмотическое давление, чем раствор сравнения.


объясняет отклонения ряда растворов от законов Рауля и Вант-Гоффа объясняет отклонения ряда растворов от законов Рауля и Вант-Гоффа Эти растворы обладали электропроводностью большей, чем чистый растворитель

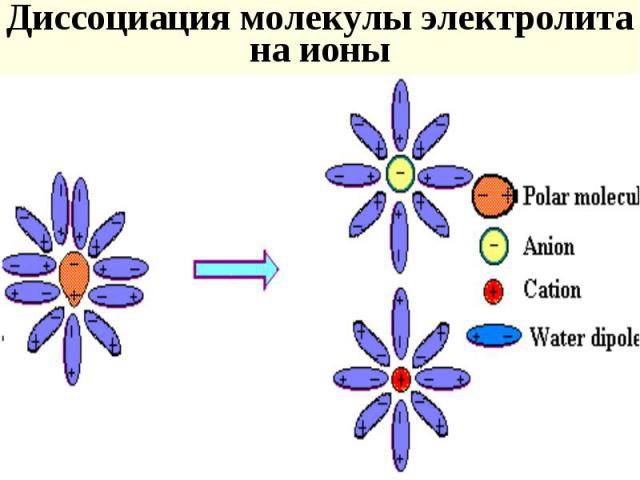
Основные положения: Основные положения: Растворяясь, в-во диссоц-ет на ионы Ионы в р-ре гидратируются (сольватируются) Сильно разб-е р-ры электролитов приближаются к идеальным с учетом числа частиц образующихся в растворе

Конц. р-ры отклоняются от свойств идеальных р-ров из-за сильного взаимодействия противоионов, которые образуют сложные частицы, что уменьшает их количество Конц. р-ры отклоняются от свойств идеальных р-ров из-за сильного взаимодействия противоионов, которые образуют сложные частицы, что уменьшает их количество
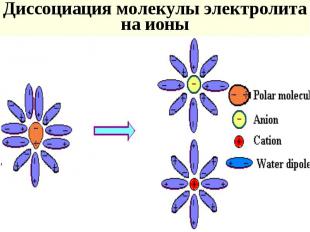

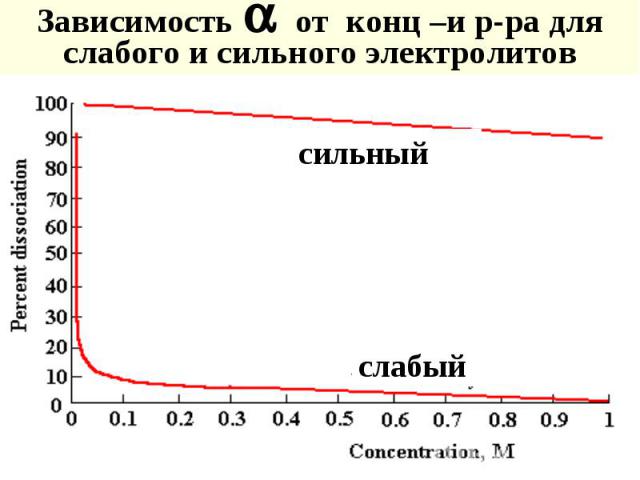
Степень диссоциации электролитов ( ) - отношение числа распавшихся молекул к общему числу растворенных и зависит от концентрации раствора Степень диссоциации электролитов ( ) - отношение числа распавшихся молекул к общему числу растворенных и зависит от концентрации раствора [ доля от 1 или %] - электропр-ость при разбавлении Электролиты делят на слабые ( <0,03), средние (0,03< <0,3), сильные ( >0,3)
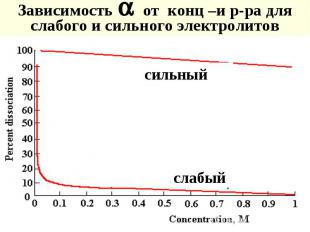

Это константа равновесия электрол-кой диссоциации Это константа равновесия электрол-кой диссоциации KnAm nKm+ + mAn- С СК СА слабые электролиты - КД<10-2 сильные электролиты - КД>10-2

Для слабых электролитов (1- ) 1 и однозарядных ионов (n = m = 1) Для слабых электролитов (1- ) 1 и однозарядных ионов (n = m = 1)

- отношение общего числа частиц в р-ре к числу раств-ных молекул - отношение общего числа частиц в р-ре к числу раств-ных молекул В р-рах электролитов реально существующее число частиц > числа растворенных молекул Поэтому вводится поправочный коэффициент (i), учитывающий изменение числа частиц: i =
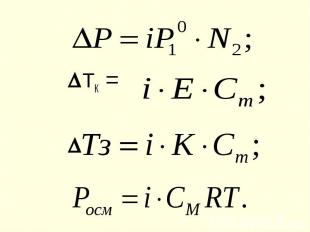
ТК =

KnAm nKm+ + mAn- KnAm nKm+ + mAn- - кажущаяся степень диссоциации сильных электролитов (<100 %) т.к. установлено наличие ассоциатов, агрегатов из гидратированных противоионов

Диссоциация многоосновных кислот и многокислотных оснований идет ступенчато Диссоциация многоосновных кислот и многокислотных оснований идет ступенчато H3PO4 = H2PO4– + H+ К1 = 7,4 10 –3 H2PO4– = НPO42– + H+ К2 = 6,3 10–8 НPO42– = PO43– + H+ К3 = 4,4 10–13

Растворимые средние соли (Na2CO3, NaCl, K2SO4 и др.) - обычно сильные электролиты и диссоц-ют в воде нацело Растворимые средние соли (Na2CO3, NaCl, K2SO4 и др.) - обычно сильные электролиты и диссоц-ют в воде нацело Кислые соли диссоциируют на катион металла и гидроанион: NaHCO3 = Na+ + HCO3– Основные соли - на гидроксокатион и анион: MgOHCl = MgOH+ + Cl–

Равновесие в ионных реакциях смещено в сторону образования нерастворимых соед-ний, газов и слабых электролитов Равновесие в ионных реакциях смещено в сторону образования нерастворимых соед-ний, газов и слабых электролитов К1А1 + К2А2 = К1А2 + К2А1 К1А1 = К1+ + А1-

а) Кр > 1 ; К11• К22 > К12 • К21 а) Кр > 1 ; К11• К22 > К12 • К21 б) Кр < 1 ; К11• К22 < К12 • К21 в) Кр реакция необратима

Вода - слабый электролит Вода - слабый электролит Н2О = Н+ + ОН– Ионное произведение воды: Kд.[H2O] = 1,86.10–16.55,5 = = [H+].[OH–] = 10–14 = Кw Кw не зависит от конций ионов
![Кислотность или основность водных растворов характеризуется конц-ей [Н+] или [ОН Кислотность или основность водных растворов характеризуется конц-ей [Н+] или [ОН](https://fs1.ppt4web.ru/images/95241/150277/310/img58.jpg)
Кислотность или основность водных растворов характеризуется конц-ей [Н+] или [ОН–] ионов Кислотность или основность водных растворов характеризуется конц-ей [Н+] или [ОН–] ионов Удобнее использовать логарифмическое выражение: рН = -lg [H+] и pOH = -lg [OH–] Для воды [Н+] = [ОН–] = 10–7 рН = рОН = 7 - нейтральная среда
![Если в растворе: Если в растворе: [Н+] > [ОН–], то рН < 7, а рОН > 7 – Если в растворе: Если в растворе: [Н+] > [ОН–], то рН < 7, а рОН > 7 –](https://fs1.ppt4web.ru/images/95241/150277/310/img59.jpg)
Если в растворе: Если в растворе: [Н+] > [ОН–], то рН < 7, а рОН > 7 – это кислые растворы [Н+] < [ОН–], то рН > 7, а рОН < 7 – это щелочные р-ры pН + pOH = 14

Для трудно растворимых соед-ний Для трудно растворимых соед-ний Ag2СO3 (тв) 2Ag+ р + CO32- р ПРAg2CO3 – произведение растворимости

Ув-ие или ум-ие одной из концентраций ионов приведет к изменению другой ПР связано с раств-стью (S) Для электролита, имеющего катион и анион равного заряда вытекает: ПР = S2 или

Гидролиз (сольволиз) - разложение воды ионами соли Гидролиз (сольволиз) - разложение воды ионами соли Гидролиз сопровождается диссоци-ацией их на ионы, гидратацией этих ионов и взаимодействием молекул воды с ионами Na2CO3 = 2Na+ + CO32– Na+ + H2O CO32– + H2O = HCO3– + OH–
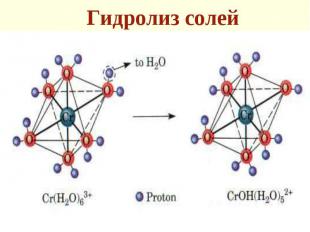

При гидролизе (сольволизе) идет разрыв ков-ной полярной связи в молекуле раств-ля и образование новой связи с ионом соли При гидролизе (сольволизе) идет разрыв ков-ной полярной связи в молекуле раств-ля и образование новой связи с ионом соли Гидролиз тем легче, чем > степень ионности связи в раств-ле и < между молекулой раств-ля и ионом соли Чем > поляризация, тем < ионность и > ковалентность и тем полнее идет гидролиз (сольволиз)

Сильному гидролизу подвергаются: Сильному гидролизу подвергаются: — катионы с сильно поляризующей способностью (Al3+, Fe3+, Bi3+) — анионы с сильной поляризуемостью (CO32–, SO32–, NO2–, CN–, S2– и др.) Не гидролизуются: — слабо поляризующие катионы I и II группы (Na+, Ca2+и др.) — слабо поляризуемые анионы (Hal– , NO3–, SO42–, MnO4–, ClO4–, Cr2O72–)

Сильно поляризующие катионы образуют слабые основания Сильно поляризующие катионы образуют слабые основания сильно поляризуемые анионы образуют слабые кислоты Закономерности гидролиза р-ров солей: — гидролизуются катионы слабых оснований и анионы слабых кислот; Al3+ + H2O = Al(OH)2+ + H+ SO32– + H2O = HSO32– + OH– — не гидролизуются анионы сильных кислот и катионы сильных оснований

h - степень гидролиза (доля гидролизованных частиц) h - степень гидролиза (доля гидролизованных частиц) Кh - константа гидролиза Пример: А– + Н2О = НА + ОН–

Гидролиз соли по катиону: Гидролиз соли по катиону: Гидролиз соли по соли по катиону и аниону:











































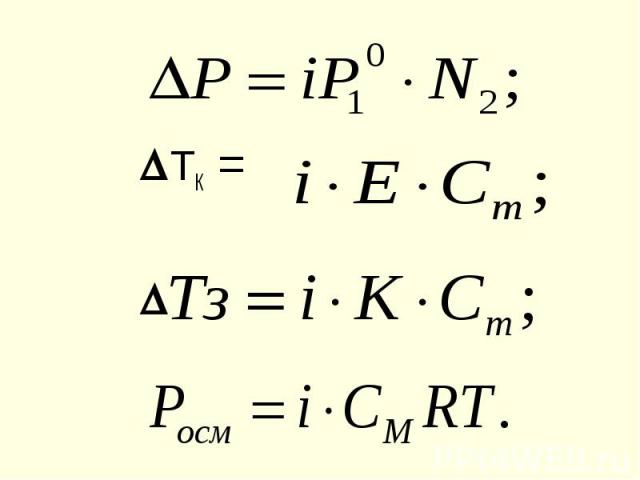





![Вода - слабый электролит Вода - слабый электролит Н2О = Н+ + ОН– Ионное произведение воды: Kд.[H2O] = 1,86.10–16.55,5 = = [H+].[OH–] = 10–14 = Кw Кw не зависит от конций ионов Вода - слабый электролит Вода - слабый электролит Н2О = Н+ + ОН– Ионное произведение воды: Kд.[H2O] = 1,86.10–16.55,5 = = [H+].[OH–] = 10–14 = Кw Кw не зависит от конций ионов](https://fs1.ppt4web.ru/images/95241/150277/640/img57.jpg)
![Кислотность или основность водных растворов характеризуется конц-ей [Н+] или [ОН–] ионов Кислотность или основность водных растворов характеризуется конц-ей [Н+] или [ОН–] ионов Удобнее использовать логарифмическое выражение: рН = -lg [H+] и pOH = -… Кислотность или основность водных растворов характеризуется конц-ей [Н+] или [ОН–] ионов Кислотность или основность водных растворов характеризуется конц-ей [Н+] или [ОН–] ионов Удобнее использовать логарифмическое выражение: рН = -lg [H+] и pOH = -…](https://fs1.ppt4web.ru/images/95241/150277/640/img58.jpg)
![Если в растворе: Если в растворе: [Н+] > [ОН–], то рН < 7, а рОН > 7 – это кислые растворы [Н+] < [ОН–], то рН > 7, а рОН < 7 – это щелочные р-ры pН + pOH = 14 Если в растворе: Если в растворе: [Н+] > [ОН–], то рН < 7, а рОН > 7 – это кислые растворы [Н+] < [ОН–], то рН > 7, а рОН < 7 – это щелочные р-ры pН + pOH = 14](https://fs1.ppt4web.ru/images/95241/150277/640/img59.jpg)