Презентация на тему: Путешествие в Кислоград

Что общего между этими фотографиями?

Путешествие в Кислоград

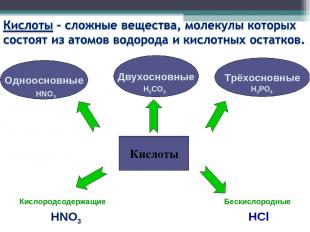
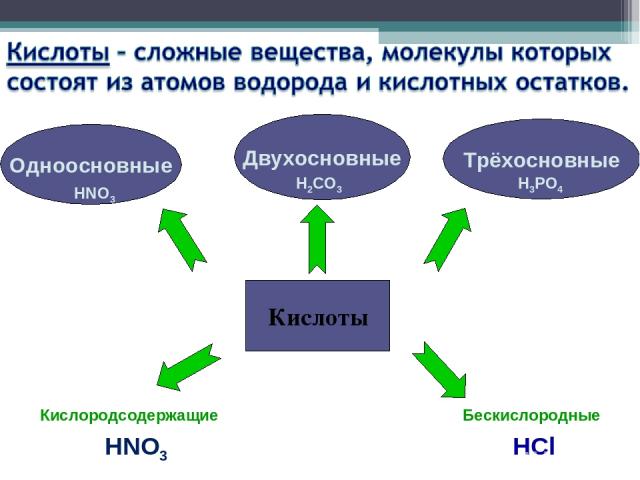
Кислоты Одноосновные Двухосновные Трёхосновные HNO3 H2CO3 H3PO4 Кислородсодержащие Бескислородные HNO3 HCl

Кислоты H2SO4-серная кислота HCl-хлороводородная кислота неорганические; Р H3BO3-борная кислота CH3COOH-уксусная кислота — органическая; Р H2SiO3-кремниевая кислота -- неорганическая; Н

По какому признаку кислоты разделены на группы HNO3 - азотная HNO2 - азотистая HClO4 - хлорная H2SO4 - серная H2SO3 - сернистая H2CO3 - угольная H2SiO3- кремниевая H3PO4 - фосфорная H3BO3 - борная HF - фтороводородная HCl - хлороводородная HBr - бромоводородная HI - йодоводородная H2S - сероводородная

По какому признаку кислоты разделены на группы. HF - фтороводородная HCl - хлороводородная HBr - бромоводородная HI - йодоводородная HNO3 - азотная HNO2 - азотистая HClO4 - хлорная H3PO4 - фосфорная H3BO3 - борная H2S - сероводородная H2SO4 - серная H2SO3 - сернистая H2CO3 - угольная H2SiO3 - кремниевая
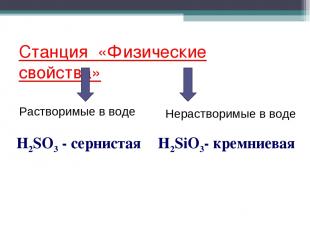
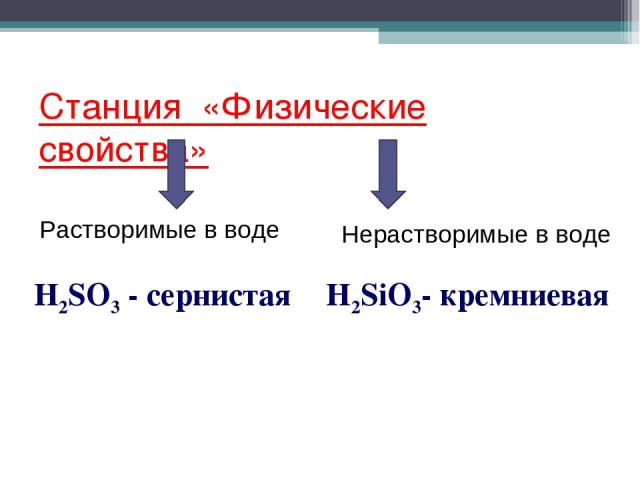
Станция «Физические свойства» Растворимые в воде Нерастворимые в воде H2SiO3- кремниевая H2SO3 - сернистая

Серная кислота

Хлороводородная (соляная) кислота

H3BO3 Борная кислота

Уксусная кислота

ПРАВИЛА ТЕХНИКИ БЕЗОПАСНОСТИ Едкое вещество—кислота! Разрушает и раздражает кожу, слизистые оболочки. Попавшие на кожу капли раствора кислоты немедленно смойте сильной струей холодной воды, а затем обработайте поврежденную поверхность 2%-м раствором питьевой соды.

Станция «Экспериментальная» Химические свойства 1. Взаимодействуют с индикаторами Название индикатора Цвет индикатора в среде кислой щелочной нейтральной Лакмус Синий Фиолетовый Фенолфталеин Малиновый Бесцветный Метиловый оранжевый Желтый Оранжевый

2. Взаимодействует с металлами Zn + 2HCl → ZnCl2 + H2 Cu + HCl → не возможна 3. Взаимодействуют с основными оксидами. CaO + 2HCl → CaCl2 +H2O Fe2O3 + 6HCl→ 2FeCl3 + 3H2O

Лабораторная работа Распознавание кислот Задание 1: проведите опыт, согласно инструкции; сделайте вывод о распознавании кислот среди других растворов. Задание 2: Определите, в каком из пронумерованных стаканов находится раствор лимонной кислоты. 1 балл

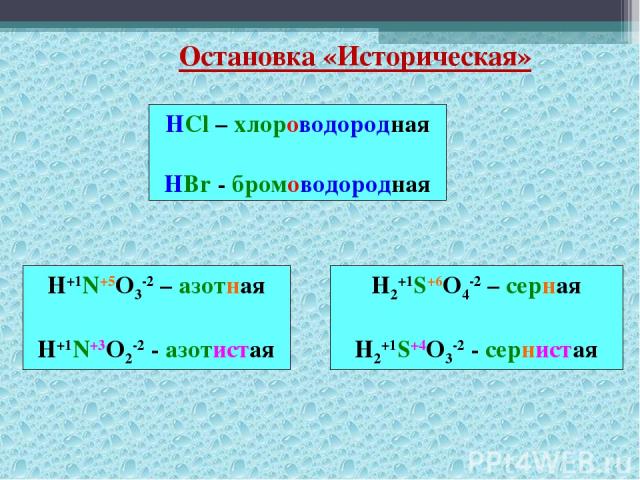
Остановка «Историческая» HCl – хлороводородная HBr - бромоводородная H+1N+5O3-2 – азотная H+1N+3O2-2 - азотистая H2+1S+6O4-2 – серная H2+1S+4O3-2 - сернистая

Формулы кислот H2OSOHBrNa2CО3MgBaH2CO3SO4KOH H3PO4P2O5CaH2SKPHNO2CS2NH3O3C HClBaSHKSHH2Na2OH2SiO3NaClH2SO4 1 балл

1. Укажите номер формулы кислоты : 1) NaCl 2) Na2O 3) HCl 4) NaOH 2. Двухосновной кислотой является: 1) HCl 2) H2SO4 3) HNO3 4) H3PO4 3. Цвет лакмуса в кислой среде: 1) красный 2) фиолетовый 3) оранжевый 4) бесцветный

Схема составления: 1 строчка – существительное 2 строчка – два прилагательных 3 строчка – 3 глагола 4 строчка – предложение из 4-х слов. 5 строчка – синоним к слову из 1 строчки

Домашнее задание: 1) §20 упр.1,4 2) Индивидуальное задание: Какие кислоты Вы используете дома? Отчего укусы муравьев так болезненны?