Презентация на тему: "Электрохимический ряд напряжений металлов. Общие химические свойства металлов". 11-й класс


Цель урока: Повторить и обобщить общие химические свойства металлов с учетом их положения в ЭХРНМ

Задачи урока: Повторить общие химические свойства металлов Объяснить зависимость свойств металлов от их положения в ЭХРНМ Выполнить упражнения на написание уравнений химических реакций, характеризующих общие химические свойства металлов Провести диагностику и коррекцию знаний

Вспомним! Положение металлов в ПСХЭ Особенности строения атомов металлов (радиус атома, количество электронов на внешнем энергетическом уровне, электроотрицательность) Способность к принятию или отдаче электронов
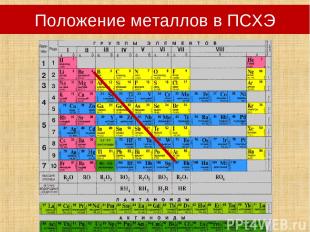
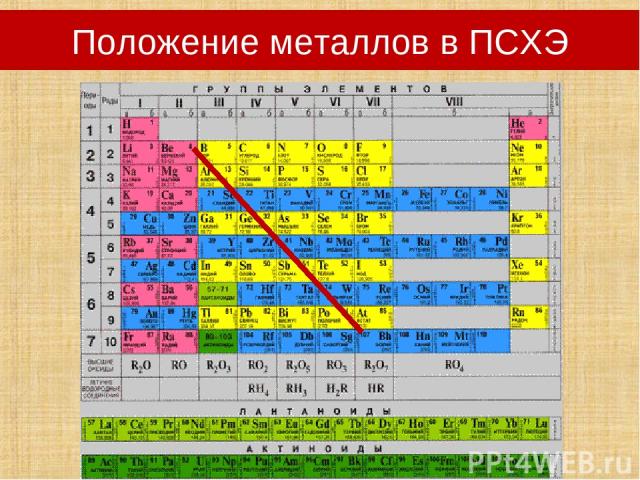
Положение металлов в ПСХЭ

2 8 1 11p + 1 12n 0 1

Вывод: Атомы металлов – ……………. электроны с внешнего энергетического уровня, поэтому являются ………………………..

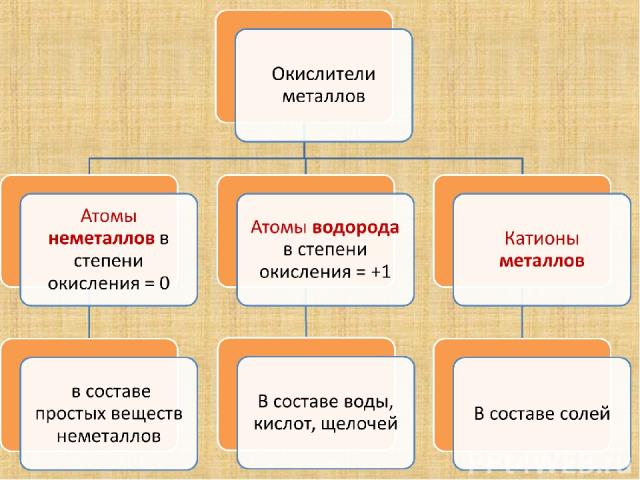
Атомы металлов – восстановители, а катионы металлов? Катионы металлов принимают электроны, и являются окислителями
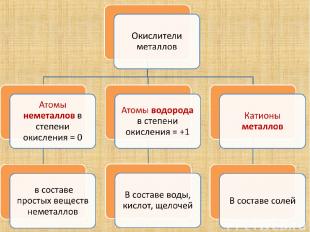

Металлы взаимодействуют С неметаллами с образованием бинарных соединений (оксидов, гидридов, сульфидов, галогенидов и др.) С водой с образованием щелочей или оксидов и выделением водорода С растворами кислот с образованием солей и выделением водорода С растворами солей с образованием новой соли и нового металла

Электрохимический ряд напряжений металлов. Стр. 201

4 правила ЭХРНМ 1. Чем левее стоит металл в ЭХРНМ тем более сильным восстановителем он является 2. Каждый металл способен вытеснять из растворов солей те металлы , которые в ЭХРНМ стоят правее его Опыт 1 3. Металлы, находящиеся в ряду напряжений левее водорода, вытесняют его из кислот в растворе Опыт 2 4. Металлы, являющиеся самыми сильными восстановителями (щелочные и щелочноземельные ), в водных растворах взаимодействуют прежде всего с водой Опыт 3 ↓

Металлы после водорода… Взаимодействие с концентрированной серной кислотой при нагревании Cu + 2H2SO4 = CuSO4 + 2H2O + SO2↑

Металлы после водорода… Взаимодействие с концентрированной и разбавленной азотной кислотой. Опыт - 4 Cu + 4HNO3 = Cu(NO3)2 + 2H2O + NO2↑ 3Cu + 8HNO3 = 3Cu(NO3)2 + 4H2O + 2NO↑

Металлы после водорода… 3. Взаимодействие золота с «царской водкой» Au + HNO3 + 4HCl = H[AuCl4] + NO + 2H2O

Подведем черту… Металл + кислород = оксид металла Металл + хлор = хлорид металла Металл + сера = сульфид металла Металл + вода = щелочь (оксид) + H2 Металл + кислота (р) = соль + H2 Металл + соль (р) = соль + металл

Подведем черту… Металл + серная кислота (к) = соль + вода + «Х», где «Х» - SO2, S, H2S в зависимости от положения металла в ЭХРНМ Металл + азотная кислота = соль + вода + «У» где «У» - NO2, NO, N2O, N2, NH3 в зависимости от положения металла в ЭХРНМ и концентрации кислоты

Напишите реакции: калий + вода = гидроксид калия + водород кальций + вода = гидроксид кальция + водород цинк + вода = оксид цинка + водород олово + вода = оксид олова (II) + водород металлы, стоящие в ЭХРНМ до водорода, взаимодействуют с водой с образованием щелочи и водорода или с образованием оксида и водорода. Это зависит от их активности.

железо + соляная кислота = хлорид железа (II) + водород никель + серная кислота = сульфат никеля (II) + водород металлы, стоящие в ЭХРНМ до водорода, взаимодействуют с растворами кислот (кроме азотной) с образованием растворимой соли и водорода.

железо + сульфат меди (II) = медь + сульфат железа (II) медь + нитрат ртути (II) = ртуть + нитрат меди (II) металлы взаимодействуют с растворами солей. Согласно ЭХРНМ, каждый более активный металл вытесняет менее активный из раствора соли. НЕ БРАТЬ АКТИВНЫЕ МЕТАЛЛЫ!

Диагностика Напишите реакции взаимодействия магния с кислородом, хлором, азотом, водой, соляной кислотой, хлоридом меди(II) Напишите реакцию взаимодействия цинка с концентрированной серной кислотой при нагревании. Определите с какими из перечисленных веществ (H2SO4(p), H2SO4(к), MgCl2, CuSO4) при обычных условиях взаимодействует железо. Составьте уравнения возможных реакций, укажите в них окислитель и восстановитель, запишите процессы окисления и восстановления.

Решение диагностики: 1. 2Mg +O2 = 2MgO Mg +Cl2 = MgCl2 3Mg +N2 = Mg3N2 Mg +2H2O = Mg(OH)2 +H2 Mg +2HCl = MgCl2 +H2 Mg +CuCl2 = MgCl2 + Cu 4Zn +5H2SO4(конц) = 4ZnSO4 +4H2O + H2S↑ Fe + H2SO4 = FeSO4 + H2↑ Fe + CuSO4 = FeSO4 + Cu

Домашнее задание Выполните задания диагностики для следующих металлов: 1 задание для лития Li 2 задание для ртути Hg и концентрированной азотной кислоты HNO3 3 задание для цинка Zn













![Металлы после водорода… 3. Взаимодействие золота с «царской водкой» Au + HNO3 + 4HCl = H[AuCl4] + NO + 2H2O Металлы после водорода… 3. Взаимодействие золота с «царской водкой» Au + HNO3 + 4HCl = H[AuCl4] + NO + 2H2O](https://fs3.ppt4web.ru/images/132111/178672/640/img14.jpg)