Презентация на тему: Реакция электролиза

Государственное общеобразовательное учреждение - средняя общеобразовательная школа при Посольстве России в Турции Электролиз расплавов и растворов (изучение темы при подготовке обучающихся к сдаче ЕГЭ, базовый уровень) урок химии, 11 класс Автор: Попова Елена Игоревна, учитель химии и биологии 5klass.net


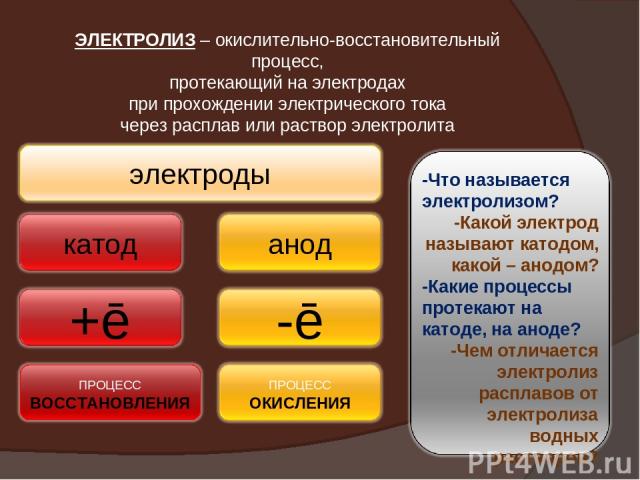
ЭЛЕКТРОЛИЗ – окислительно-восстановительный процесс, протекающий на электродах при прохождении электрического тока через расплав или раствор электролита

Процессы на КАТОДЕ Катионы активных металлов Катионы менее активных металлов Катионы неактивных металлов Li+, Cs+, Rb+, K+, Ba2+, Sr2+, Ca2+, Na+, Mg2+, Be2+, Al3+ Mn2+, Cr3+, Zn2+, Ga3+, Fe2+, Cd2+, In3+, Tl+, Co2+, Ni2+, Mo4+, Sn2+, Pb2+ Bi3+, Cu2+, Ag+, Hg2+, Pd3+, Pt2+, Au3+ Тяжело разряжаются (только из расплавов), в водном растворе электролизу подвергается вода с выделением водорода Н2 В водном растворе восстанавливаются металл (при малой концентрации катионов в растворе — металл и водород) Металл, Н2 Легко разряжаются и восстанавливается только металл Металл


Процессы на АНОДЕ Анионы кислородсодержащих кислот Гидроксид-ионы; анионы бескислородных кислот (кроме F−) PO43−, CO32−, SO42−, NO3−, NO2−, ClO4− OH−, Cl−, Br−, I−, S2− Тяжело разряжаются (только из расплавов), в водном растворе электролизу подвергается вода с выделением кислорода О2 Легко разряжаются неметаллы



Алгоритм составления уравнений электролиза: Исходные частицы Процесс Продукты Металл M – nē = Mn+ Ионы металла Анионы бескислородных кислот. S2– > I– > Br – > Cl– 2Hal– –2ē = Hal2 Свободные неметаллы Анионы кислот с промежуточной степенью окисления элемента SO32–, NO2–, и т.п. SO32– + H2O –2ē = SO42–+2H+ Анионы кислот с высшей степенью окисления элемента Анионы карбоновых кислот 2RCOO––2ē = R-R + 2CO2 Углеводороды и оксид углерода(IV) Гидроксид-ион 4OH– – 4ē = O2 + 2H2O Кислород Вода 2H2O – 4ē = O2 + 4H+ Кислород Анионы кислот с высшей степенью окисления элемента SO42–, NO3–, и т.п. SO42– –2ē = S2O82– Перекисные соединения Фторид-ион 2F– –2ē = F2 Фтор

П р и м е р 3. Установите соответствие между формулой вещества и итоговым уравнением электролиза его водного раствора. Формула вещества Уравнение электролиза А) CuSO4; 1) 2AgF = 2Ag + F2; Б) KCl; 2) 4AgF + 2H2O = 4Ag + 4HF + O2; В) AgF; 3) 2CuSO4 + 2H2O = 2Cu + 2H2SO4 + O2; Г) NaNO3. 4) 2KCl + 2H2O = H2 + 2KOH + Cl2; 5) NaNO3 + H2O = NaOH + HNO3; 6) 2H2O = 2H2 + O2.


Учебник: п. 19, записи в тетради, упр. 8,9, задача 2 (стр. 88) Сборник: стр.90-91, № 6-18 (чётные), стр. 92, №20-24

Использованная литература: Химия: основы общей химии: учеб. для 11 кл. ОУ: базовый уровень/Г.Е. Рудзитис, Ф.Г. Фельдман - М., Просвещение, 2008 Репетитор по химии/Под ред. А.С. Егорова. – Ростов н/Д: Феникс, 2005г. Химия. 11-й класс. Тематические тестовые задания для подготовки к ЕГЭ./Авт.-сост. Л.И. Асанова. – Ярославль:Академия развития, 2010 г. Материалы курса «Подготовка выпускников средних учебных заведений к сдаче УГЭ по химии»: лекции 1-4 / О.С. Габриелян, С.А. Сладков – М.: Педагогический университет «Первое сентября», 2010.