Презентация на тему: Квантовые числа

Квантовые числа

Квантовые числа Главное квантовое число n определяет энергетические уровни электрона в атоме. n = 1,2,3,…L = n

Орбитальное квантовое число Принимает значения l = 0, 1, 2,…(n - 1)Определяет величину момента импульса электрона в атоме l = 0 – s-состояниеl = 1 – p-состояниеl = 2 – d-состояниеl = 3 – f-состояние l = 4 – g-состояние
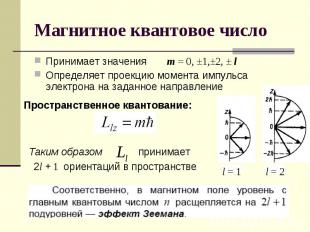
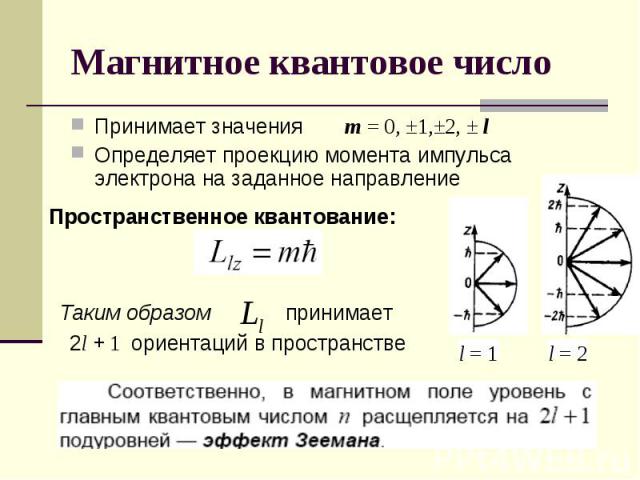
Принимает значения m = 0, ±1,±2, ± lОпределяет проекцию момента импульса электрона на заданное направление Пространственное квантование: Таким образом 2l + 1 ориентаций в пространстве
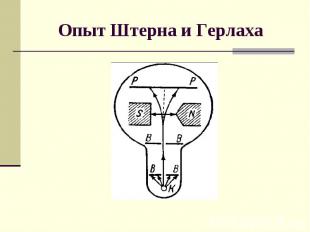
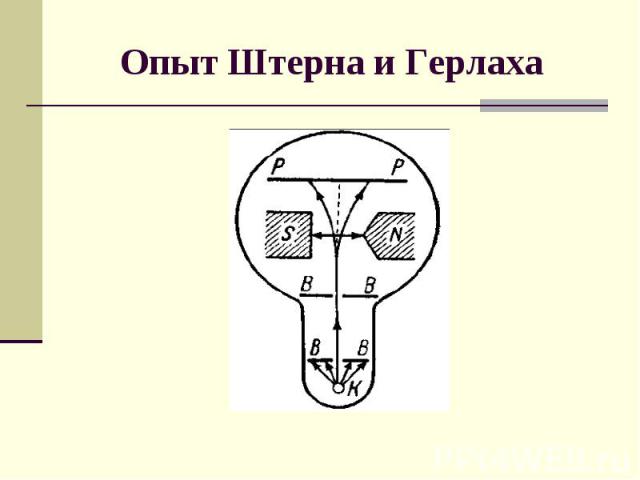
Опыт Штерна и Герлаха
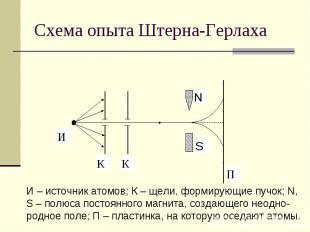
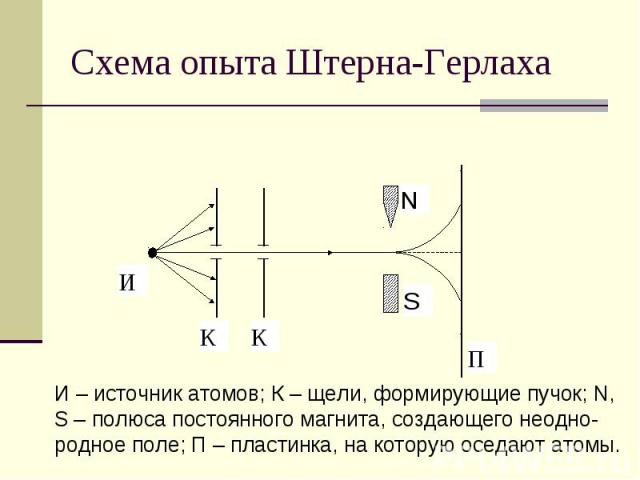
Схема опыта Штерна-Герлаха И – источник атомов; К – щели, формирующие пучок; N, S – полюса постоянного магнита, создающего неодно- родное поле; П – пластинка, на которую оседают атомы.

Результаты опыта Штерна-Герлаха

Спиновое квантовое число (спин) Спин - собственный механический момент импульса электрона s = ½ — спиновое квантовое число Проекция спина на внешнее магнитное поле квантуется ms = ± ½ - магнитное спиновое квантовое число,

Принцип Паули. Распределение электронов в атоме.

Состояние электрона в атоме определяется набором квантовых чисел

Переходы между электронными состояниями возможны только в том случае, если:1) изменение ∆l орбитального квантового числа l удовлетворяет условию∆l = ± 12) изменение ∆m магнитного квантового числа m удовлетворяет условию ∆m = 0, ± 1

В одном и том же атоме не может быть более одного электрона с одинаковым набором четырех квантовых чисел n, l, m, ms . Z(n, l, m, ms) =0 или 1

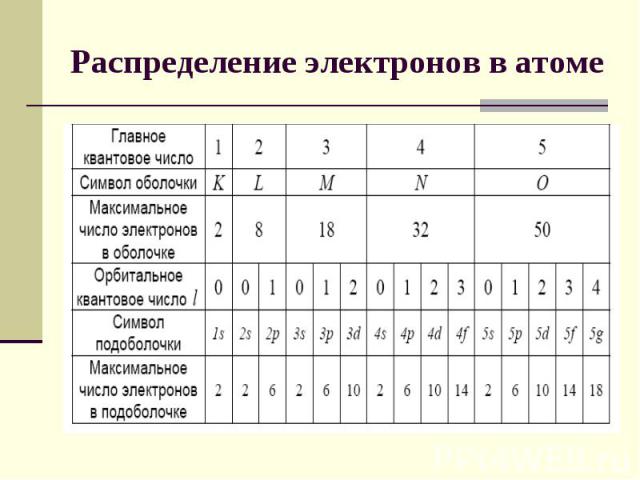
Распределение электронов в атоме по состояниям Совокупность электронов в многоэлектронном атоме, имеющих одно и то же главное квантовое число n , называется электронной оболочкой (слой).Максимальное число электронов, находящихся в состояниях определяемых данным главным квантовым числом, равно В каждой из оболочек электроны распределяются по подоболочкам, соответствующим данному l
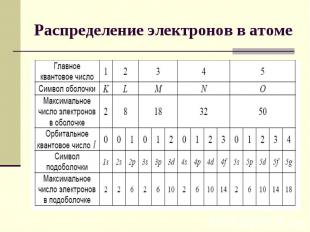
Распределение электронов в атоме

Периодическая система элементов Д.И.Менделеева Дмитрий Иванович МЕНДЕЛЕЕВ(8.II.1834 - 2.II.1907) - великий русский ученый-энциклопедист, химик, физик, технолог, геолог и даже метеоролог. Менделеев был членом более 90 академий наук, научных обществ, университетов разных стран. Он является одним и основателей Русского химического общества; неоднократно избирался его президентом. Имя ученого – Менделеевий – носит 101-й элемент в периодической таблице.

Теория периодической системы элементов Д.И.Менделеева Порядковый номер химического элемента равен общему числу электронов в атоме данного элемента;Состояние электронов в атоме определяется набором их квантовых чисел. Распределение электронов по энергетическим состояниям должно удовлетворять принципу минимума потенциальной энергии;Заполнение электронами энергетических состояний в атоме должно происходить в соответствии с принципом Паули.

Порядковый номер химического элемента равен общему числу электронов в атоме данного элемента;Состояние электронов в атоме определяется набором их квантовых чисел. Распределение электронов по энергетическим состояниям должно удовлетворять принципу минимума потенциальной энергии;Заполнение электронами энергетических состояний в атоме должно происходить в соответствии с принципом Паули.