Презентация на тему: Будщва атома. Дослід Резерфорда.




Історична довідка. 2. Що вивчає ядерна фізика. 3. Ідеї давніх учених щодо атомістичної будови матерії 4. Атомістична теорія в римській науці 5. Модель атома Дж. Томсона



Геологія Археологія Сільське господарство Медицина Хімія

Ідея атомістичної будови матерії була висловлена вперше Левкіппом Левкіпп 500 - 440 р. до н.е.

Вчення Левкіппа розвинуте його учнем – геніальним Демокрітом. На жаль, твори Демокріта не дійшли до нашого часу, і про Їх зміст ми дізнаємося лише з книг інших авторів. Демокріт 430 - 370 р. до н.е.

Суть вчення Все, що існує навколо, складається з атомів і порожнечі. Атоми якісно не відрізняються між собою. У них лише різна величина і форма Вони НЕПОДІЛЬНІ

Демокріт дав їм назву атоми, тобто неподільні Це ніби зернинки, з яких складаються всі тіла Вони рухомі і різноманітно поєднані Атоми існували і будуть існувати завжди
Чому атоми з’єднуються між собою? Одні атоми мають гачки, інші - петельки

Заслуга давніх атомістів Вони своїми геніальними здогадками вказали науці шлях, передбачили майбутній успіх АТОМНОЇ ТЕОРІЇ


Джозеф Джон Томсон(1856 - 1940) – англійський фізик, директор Кавендишської лабораторії, лауреат Нобелівської премії У 1903 році запропонував першу модель атома

У 1897 р. англійський фізик Дж.Дж. Томсон експериментально відкрив електрон як складову частинку атома і носія найменшого електричного заряду. Він припустив, що атом - це позитивно заряджена куля, всередині якої міститься негативно заряджені електрони. Рівномірність їх розподілу в об'ємі кулі та рівність позитивного і негативного зарядів зумовлюють електричну нейтральність атома.

“Модель пудинга” Томсон представив модель атома у вигляді позитивно зарядженої кулі, усередині якої розміщуються електрони. Ця модель називається “моделлю пудинга”, оскільки згідно з нею електрони вкраплені в атом, як родзинки в пудинг.

Плюси і мінуси моделі атома Томсона Переваги: Модель Томсона дозволила з’ясувати періодичність у властивостях елементів Недоліки: Модель Томсона не відповіла на запитання: як саме розподіляються в атомі позитивні і негативні заряди

Німецький фізик Ф. Ленард у 1903 р. запропонував модель “порожнього” атома, в середині якого літають нейтральні частинки, складені із взаємно зрівноважених позитивних і негативних зарядів.

Е. Резерфорд Х. Гейгер О. Лебедєв Н. Бор
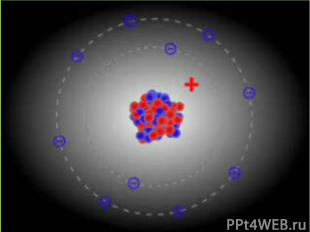

Висновки В центрі атома знаходиться ядро, в якому зосереджено всю його масу і весь позитивний заряд Ядро займає дуже малу частину атома Навколо ядра по замкнених орбітах рухаються електрони

Розміри атома і ядра Згідно із сучасними методами оцінювання Діаметр атома 10-10 м Діаметр ядра 10-15 м

Планетарна модель атома Ядерну модель атома Резерфорда називають ще планетарною моделлю, тому що електрони рухаються по орбітах навколо ядра подібно як планети рухаються по своїх орбітах навколо Сонця. + + + + + + +

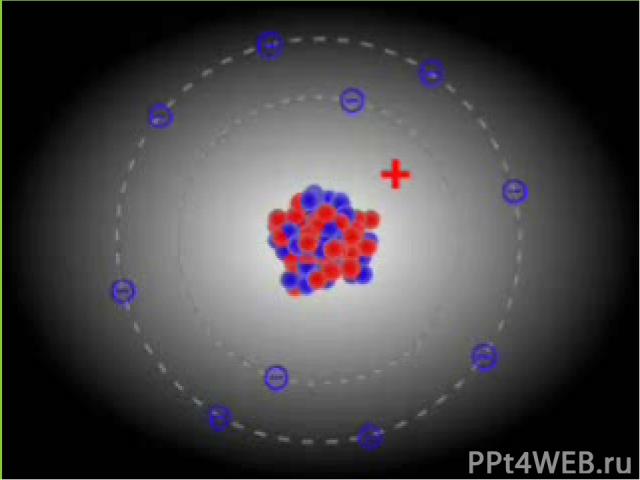
Як виглядає атом:
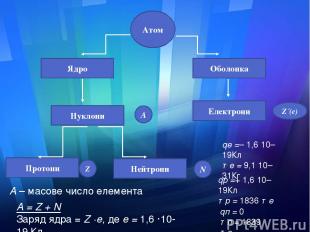
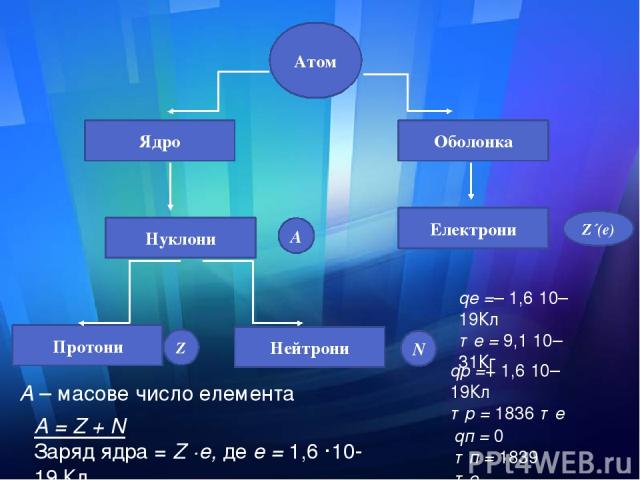
А = Z + N Заряд ядра = Z ·е, де е = 1,6 ·10-19 Кл Атом А N Z Z´(e) Ядро Нуклони Нейтрони Протони Електрони Оболонка qе =– 1,6·10–19Кл те = 9,1·10–31Кг qр =+ 1,6·10–19Кл тр = 1836 те qп = 0 тп = 1839 те А – масове число елемента

. Навчаємося розв'язувати задачі Визначте, яка кількість нукло нів (А), протонів (Z), нейтронів (N) та електро нів (Z ') міститься в нейтральному атомі хімічних елементів 2. У ядрі атома Карбону міститься 12 частинок. Навколо ядра рухаються 6 електронів. Скільки в ядрі цього атома протонів і нейтронів? 3. У ядрі атома Бору 5 протонів і 6 нейтронів. Скільки електронів у цьому атомі? 4. У ядрі атома певного хімічного елемента 31 протон і 39 нейтро нів. Що це за елемент?

Заповніть таблицю Ядро Протони Нейтрони Нуклони Електрони Будова атома 4 1 23 1 2 2 і 3 3 4
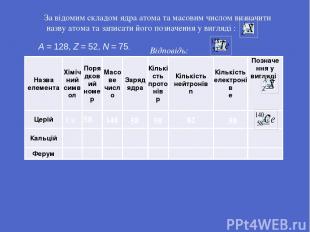
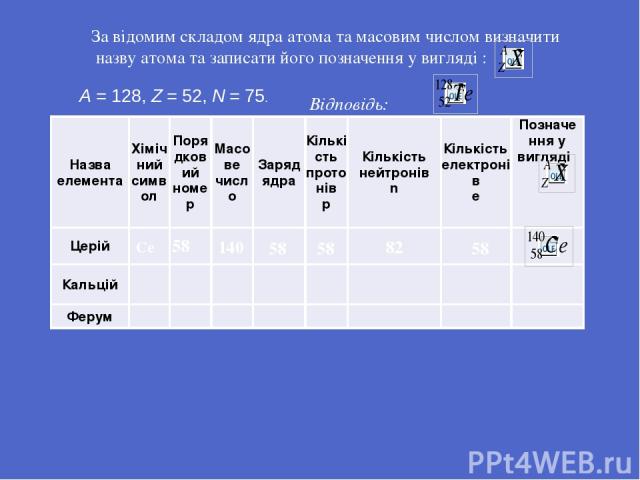
Се 58 58 58 58 82 140 За відомим складом ядра атома та масовим числом визначити назву атома та записати його позначення у вигляді : А = 128, Z = 52, N = 75. Відповідь: Назваелемента Хімічнийсимвол Порядковийномер Масове число Заряд ядра Кількість протонів p Кількість нейтронів n Кількість електронів e Позначення у вигляді Церій Кальцій Ферум

Знайдіть помилки у наступному тексті. «Французький фізик Е. Резерфорд, провівши дослідження будови атомів, запропонував планетарну модель атома. Згідно з цією моделлю, атом складається з електронів що знаходяться в центрі атома й ядра яке рухається навколо електронів. Заряд ядра визначається зарядом нейтронів. Кількість нейтронів і кількість електронів однакова, тому негативний заряд ядра дорівнює за абсолютною величиною сумарному позитивному заряду електронів.

Знайдіть помилки у наступному тексті. «Французький (Англійський) фізик Е. Резерфорд, провівши дослідження будови атомів, запропонував планетарну модель атома. Згідно з цією моделлю, атом складається з електронів (ядра), що знаходяться в центрі атома й ядра (електронів), яке рухається навколо електронів (ядра). Заряд ядра визначається зарядом нейтронів (протонів). Кількість нейтронів (протонів) і кількість електронів однакова, тому негативний (позитивний) заряд ядра дорівнює за абсолютною величиною сумарному позитивному (негативному) заряду електронів.

Вправа «Закінч речення» Модель атома за Резерфордом … ядерна Її ще називають … планетарна Розміри атома … 10 – 10м Розміри ядра … 10 – 15м

Вправа «Закінч речення» Першу модель атома запропонував … Дж. Томсон Він представив модель атома у вигляді … позитивно зарядженої кулі, усередині якої розміщуються електрони Її ще називають … “моделлю пудинга”

Що ми дізналися на уроці Атоми дуже малі — їхні розміри близько 10-10 м, а розміри ядра ще приблизно в 100 000 разів менше 10-15м. Атомне ядро складається з нуклонів — позитивно заряджених протонів і нейтральних нейтронів, що зв'язані між собою за до помогою сильної взаємодії. Навколо ядра обертаються негативно заряджені електрони

Домашнє завдання: Вивчити: § 31. Розв’язати: вправа 28 (3-5) Знайти в Інтернеті: 1. Історія відкриття радіоактивності. 2. Складові радіоактивного випромінювання. 3. Вплив радіації на живи організми. 4. Радіоактивні елементи в періодичній системі

«Чи вірите ви в те, що…» Атом – це складна система, що складається з ядра та електронної оболонки. В центрі атома знаходиться – ядро. Ядро атома не має заряду. Навколо ядра рухаються електрони. Ядро складається з протонів, нейтронів та електронів. Протони - позитивно заряджені частинки. Нейтрони заряджені негативно.

Дякую за роботу на уроці!