Презентация на тему: Строение атома

Строение атома

Ученые древности о строении вещества Древнегреческий ученый Демокрит 2500 лет назад считал, что любое вещество состоит из мельчайших частиц, которые впоследствии были названы «атомами», что в переводе на русский язык означает «неделимый» Долгое время считалось, что атом является неделимой частицей.

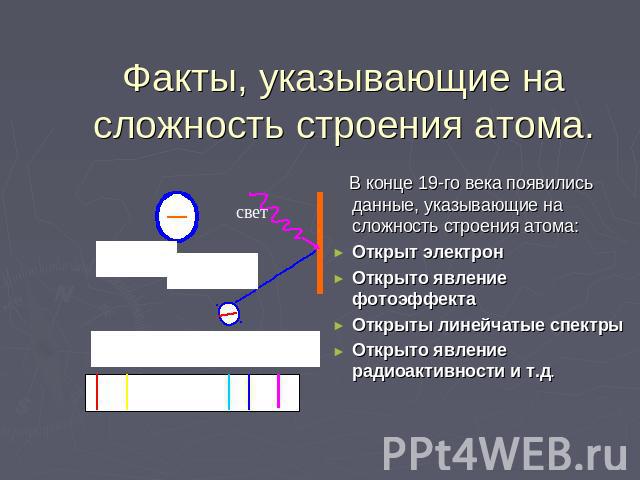
Факты, указывающие на сложность строения атома. В конце 19-го века появились данные, указывающие на сложность строения атома: Открыт электрон Открыто явление фотоэффекта Открыты линейчатые спектры Открыто явление радиоактивности и т.д.
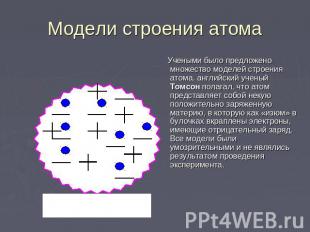
Модели строения атома Учеными было предложено множество моделей строения атома. английский ученый Томсон полагал, что атом представляет собой некую положительно заряженную материю, в которую как «изюм» в булочках вкраплены электроны, имеющие отрицательный заряд. Все модели были умозрительными и не являлись результатом проведения эксперимента.

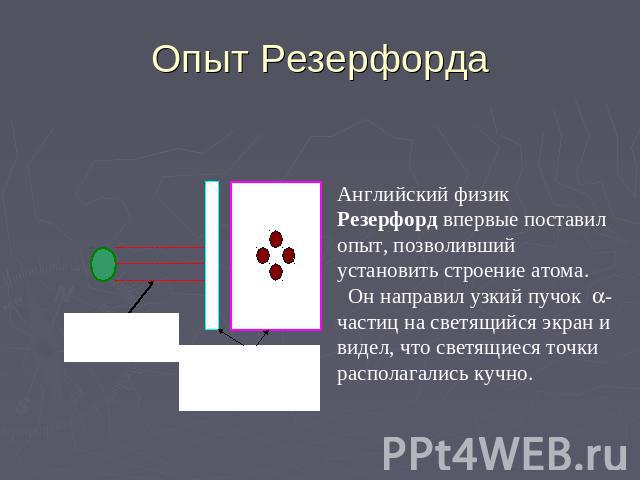
Опыт Резерфорда Английский физик Резерфорд впервые поставил опыт, позволивший установить строение атома. Он направил узкий пучок -частиц на светящийся экран и видел, что светящиеся точки располагались кучно.
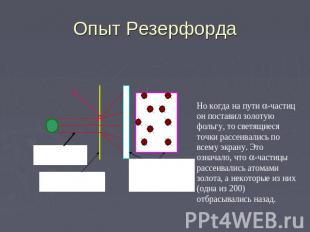
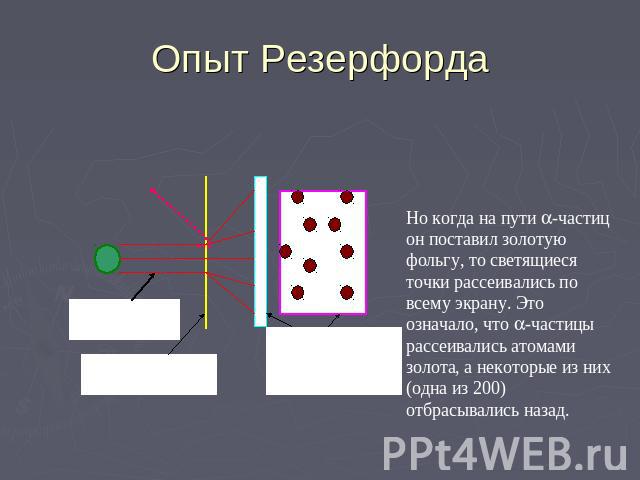
Опыт Резерфорда Но когда на пути -частиц он поставил золотую фольгу, то светящиеся точки рассеивались по всему экрану. Это означало, что -частицы рассеивались атомами золота, а некоторые из них (одна из 200) отбрасывались назад.

Причины рассеивания -частиц Электрон, входящий в состав атома нет мог рассеивать -частиц так как масса -частицы примерно в 8000 раз больше массы электрона. Значит -частицы рассеивались положительным зарядом атома в котором сосредоточена вся масса.

Механизм рассеивания. -частица имеет положительный заряд, поэтому отталкивается от положительного заряда, расположенного где-то внутри атома. При этом чем ближе будет проходить траектория -частицы к положительному заряду атома – тем больше сила действующая на нее, тем сильнее изменится ее траектория.

Вывод из опыта Резерфорда. Учитывая то, что из 2000 испущенных -частиц только одна отбрасывалась назад Резерфорд сделал вывод, что положительный заряд в атоме занимает небольшое пространство, то есть в атоме есть положительно заряженное ядро, а электроны вращаются вокруг ядра.

Строение атома Из опыта Резерфорда следует, что атом устроен следующим образом: в центре атома расположено положительно заряженное ядро размер которого от 10 000 до 100 000 раз меньше размера атома, а по орбите вокруг ядра вращаются электроны. Данная модель строения атома называется планетарной. Заряд ядра по величине равен заряду всех электронов, поэтому атом нейтрален