Презентация на тему: Простые и сложные химические вещества

Вещества: ПРОСТЫЕ: Металлы: Fe, Cu,AI,Zn. Неметаллы: H2, О2, N2, CI2. СЛОЖНЫЕ: Оксиды: СаО, СuO, MgO Основания: Са(ОН)2, Сu(ОН)2, Mg(ОН)2 Кислоты: Н2SO4, НCI, НNO3. Соли: NaCI,NaNO3, CuSO4. 900igr.net

Почему в природе существуют простые и сложные вещества?

ХИМИЧЕСКАЯ СВЯЗЬ Химическая связь-это совокупность сил, удерживающих атомы друг около друга

Варианты соединения атомов: Ме + Ме = металлическая связь Ме + НеМе = ионная связь НеМе + НеМе = ковалентная неполярная связь НеМе + НеМе = ковалентная полярная связь Н2О + Н2О = водородная связь -
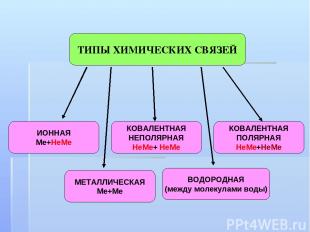
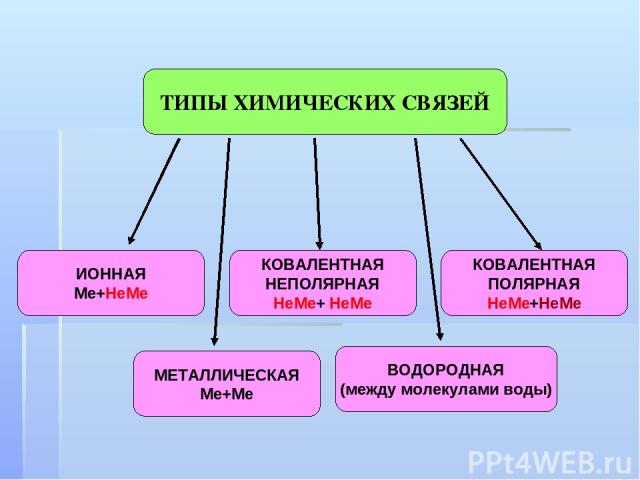
ТИПЫ ХИМИЧЕСКИХ СВЯЗЕЙ ИОННАЯ Ме+НеМе КОВАЛЕНТНАЯ НЕПОЛЯРНАЯ НеМе+ НеМе МЕТАЛЛИЧЕСКАЯ Ме+Ме ВОДОРОДНАЯ (между молекулами воды) КОВАЛЕНТНАЯ ПОЛЯРНАЯ НеМе+НеМе
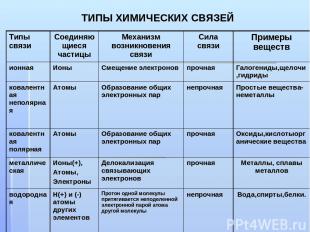
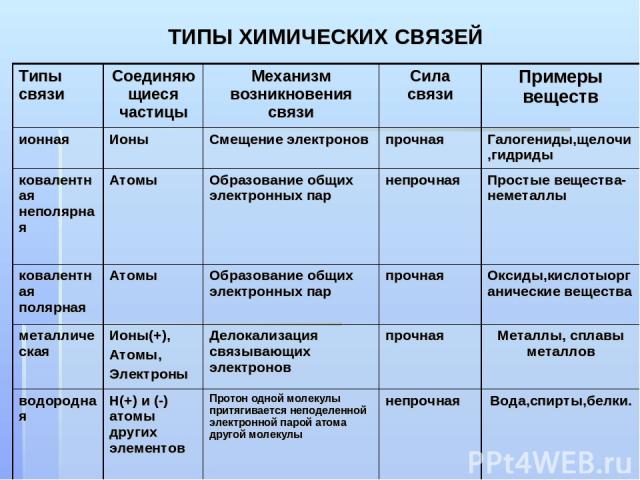
ТИПЫ ХИМИЧЕСКИХ СВЯЗЕЙ Типы связи Соединяющиеся частицы Механизм возникновения связи Сила связи Примеры веществ ионная Ионы Смещение электронов прочная Галогениды,щелочи,гидриды ковалентная неполярная Атомы Образование общих электронных пар непрочная Простые вещества-неметаллы ковалентная полярная Атомы Образование общих электронных пар прочная Оксиды,кислотыорганические вещества металлическая Ионы(+), Атомы, Электроны Делокализация связывающих электронов прочная Металлы, сплавы металлов водородная Н(+) и (-) атомы других элементов Протон одной молекулы притягивается неподеленной электронной парой атома другой молекулы непрочная Вода,спирты,белки.

Физическая природа химической связи ЕДИНА – это ядерно-электронное взаимодействие

Основные понятия: Атом Молекула Простое вещество Сложное вещество Оксид Основание Кислота Соль Атом Молекула Простое вещество Сложное вещество Оксид Основание Кислота Соль

ИОННАЯ СВЯЗЬ Na + CI = Связь между ионами (катионами и анионами) В образовании связи участвуют атомы металлов и неметаллов. е
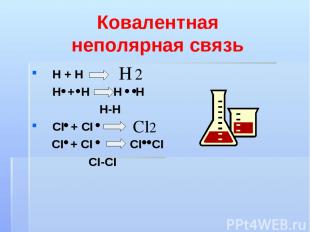
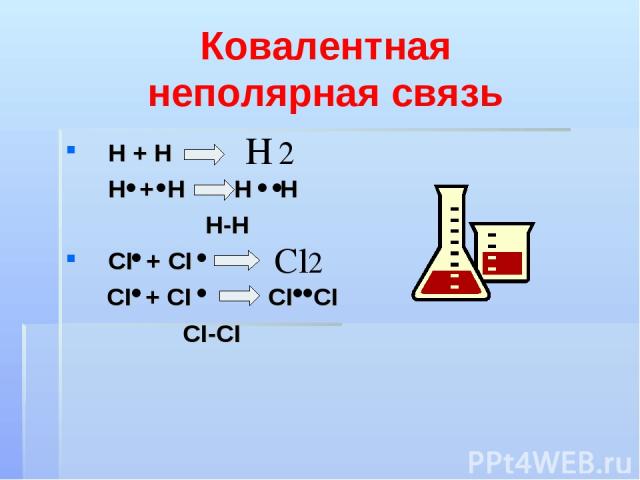
Ковалентная неполярная связь H + H H + Н Н Н Н-Н CI + CI CI + СI СI СI СI-СI
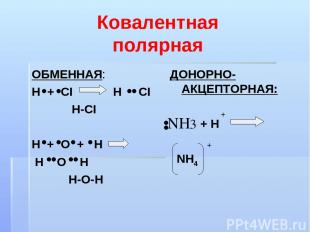
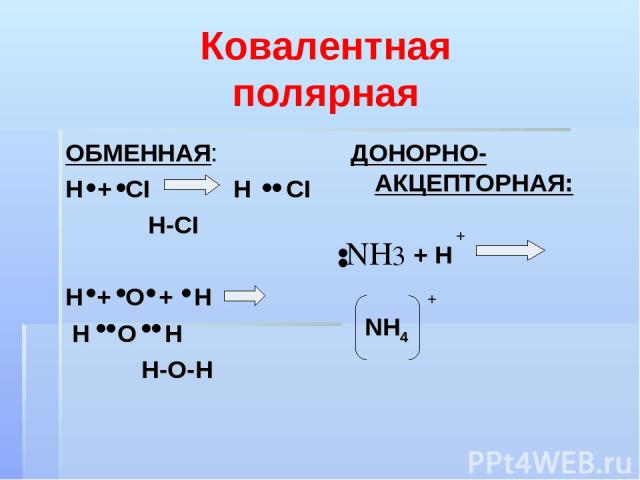
Ковалентная полярная ОБМЕННАЯ: Н + СI Н СI H-CI H + O + H H O H H-O-H ДОНОРНО-АКЦЕПТОРНАЯ: + H NH4 + +

Металлическая СВЯЗЬ Характерна для металлов и сплавов: Na Na Na Na Na Na Na Na Na Na Na Na Na Na Na Na + 0 + 0 + 0 + 0 + 0 + 0 + 0 + 0 e e e e e e e e e
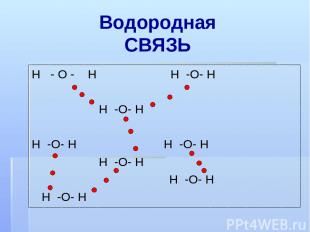
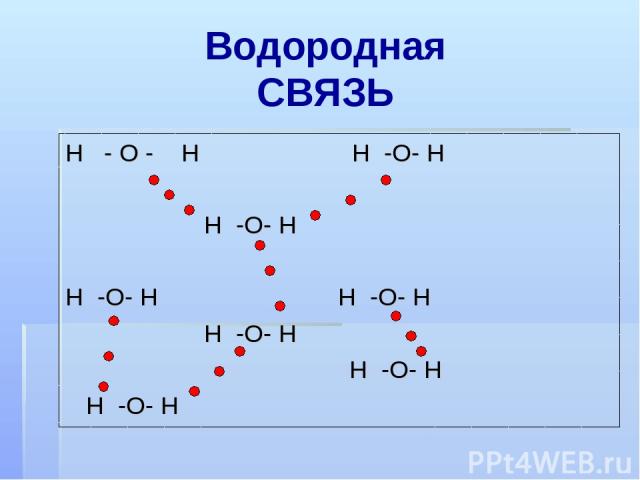
Водородная CВЯЗЬ Н - О - Н Н -О- Н Н -О- Н Н -О- Н Н -О- Н Н -О- Н Н -О- Н Н -О- Н
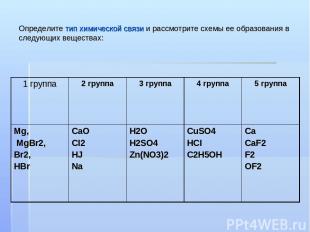
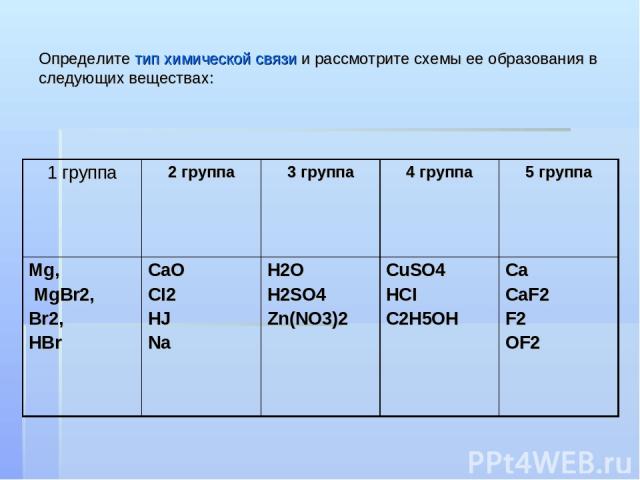
Определите тип химической связи и рассмотрите схемы ее образования в следующих веществах: 1 группа 2 группа 3 группа 4 группа 5 группа Mg, MgBr2, Br2, HBr CaO CI2 HJ Na H2O H2SO4 Zn(NO3)2 CuSO4 HCI C2H5OH Ca CaF2 F2 OF2
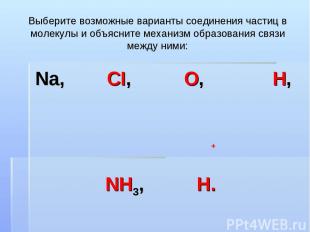
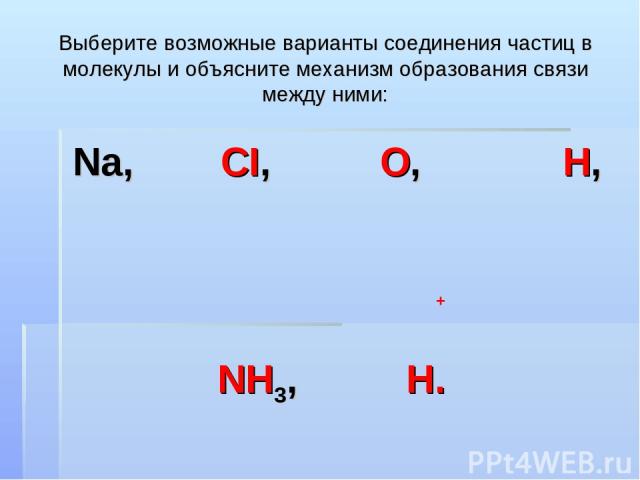
Выберите возможные варианты соединения частиц в молекулы и объясните механизм образования связи между ними: Na, CI, O, H, NH3, H. +

ОКСИДЫ Бинарные соединения, в состав которых входит кислород. Оксиды делятся на оксиды металлов(СuO,FeO,MgO), неметаллов(СО2, SO3) и амфотерные оксиды(АI2O3, ZnO). вещества

Основания Сложные вещества, состоящие из атомов металлов, связанных с одной или несколькими гидроксидными группами. Основания делятся на растворимые-щелочи (NaOH KOH) и нерастворимые в воде(CuOH)2 (AIOH)3. вещества

Кислоты Сложные вещества, состоящие из атомов водорода, связанных с кислотными остатками. Кислоты делятся на кислородсодержащие(НNO3,Н2SO4), бескислородные (НСI,Н2S). вещества

СОЛИ Сложные вещества, состоящие из атомов металлов, связанных с кислотными остатками. Соли делятся на средние(NaCI,СuSO4). кислые (NaHCO3) основные (Cu2(OH)2CO3 вещества

Атом- это химически неделимая частица, состоящая из ядра и вращающихся вокруг него электронов.

Атом это химически неделимая частица, состоящая из ядра и вращающихся вокруг него электронов.

Молекула - мельчайшая, химически делимая частица вещества, сохраняющая его свойства

ПРОСТЫЕ ВЕЩЕСТВА Вещества, состоящие из атомов одного химического элемента. Металлы Водород Кислород Сера Фосфор Углерод

СЛОЖНЫЕ ВЕЩЕСТВА Вещества, состоящие из атомов разных химических элементов. Оксиды Соли Кислоты Основания Органические вещества
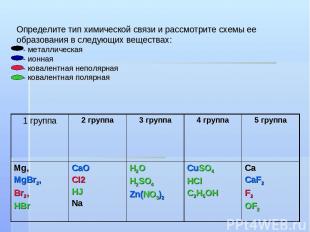
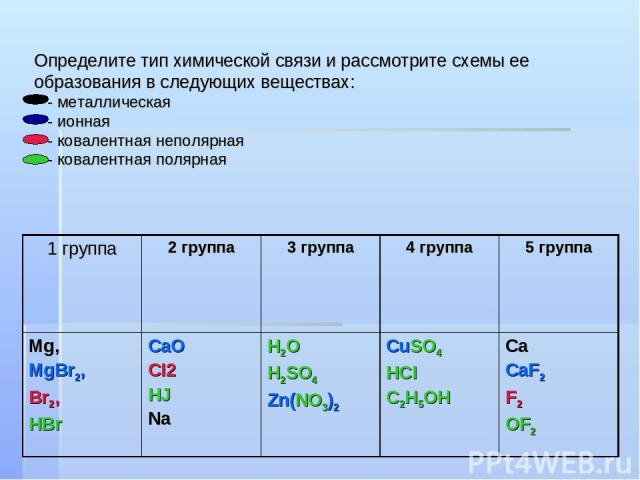
Определите тип химической связи и рассмотрите схемы ее образования в следующих веществах: - металлическая - ионная - ковалентная неполярная - ковалентная полярная 1 группа 2 группа 3 группа 4 группа 5 группа Mg, MgBr2, Br2, HBr CaO CI2 HJ Na H2O H2SO4 Zn(NO3)2 CuSO4 HCI C2H5OH Ca CaF2 F2 OF2