Презентация на тему: Дисперстные системы и растворы

МОУ СОШ №7 презентацияНа тему:Дисперстные системы и растворыВЫПОЛНИЛИ:ПРОВЕРИЛА:Ученицы 11 классаМодина ГалинаЯманова ЕкатеринаШЕВЦОВА Е.А.

Дисперсные системы Дисперсные системы состоят как минимум из двух компонентов:1. дисперсионной среды, которая играет роль растворителя и, следовательно, является непрерывной фазой; 2. дисперсной фазы, играющей роль растворённого вещества.Дисперсными называют гетерогенные системы, в которых одно вещество в виде очень мелких частиц равномерно распределено в объёме другого

Классификация По агрегатному состоянию дисперсионной среды и дисперсной фазы

Дисперсная среда: Дисперсная фаза:Всегда гомогенная смесь (воздух, природный газ)Дисперсная фаза:Туман, попутный газ с капельками нефти, карбюраторная смесь в двигателях автомобилей, аэрозолиДисперсная фаза:Твёрдое вещ-воПыли в воздухе, дымы, смог, пыльные и песчаные бури

Дисперсная среда:Дисперсная фаза:Шипучие напитки, пеныЭмульсии. Жидкие среды организма (плазма крови, лимфа, пищеварительные соки), жидкое содержимое клеток (цитоплазма, кариоплазма)Дисперсная фаза:Твёрдое вещ-воЗоли, гели, пасты (кисели, студни, клеи)Речной и морской ил, взвешенные в воде;Строительные растворы

Дисперсная среда:Снежный наст с пузырьками воздуха в нём, почва, кирпич и керамика, пористый шоколад, порошокДисперсная фаза:Влажная почва, медицинские и косметические средства (мази, тушь, помада и т.д.)Дисперсная фаза:Горные породы, цветные стёкла, некоторые сплавы
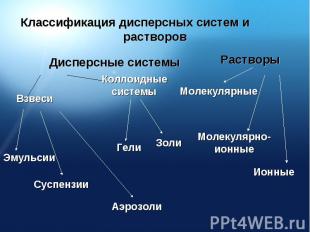
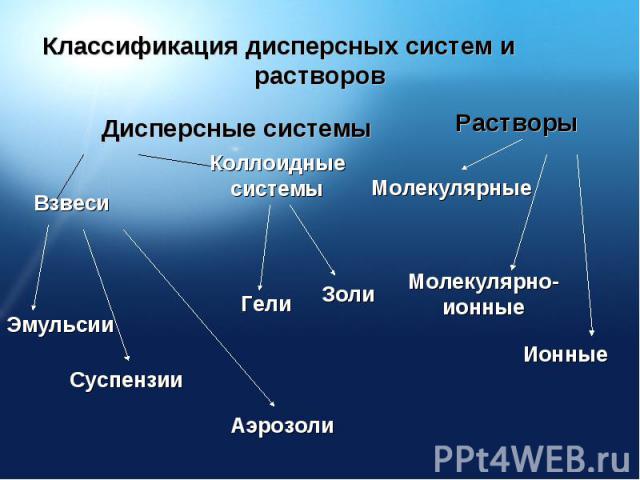
Классификация дисперсных систем и растворов

Дисперсные системы, в которых размер частицыфазы более 100 нм. Такие системы разделяют на:(и среда, и фаза - не растворимые в друг друге жидкости)(среда – жидкость, а фаза – не растворимое в ней вещество)(взвеси в газе мелких частиц жидкостейили твёрдых веществ)

это большинство жидкостей живой клетки (цитоплазма, ядерный сок) и живого организма(кровь, лимфа, тканевая жидкость)Студенистые осадки, образующиеся при коагуляции золейявление слипания коллоидных частиц и выпадения их в осадок

Водные растворы неэлектролитов – органических веществ (спирта, глюкозы, сахарозы)Растворы слабых электролитов (азотистой, сероводородной кислот)Растворы сильных электролитов (щелочей, солей, кислот - NaOH, K2SO4, HNO3, HClO4)

Эффект Тиндаля рассеяние света при прохождении светового пучка через оптически неоднородную среду. Обычно наблюдается в виде светящегося конуса (конус Тиндаля), видимого на тёмном фоне. Характерен для растворов коллоидных систем (например, золей металлов, разбавленных латексов, табачного дыма), в которых частицы и окружающая их среда различаются по преломления показателю. На Т. э. основан ряд оптических методов определения размеров, формы и концентрации коллоидных частиц и макромолекул. Назван по имени открывшего его Дж. Тиндаля. Слева – раствор крахмала, справа - вода

Роль дисперсных систем Для химии наибольшее значение имеют дисперсные системы, в которых средой является вода и жидкие растворы. Природная вода всегда содержит растворённые вещества. Природные водные растворы участвуют в процессах почвообразования и снабжают растения питательными веществами. Сложные процессы жизнедеятельности, происходящие в организмах человека и животных, также протекают в растворах. Многие технологические процессы в химической и других отраслях промышленности, например получение кислот, металлов, бумаги, соды, удобрений протекают в растворах.















![Звук [ ц ]. Буквы Ц, ц](/images/1469/49205/218/img0.jpg)







