Презентация на тему: Углеводы

ТЕМА УРОКА: «УГЛЕВОДЫ»

ПЛАН УРОКА. Состав. Классификация.Нахождение в живых организмах.История открытия.Глюкоза. Состав. Физические свойства.Строение молекулы.Изомер-Фруктоза.Глюкоза. Химические свойства.Применение.Программированный опрос.Сахароза. Состав. Физические свойства.Строение молекулы.Сахароза. Добыча.Сахароза. Химические свойства.Контрольный графический диктант.

СОСТАВ. В бескрайнем мире органи-ческих веществ есть соеди-нения, о которых можно сказать, что они состоят изуглерода и воды, они так иназываются УГЛЕВОДЫ.Поскольку многие из них сладкие на вкус, их ещё называют САХАРА.Углеводы имеют формулу: CX(H2O)Y.В состав молекул входят:-гидроксильная группа ОН--карбонильная группа-С=О или -С=О \Н \
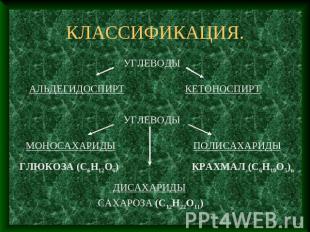
КЛАССИФИКАЦИЯ.

НАХОЖДЕНИЕ В ЖИВЫХ ОРГАНИЗМАХ. В растениях- до 80%сухого вещества В организме человека и животных- до 2%ФОТОСИНТЕЗ:xCO2+yH2O=Cx(H2O)Y+xO2

ИСТОРИЯ ОТКРЫТИЯ. Сахароза была хорошо известна на Древнем Востоке. Её выделяли из сока сахарного тростника, родиной которого является Индия. Оттуда это растение вывезли в Египет и Персию, а затем через Венецию в Европу. Фруктоза была впервые выделена из «медовой воды» в 1792 году русским химиком Т. Е. Ловицем, а глюкоза открыта в 1802 году.

ГЛЮКОЗА. СОСТАВ. ФИЗИЧЕСКИЕ СВОЙСТВА. С6Н12О6 – Виноградный сахарОт греч.GLYKUS-СЛАДКИЙ. ФИЗИЧЕСКИЕ СВОЙСТВА: кристаллическое вещество,без цвета и запаха, хорошо растворимо в воде.СОДЕРЖИТСЯ: в соке винограда, спелых фруктах, в мёде.

СТРОЕНИЕ МОЛЕКУЛЫ. ГЛЮКОЗА- АЛЬДЕГИДОСПИРТ.Альфа-форма –34% Бета-форма –64%Альдегидная форма- 2%Существуют одновременно и могут переходить друг в друга-явление ТАУТОМЕРИИ. Не изомеры.

ИЗОМЕР- ФРУКТОЗА. ФРУКТОЗА или ФРУКТОВЫЙСАХАР содержится в плодах и мёде. Слаще глюкозы. ФРУКТОЗА- КЕТОНОСПИРТ, альфа- и бета- формы представ-ляют собой пятичленные циклы в отличие от молекул глюкозы.КЕТОННАЯ ФОРМА:

ГЛЮКОЗА. ХИМИЧЕСКИЕ СВОЙСТВА. Химические свойства обусловлены наличием карбонильной игидроксильной групп. КАК МНОГОАТОМНЫЙ СПИРТ: А). В реакцию этерификации вступает каждая группа –ОН. Б). С Cu(OH)2 без to даёт соли василькового цвета. Вступает в качественные реакции: в реакцию «серебряного зеркала» и с Сu(OH)2 при to, в результате которых образуется ГЛЮКОНОВАЯ КИСЛОТА. (С5Н11О5)-С=О + Ag2O = (С5Н11О5)-С=О + 2Ag

ОСОБЫЕ СВОЙСТВА. Под действием kat-ферментов происходит:1). СПИРТОВОЕ БРОЖЕНИЕ. С6Н12О6=2С2Н5ОН+2СО2 2). МОЛОЧНОКИСЛОЕ БРОЖЕНИЕ. С6Н12О6=2СН3-СН-С=О 3). ПОЛНОЕ ОКИСЛЕНИЕ В ЖИВЫХ ОРГАНИЗМАХ.С6Н12О6+6О2=6СО2+6Н2О+Q

ПРИМЕНЕНИЕ.

ТЕСТ. 1.Какой из углеводов моносахарид: а).крахмал, б).глюкоза, в).сахароза. 2. Фруктоза-это: а).изомер, б).другое вещество. 3. Сколько форм глюкозы известно: а). 1, б). 2, в). 3, г). 4. 4. Какие f-группы в молекуле глюкозы: а)-с=о и -он, б) -с=о и -с=о, в)-он и с=о 5. С чем прореагирует глюкоза: а). СН4, б). Ag2O, в). С2Н5ОН 6. При спиртовом брожении образуется:а). молочная кислота и СО2 , б).спирт и СО2, в). масляная кислота и СО2

Сахароза. Состав. Физические свойства. С12Н22О11-свекловичный и тростниковый сахар (обычныйсахар). Кристаллическое в-во,без цвета и запаха,Тпл.=185ос, хорошо растворимо в воде, намного слаще глюкозы. Сахароза- многоатомный спирт, но не альдегид. Молекула сахарозы состоит из соединенных друг с другом остатков глюкозы и фруктозы.

САХАРОЗА. ДОБЫЧА. В наши дни две трети производства сахара (более 60 млн. тонн)-это тростниковый сахар, тогда как на долю свекловичного саха-ра приходится 35 млн. тонн. Годовой урожай сахарного трост- ника составляет около 1 млрд. тонн. Разгрузка сахарной свеклы.Уборка сахарного тростника.

Сахароза. Химические свойства. При взаимодействии с серной кислотой легко обугливается и выделяется углекислый газ. 2. Не окисляется Ag2O и Cu(OH)23. Основное свойство - ГИДРОЛИЗ:С12Н22О11+Н2О = С6Н12О6+С6Н12О6

Графический диктант. 1 вариант-глюкоза, 2 вариант- сахароза.Правильное утверждение;Неверное утверждениеВещ-во при обычных условиях кристаллическое, сладкое. 2. Хорошо растворяется в воде. 3. Получают гидролизом природного сырья. 4. Реагирует с аммиачным раствором оксида серебра. 5. Может подвергаться гидролизу. 6. Может образовывать сложные эфиры. 7. Применяется в производстве зеркал. 8. Используется в качестве пищевого продукта. 9. Используется как лекарство. 10. Применяется в хлебопечении. 11. Применяется для производства карамели.