Презентация на тему: Соединения галогенов

Соединения галогенов Опыт и наблюдение - таковы величайшие источники мудрости , доступ к которым открыт для каждого человека. В.Э.Чаннинг Выполнил учитель химииМАОУ Краснопутьской СОШЗюзина Татьяна Сергеевна

Экспресс опрос класса: 1. Какие элементы называются галогенами? 2. Охарактеризуйте положение галогенов в Периодической системе Д.И.Менделеева. 3. Каково строение атомов галогенов? 4. Какой из галогенов является самым электроотрицательным? 5. Как изменяются окислительные свойства галогенов с увеличением порядкового номера?

Галогеноводороды: HF - фтороводородная кислота ( плавиковая) HCl - хлороводородная кислота (соляная) HBr - бромоводородная кислота HI - йодоводородная кислота

Почему сила кислотыHJ>HF ? Радиус атома J>F

Лабораторная работа по теме:
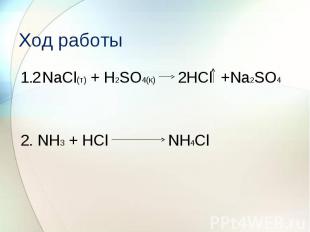
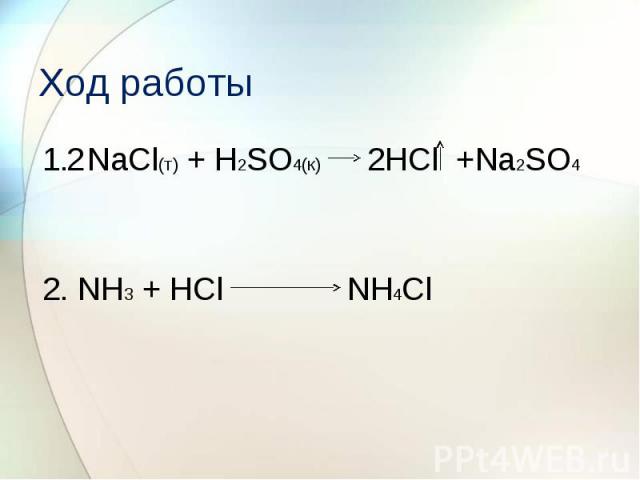
Ход работы 1. NaCl(т) + H2SO4(к) 2HCl +Na2SO4 2. NH3 + HCl
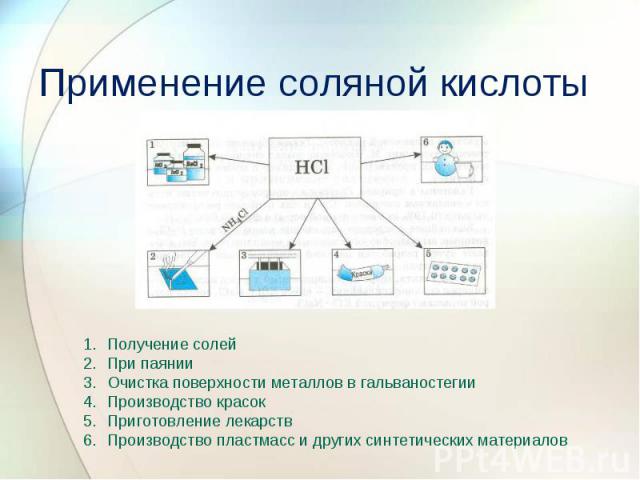
Применение соляной кислоты Получение солейПри паянииОчистка поверхности металлов в гальваностегииПроизводство красокПриготовление лекарствПроизводство пластмасс и других синтетических материалов

Соли: F фторидыCL хлориды хлорид натрия(галит) Br бромиды бромид серебраJ йодиды йодид калия

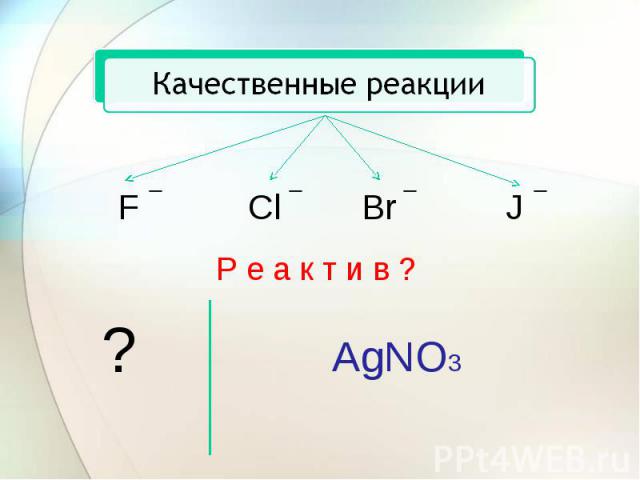
Качественные реакции

Качественные реакции NaCl + AgNO3 =NaBr + AgNO3 =NaJ + AgNO3 = AgCl + NaNO3белый AgBr + NaNO3светло-желтыйAgJ + NaNO3желтый

ХФУ1970 г.Аэрозольные распылителиОхлаждающиеВещества(хладагены) CI + O3 = CIO + O2Один атом хлора уничтожает 100000 молекул O3 и может существовать до 300 лет. Слепота из-за катарактыРаковые заболевания кожиПодавление иммунной системы организма

Тест по теме: «Галогены и их соединения».

Ответы на вопросы теста: