Презентация на тему: Брэнды и дженерики

Брэнды и дженерики Потапов Александр Петровичврач-кардиолог, к.м.н.

Зачем фармацевту информация об особенностях дженериков? Исключение претензий со стороны потребителей после приобретения ими в аптеке «кота в мешке»Повышение уровня продаж оригинальных препаратов – увеличение прибыли предприятияПредотвращение ситуаций сообщения пациентам неполной или недостоверной информации о препарате

Особенности национальной любви к дженерикам Недостаточная осведомленность населения в области фармакологии и фармакотерапииНизкий уровень разъяснительной работы среди населения в области лекарственной безопасностиНизкая покупательная способность пациентовБолее доступная ценаВозможная сопоставимая терапевтическая эффективность (все-таки они помогают)Коммерческая эффективность
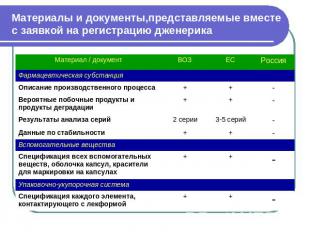
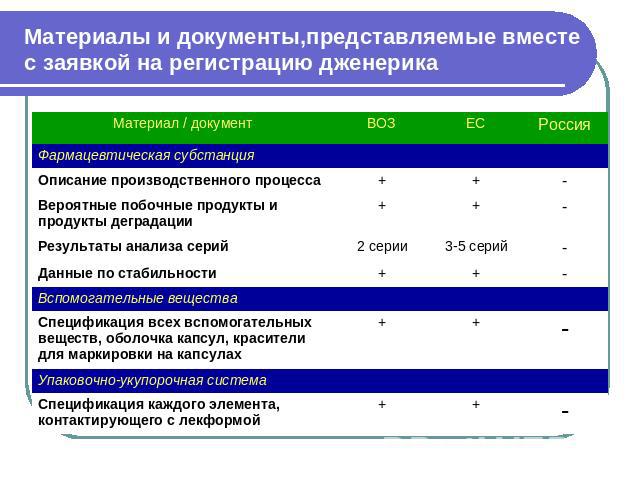
Материалы и документы,представляемые вместес заявкой на регистрацию дженерика

«Засилие» дженериков В Российской Федерации зарегистрировано более 17 000 наименований лекарственных препаратов 78% из них являются «аналогами» оригинальных препаратов

Примеры сравнения брэндов и дженериков Амлодипин и норваскАмиодарон и кордаронРенитек и энамКозаар и лозапКонкор и бисогаммаДиротон и лизиноприлВерапамил и изоптинКоринфар и адалатСедуксен и реланиумЭгилок, беталок ЗОК и метопролол

Оригинальный препарат Original (англ.) – первый, новый, истинный, прежде неизвестный, предшествующий, исходный…Новый препарат, произведенный на основе разработки новых активных субстанцийПатент и эксклюзивные права 20 лет принадлежат компании-создателю Регистрируется на основании доказательных данных многоцентровых рандомизированных исследования

Дженерик Generic (англ.) – общий, родовой, групповойДженерик (иногда — генерик, женерик) —лекарственное средство, которое выпускается без лицензии компании-разработчика инновационного лекарственного средства, и размещается на рынке после окончания срока действия патента или других исключительных правВсе воспроизведения оригинального препарата, непатентованные копии Регистрируются на основании «биоэквивалентности*»В России в большинстве случаев патентное право защищает не молекулу, а процессСостав таблетки НЕ идентичен оригиналу

Критерии сравнения Дженерик содержит то же активное лекарственное вещество (субстанцию), что и оригинальный (патентованный) препарат.Дженерик отличается от оригинального препарата вспомогательными (?) веществами (неактивными ингредиентами, наполнителями, консервантами, красителями и др.).Различия наблюдаются и в самом технологическом процессе производства дженериков.Соблюдение технологии производства и контроль качества выпускаемой продукции у брендов всегда на более высоком уровне

Эквивалентность брэндов и дженериков (требования FDA) Фармацевтически эквивалентные лекарственные препараты содержат одинаковые активные ингредиенты в одинаковой лекарственной форме, предназначены для одного способа введения и идентичны по силе действия или концентрации активных веществ (FDA, Electronic Orange Book. Approved Drug Products with Therapeutic Equivalence Evaluations, 20th Edition, 2000). Биоэквивалентные лекарственные препараты — это фармацевтически эквивалентные или фармацевтически альтернативные препараты, которые имеют сравнимую биодоступностъ при исследовании в сходных экспериментальных условиях (FDA, Electronic Orange Book, Approved Drug Products with Therapeutic Equivalence Evaluations, 20th Edition, 2000). Эквивалентность препаратов оценивается также по уровню требований к контролю качества производства (соответствие стандартам GMP), к инструкциями к лекарствам, к этикетированию и т.д.Эквивалентность лекарств оценивается также по физико-химическим свойствам действующих веществ (степень дисперсности, полиморфизм и др.), свойствам вспомогательных веществ, особенностям технологического процесса, условиям хранения, упаковке (стекло, пластмасса, бумага и т.п.). Терапевтически эквивалентными лекарственные препараты могут считаться только в том случае, если они фармацевтически эквивалентны и можно ожидать, что они будут иметь одинаковый клинический эффект и одинаковый профиль безопасности при использовании пациентами в соответствии с указаниями на этикетке (FDA, Electronic Orange Book. Approved Drug Products with Therapeutic Equivalence Evaluations, 20th Edition, 2000).

Фармацевтическая эквивалентность Фармацевтически эквивалентные лекарственные препараты содержат одинаковые активные ингредиенты в одинаковой лекарственной форме, предназначены для одного способа введения и идентичны по силе действия или концентрации активных веществ (FDA, Electronic Orange Book. Approved Drug Products with Therapeutic Equivalence Evaluations, 20th Edition, 2000).Стоимость субстанции (действующего вещества) составляет 50% себестоимости лекарственного средстваДженериковые компании постоянно совершенствуют способы снижения стоимости вспомогательных веществВспомогательные вещества могут на 50% изменять терапевтическую эффективность и биодоступность фармацевтического средстваВыявление многих токсических примесей возможно только благодаря специальному химическому анализу, не предусмотренному в фармакопейных статьях РФ
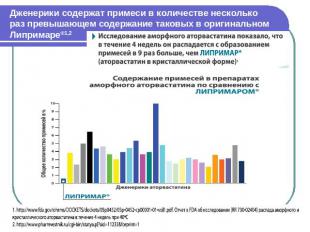
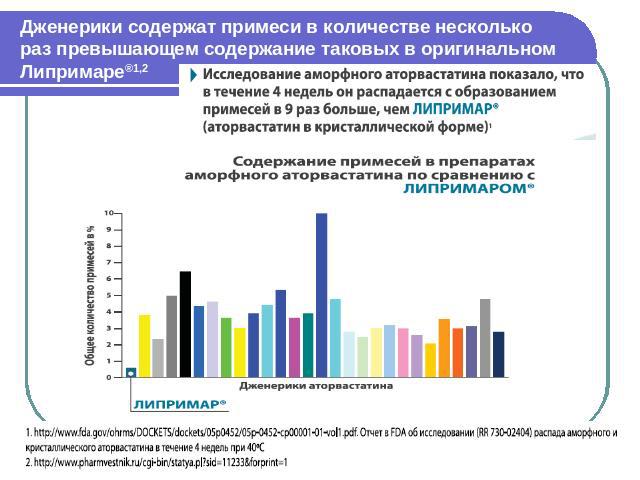
Дженерики содержат примеси в количестве несколько раз превышающем содержание таковых в оригинальном Липримаре®1,2

Electronic Orange Book – результаты поиска Периндаприл (Perindapril)– не зарегистрированАторвастатин – кодуэт, липитор (PFIZER)Квинаприл – квинаретик (ACTAVIS); квинаприл (AUROBINDO, MYLAN, GENPHARM, INVAGEN, LUPIN, RANBAXY, SANDOZ, TEVA, TORPHARM, WATSON LABS FLORIDA); аккуретик*, аккуприл* (PFIZER)Амлодипин – норваск* (PFIZER) + 22 фирмы (в т.ч. DR REDDYS LABS LTD и GEDEON RICHTER USA)Ренитек – нет (в т.ч. и поиск по эналаприлам)Лизиноприл – 42 фирмыБисопролол – 7 фирмЛозартан – козаар*, гизаар* (MERCK)Симвастатин – зокор 80* (MERCK), симвастатин (15 фирм)Триметазидин (Trimetazidine) – нет регистрации Клонидин (клофелин) – 11 фирм

Рекомендации ВОЗ в отношении биоэквивалентности Биоэквивалентность дженерика следует определять по отношению к оригинальному лекарственному препарату. Если он не представлен на национальном рынке, то его берут из указанного в перечне (первичный рынок), где, по мнению компании-производителя, он более всего отвечает требованиям, предъявляемым к качеству, безопасности, эффективности и маркировке.При невозможности использования оригинального лекарственного препарата стандартом может служить лекарственный препарат, лидирующий на рынке страны, если подтверждены его качество, безопасность и эффективность.При отсутствии препарата-лидера регистрируемый дженерик производят в соответствии с местными, государственными или региональными стандартами, в том числе Международной фармакопеей и Руководством ВОЗ по регистрационным требованиям для определения взаимозаменяемости лекарственных препаратов, выпускаемых несколькими производителями (WorldHealth Organization, 1996, WHO Expert Expert Committee on Specifications for Pharmaceutical Preparations: thirty-fourth report. WHO Technical Report Series No. 863, Geneva, pp. 114-154).

Терапевтическая эквивалентность Терапевтически эквивалентными лекарственные препараты могут считаться только в том случае, если они фармацевтически эквивалентны и можно ожидать, что они будут иметь одинаковый клинический эффект и одинаковый профиль безопасности при использовании пациентами в соответствии с указаниями на этикетке (FDA, Electronic Orange Book. Approved Drug Products with Therapeutic Equivalence Evaluations, 20th Edition, 2000). В отличие от биоэквивалентности, определение которой регламентируется жесткими стандартами и не вызывает, как правило, неоднозначностей в трактовке результатов, отсутствие четких определений терапевтической эквивалентности приводит к неуверенности как врачей, так и пациентов в правильности выбора тех или иных препаратов генерического ряда.В опубликованном в 1998 году FDA проекте правил оценки терапевтической эквивалентности дженериков предлагается указывать на этикетке препарата наличие или отсутствие терапевтической эквивалентности, а также препарат, с которым производилось сравнение (как правило, это оригинальный препарат).

Мнение специалиста Марцевич Сергей Юрьевич Профессор, доктор медицинских наук.Профессор кафедры доказательной медицины ФДПОП ММА им М.И. Сеченова. Председатель секции рациональной фармакотерапии ВНОК,член-корреспондент Российской академии естественных наук «…все крупные исследования, оценивающие влияние препарата на прогноз жизни и заболевания, в огромном большинстве используют только оригинальные лекарственные препараты…» «Знакомство с данными … исследований по сравнению клинической эффективности оригинальных препаратов и дженериков показывает, что в их действии могут наблюдаться весьма существенные отличия…»
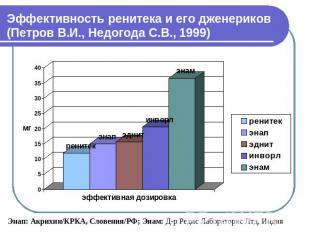
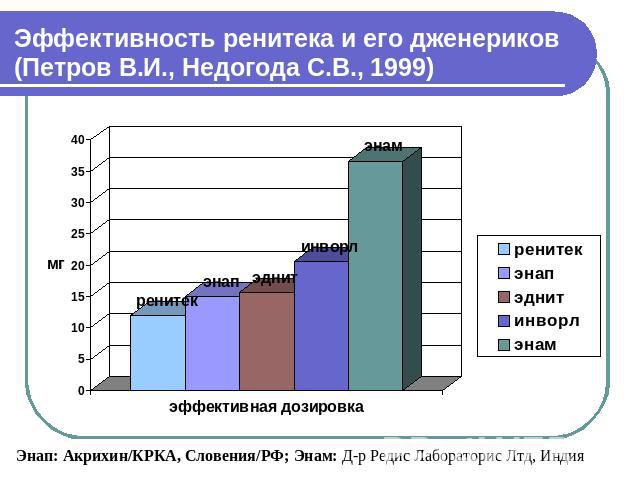
Эффективность ренитека и его дженериков (Петров В.И., Недогода С.В., 1999) Энап: Акрихин/КРКА, Словения/РФ; Энам: Д-р Редис Лабораторис Лтд, Индия

Дженерики: преимущества и недостатки Таблиц взаимозаменяемости дженерических препаратов в РФ не существует. В Интернете можно воспользоваться таблицами из базы FDA (Electronic Orange Book FDA).Дженерики не хуже и не лучше оригинальных ЛС, они - иные ЛС. Пример: дженерики аторвастатина - аторвастатин в аморфной форме распад в течение 7 недель в 10 раз быстрее оригинального препарата содержат примеси от 2 до 10% (оригинальный препарат менее 1%).

Оранжевая книга FDA Electronic Orange BookApproved Drug ProductswithTherapeutic Equivalence EvaluationsCurrent through December 2008**** In order to provide timely consumer information on generic drugs, the Electronic Orange Book is updated daily as new generic approvals occur.Refer to FAQ for additional information.U.S. Department of Health and Human ServicesFood and Drug AdministrationCenter for Drug Evaluation and ResearchOffice of Pharmaceutical ScienceOffice of Generic Drugs

Сравнение терапевтической эффективности липримара и его дженериков Эффективная дозировка – от 20 мг/сутСкорость наступления клинических эффектов – 25-40 дней постоянного приемаКлинические эффекты:Урежение приступов загрудинных болей, повышение порога переносимых физических нагрузокСнижение среднесуточного АДУменьшение и полное исчезновение аритмийНа фоне применения аториса, атомакса и торвакарда подобных клинических эффектов не зарегистрировано

Результаты исследования FDA 1996 г. при принятии врачом решения о переводе пациента с оригинального препарата на генерический у 2/3 больных возникали проблемы, средний показатель при других видах замен ЛС (с дженерика на оригинальный, с дженерика на дженерик) составил 10%.

Мнение Association of American Physicians (основана в 1885 г.) Американская ассоциация врачей не рекомендует в качестве замены отпускать лекарственный препарат, которому FDA присвоило код «В» (в США к категории препаратов с кодом «В» FDA относит лекарственные средства, которые по разным причинам в данный момент нельзя считать терапевтически эквивалентными соответствующим препаратам сравнения) (Drug evaluations annual, American Medical Association, 1999, p. 7). Любой врач в США может легко узнать код нужного ему рецептурного лекарственного препарата, заглянув в ежегодно переиздаваемую «Оранжевую книгу», доступную и в сети Интернет. В руководстве ВОЗ по регистрационным требованиям, предъявляемым для определения взаимозаменяемости генерических лекарственных препаратов, также указывается, что «невозможность гарантировать взаимозаменяемость (лекарственных препаратов) может нанести вред здоровью и безопасности пациентов» (WHO Technical Report Series, No. 863, 1996).

Особенности отечественного амлодипина Компания «Pfizer» не передавала лицензию на производство и распространение «Норваска»Действие глобального патента на Норваск завершилось лишь в 2008 году!Существующие на российском рынке другие амлодипины («дженерики») были выпущены до завершения действия глобального патента

Особенности дженериков аторвастатина Компания «Pfizer» не передавала лицензию на производство и распространение «Липримара»Глобальный патент на «Липримар» действует до 2011 годаВсе другие аторвастатины («дженерики») являются непатентованными копиями

Что общего между ЛИПРИМАРОМ® и его дженериками? Что общего между алмазом и углем?

Почему все-таки Оригинальный препарат? Оригинальный препарат:Стабильность физико-химических свойств действующего веществаВысококачественные наполнители и оболочкаДоказательства высокой эффективности и безопасностиКопия (дженерик):Наличие токсических веществ, продуктов деградации и распадаМеньший срок годностиИзмененные показатели биодоступностиВысокий риск токсических и аллергических реакцийРиск неожиданных межлекарственных взаимодействийОтсутствие доказательств эффективности и безопасности

Спасибо за внимание

Е.М. Тареев Академик Академии медицинских наук СССР (1948), Герой Социалистического Труда (1965), лауреат Сталинской (1946), Ленинской (1974), и Государственной премий СССР (1983), заслуженный деятель науки РСФСР(1948). Один из основоположников советской нефрологии, гепатологии, ревматологиии паразитологии. «Для того, чтобы в наш век лечиться, нужно иметь хорошее здоровье!»

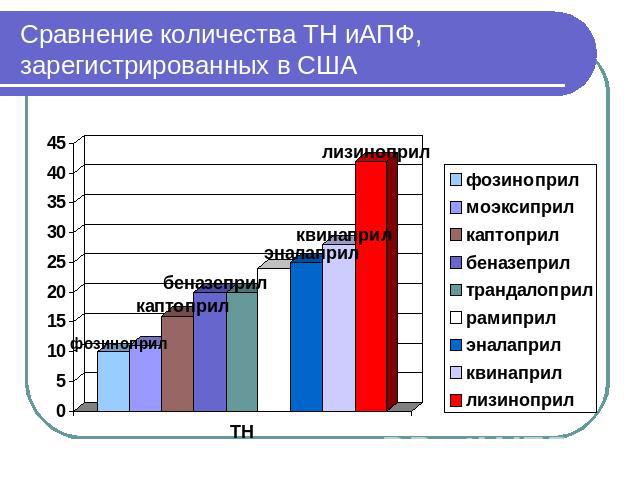
иАПФ, зарегистрированные в США (результаты поиска в Electronic Orange Book по “…pril” Беназеприл - 20Каптоприл - 16Эналаприл - 25Фозиноприл - 10Лизиноприл – 42Моэксиприл - 11Квинаприл - 28Рамиприл – 24Трандалоприл - 20Периндаприл (PERINDAPRIL)– нетЦилазаприл (CILAZAPRIL) - нетСпираприл (SPIRAPRIL) - нетЗофеноприл (ZOFENOPRIL) - нет

Сравнение количества ТН иАПФ, зарегистрированных в США

Маркировка лекарственных средств по системе FDA A Drug products that FDA considers to be therapeutically equivalent to other pharmaceutically equivalent products, i.e., drug products for which:(1) there are no known or suspected bioequivalence problems. These are designated AA, AN, AO, AP, or AT, depending on the dosage form; or(2) actual or potential bioequivalence problems have been resolved with adequate in vivo and/or in vitro evidence supporting bioequivalence. These are designated AB.B Drug products that FDA at this time, considers NOT to be therapeutically equivalent to other pharmaceutically equivalent products, i.e.,drug products for which actual or potential bioequivalence problems have not been resolved by adequate evidence of bioequivalence. Often the problem is with specific dosage forms rather than with the active ingredients. These are designated BC, BD, BE, BN, BP, BR, BS, BT, BX, or B*.AA Products in conventional dosage forms not presenting bioequivalence problemsProducts coded as AA contain active ingredients and dosage forms that are not regarded as presenting either actual or potential bioequivalence problems or drug quality or standards issues. However, all oral dosage forms must, nonetheless, meet an appropriate in vitro bioequivalence standard that is acceptable to the Agency in order to be approved.Код «А» - препарат с подтвержденной терапевтической эквивалентностью (сведения о прблемах биоэквивалентности препарата отсутствуют)Код «АВ» - то же, что и код «А», но сведения о прблемах биоэквивалентности имели место (но были опровергнуты дополнительными исследованиями)Код «В» - терапевтическая эквивалентность препарата не подтверждена