Презентация на тему: Sulfur

Сера Sulfur

Историческая справка Сера известна человечеству с древних времен, т. к. она в природе встречается в самородном виде. Считалось, что голубое пламя и запах, распространяемый при горении серы, отгоняет демонов.

Сернистый газ использовали для отбеливания тканей. При раскопках Помпеи нашли картину, на которой изображен противень с серой и приспособление для подвешивания над ним материи.

Кроме того, серу и ее соединения использовали для приготовления косметических средств и для лечения кожных заболеваний..

Ее применяли для военных целей. Так в 670 г защитники Константинополя сожгли арабский флот с помощью смеси селитры, угля и серы (“греческий огонь”). Сера также входит в состав черного пороха


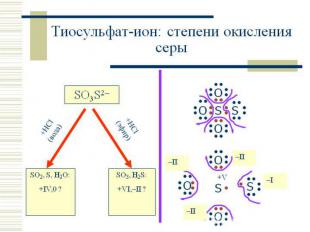
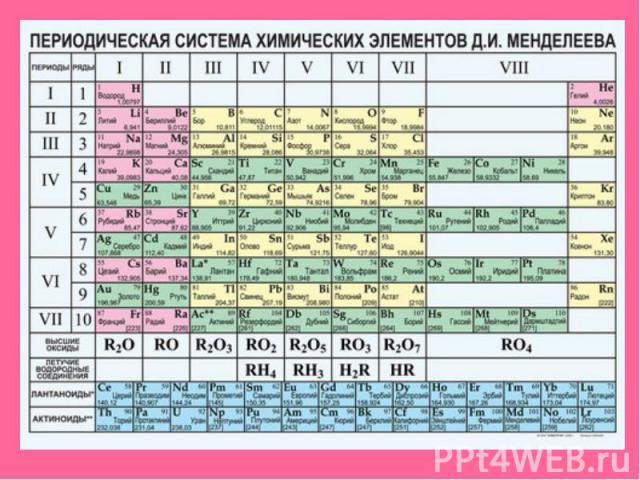
Характеристика серы по ПСХЭ +16Sа) находится в Vl группе, главной подгруппеб) lll период. 3 рядв) неметаллг) проявляет степени окисления -2, 0,+2,+4,+6д) образует кислотные оксиды SO2 (сернистый газ) и SO3 (серный газ)е) этим оксидам соответствуют кислоты H2SO3(сернистая) и H2SO4(серная)ё) с водородом образует летучее водородное соединение H2S
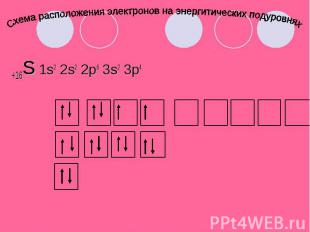
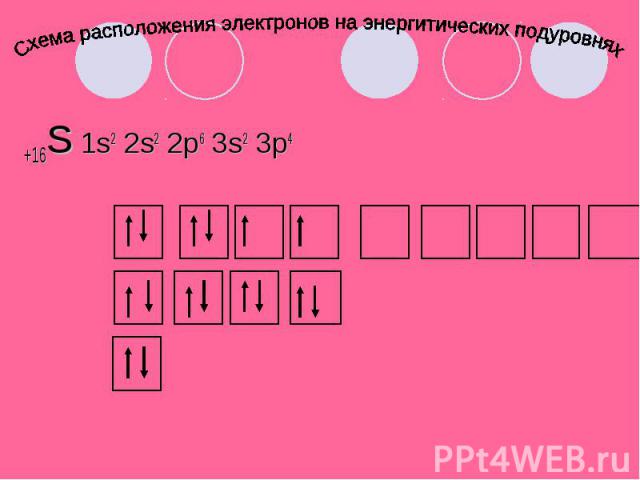
Схема расположения электронов на энергитических подуровнях +16S 1s2 2s2 2p6 3s2 3p4

Строение молекулы серы S8-молекула серы состоит из 8-и атомовсвязь в молекуле - ковалентная неполярнаямолекула неполярнаякристаллическая решётка - молекулярная неполярная
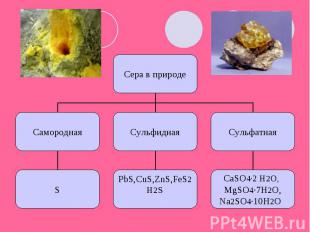

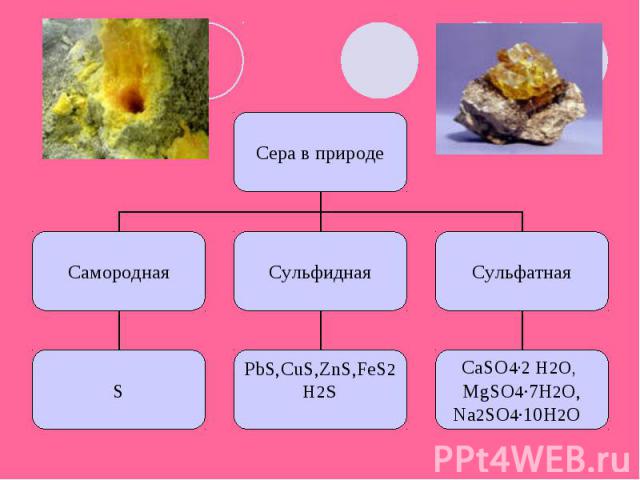
Получение а) Самородную серу очищают от примесей песка и глины. Для этого ее расплавляют перегретым водяным паром, в результате жидкая сера легко отделяется от твердых примесей. При затвердевании получается комовая сера, дальнейшую очистку которой проводят перегонкой.б) Из сульфидов t FeS2 =>FeS +S в) Из сероводорода - неполным окислением H2S+O2 =>S+H2O
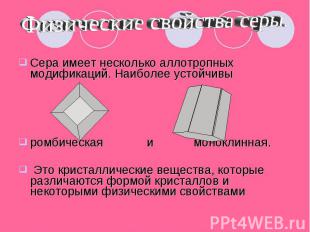
Физические свойства серы. Сера имеет несколько аллотропных модификаций. Наиболее устойчивы ромбическая и моноклинная. Это кристаллические вещества, которые различаются формой кристаллов и некоторыми физическими свойствами

Кристаллы состоят из молекул S8( кр. решетка молекулярная –неполярная) ромбическая сера имеет цвет лимонно-желтый, tпл.=112,8C, моноклинная сера имеет цвет темно-желтый tпл.=119.3C,

При быстром охлаждении расплавлено серый образуется ещё одна неустойчивая аллотропная модификация- пластическая сера Sn , которая легко растягивается подобно резине. S S S S S ..S S S S S S…В воде сера практически нерастворима. Хорошим растворителем для неё является сероуглерод, толуол и некоторые другие вещества.


Применение серы Большая часть серы используется для производства серной кислоты. Значительное количество серы расходуется для вулканизации каучука (она повышает его прочность и эластичность). При введении в каучук большого количества серы получают твердый продукт - эбонит, являющийся электроизоляционным материалом. Сера применяется для борьбы с вредителями сельского хозяйства, для изготовления черного пороха, а также в медицине для изготовления мазей против кожных заболеваний.

Физические свойства Твердое кристаллическое вещество желтого цвета, нерастворима в воде, водой не смачивается (плавает на поверхности), t°кип = 445°С

Химические свойства Сера реагирует со щелочными металлами без нагревания: 2Na + S ® Na2S c остальными металлами (кроме Au, Pt) - при повышенной t°: 2Al + 3S –t°® Al2S3Zn + S –t°® ZnS С некоторыми неметаллами сера образует бинарные соединения: H2 + S ® H2S2P + 3S ® P2S3C + 2S ® CS2

Восстановительные свойства сера проявляет в реакциях с сильными окислителями: c кислородом:S + O2 –t°® S+4O22S + 3O2 –t°;pt® 2S+6O3 c галогенами (кроме йода):S + Cl2 ® S+2Cl2 c кислотами - окислителями:S + 2H2SO4(конц) ® 3S+4O2 + 2H2OS + 6HNO3(конц) ® H2S+6O4 + 6NO2 + 2H2O