Презентация на тему: Производство серной кислотыH2SO4

Производство серной кислоты H2SO4 « Едва найдется другое, искусственно добываемое вещество, столь часто применяемое в технике, как серная кислота…» (Д. И. Менделеев)

Серная кислота H2SO4 cуществует в природе как самостоятельное химическое соединение, представляет собой бесцветную маслянистую жидкость без запаха плотностью 1,83 г/см3 Пагубно действует на растительные и животные ткани, отнимая от них воду, вследствие чего они обугливаются С водой смешивается во всех соотношениях, причём при разбавлении соединения водой происходит сильное разогревание, сопровождающееся разбрызгивание жидкости. Разбавляем по правилу: «Химик! Запомни как оду! Лей кислоту в воду!!!» Одна из самых сильных кислот. В водных растворах практически полностью диссоциирует на ионы: H2SO4 = 2 Н+ + SO42- Раствор оксида серы (+6) SO3 в серной кислоте называется олеумом H2SO4●SO3

История развития производства VIII век – арабский алхимик Аджабир ибн Хайян получил «кислые газы» из «зеленого камня» (железного купороса). IX век – персидский алхимик Ар-Рази получал прокаливанием смеси медного и железного купороса XIII век – европейский алхимик Альберт Магнус усовершенствовал способ. XV век – алхимики 300 лет получали серную кислоту из пирита FeS2 В середине XVIII столетия было обнаружено, что свинец не растворяется в серной кислоте, поэтому стеклянное оборудование заменили на металлическое 1740-46 г.г. – был построен первый сернокислотный завод в Англии с использованием свинцовых камер. 1926 г. – в СССР построена первая башенная установка на Полевском металлургическом заводе (Урал) - малоэффективна. 1903 г. – запуск первой в России контактной установки на Тентелеевском химическом заводе (Петербург), к 1913 г. работало 6 систем (производство до 5 тыс.т.). Далее контактная система получила распространение во всём мире (Германия, Англия, США…)

Исходное сырье Сырьё – исходный материал для производства промышленных продуктов. В мире 75% получают из серы. В России 60% получают из серы. В Японии 60% из отходящих газов.
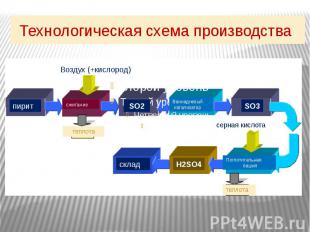
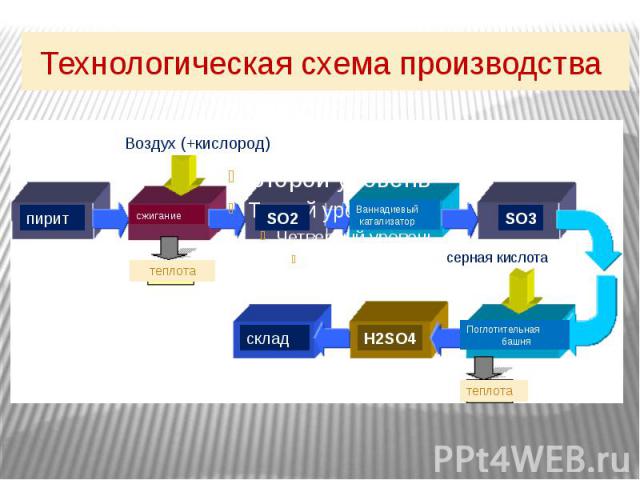
Технологическая схема производства

Технология – наука о наиболее экологичных способах и процессах получения сырья, полупродуктов и продуктов. I стадия Обжиг сырья (пирита) и получение оксида серы SO2. 4FeS2+11O2=2Fe2O3+8SO2 + Q (минерал пирит.) Характеристика реакции: экзотермическая, необратимая, окислительно-восстановительная.
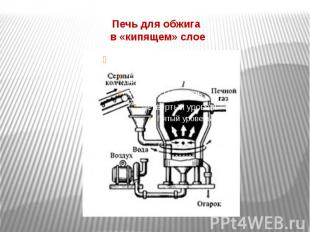
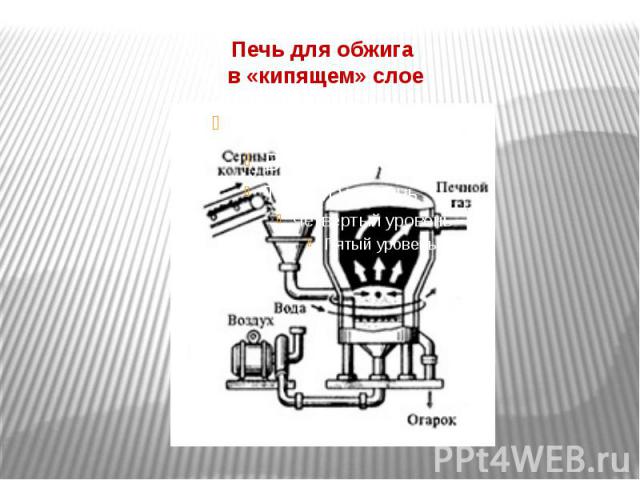
Печь для обжига в «кипящем» слое

Оптимальные условия I стадии Воздух, обогащенный кислородом. t=8000 , теплота экзотермической реакции отводиться. «Кипящий» слой (увеличение площади соприкосновения). Время обжига - несколько секунд.

Принципы производства I стадии (печь для обжига с «кипящим» слоем) 1. «Кипящий» слой. 2. Большая мощность. 3. Механизация и автоматизация. 4. Непрерывность. 5. Принцип противотока.

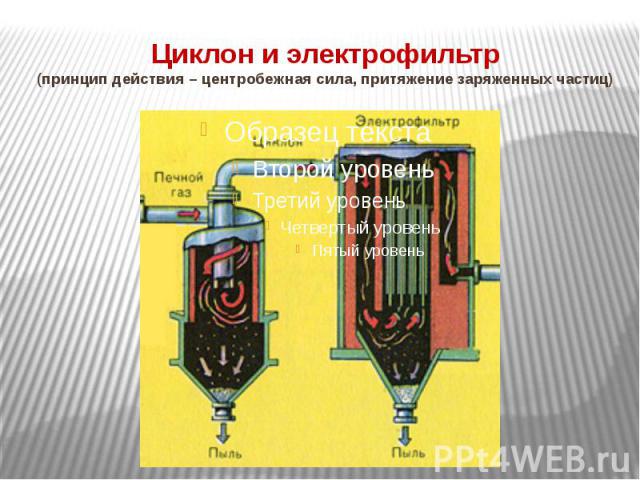
Подготовка сырья для II стадии (циклон, электрофильтр, сушильная башня) Прежде чем приступить ко II стадии SO2 очищают от пыли: 1. “Циклон” – от крупных частиц пыли. 2. Электрофильтр – от мелких частиц пыли Осушить в сушильной башне Нагреть до t=4000 в теплообменнике
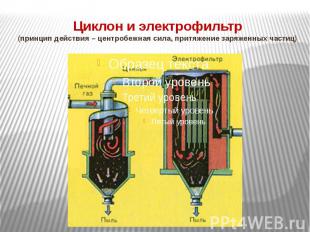
Циклон и электрофильтр (принцип действия – центробежная сила, притяжение заряженных частиц)

Сушильная башня (принцип действия – поглощение воды концентрированной серной кислотой)

Принципы II стадии (контактный аппарат) 2 SO2 + O2 ↔ 2 SO3 + Q (обратимая, каталитическая, экзотермическая) 1. Понижают температуру от 6000С до 4000С. 2. Катализатор V2O5 на керамике. 3. Противоточное движение. 4. Теплообмен. Выход продукта 99,2%

Контактный аппарат

III Стадия (поглотительная башня) SO3+H2O=H2SO4+Q (до 3000C) Увеличивают площадь соприкосновения (керамические кольца Рашига) Отводят продукты реакции Орошают 98% серной кислотой, образуется олеум(раствор SO3 в H2SO4)

Поглотительная башня

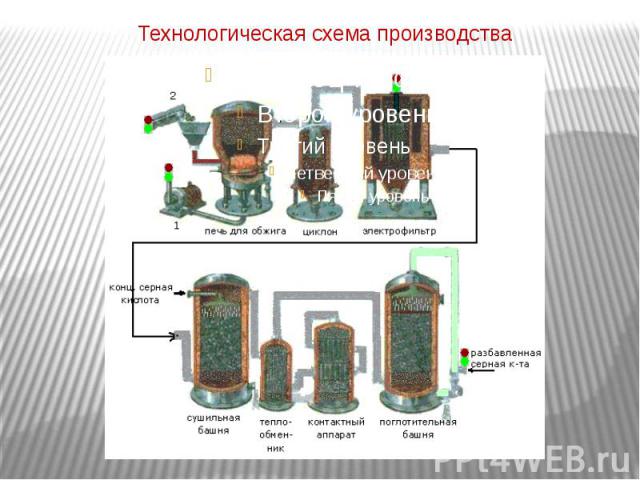
Технологическая схема производства

Транспортировка и хранение серной кислоты Транспортируют в железнодорожных и автоцистернах из кислотостойкой стали Хранят в герметически закрытых емкостях из полимера или нержавеющей стали, покрытой кислотоупорной плёнкой
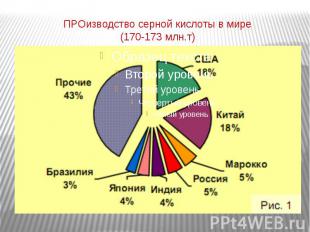
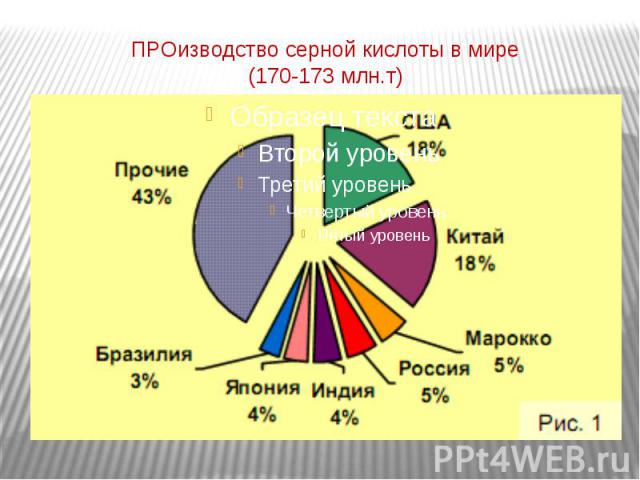
ПРОизводство серной кислоты в мире (170-173 млн.т)
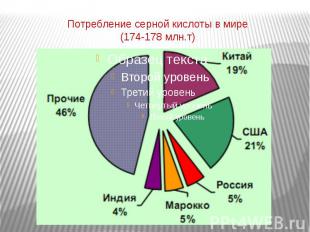
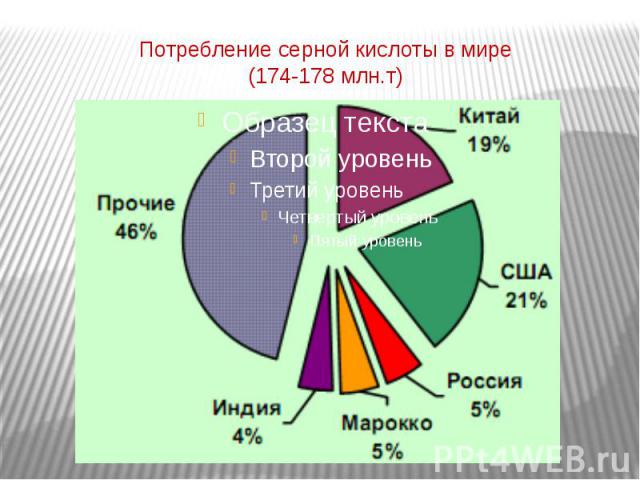
Потребление серной кислоты в мире (174-178 млн.т)

потребление серной кислоты 1. Производство минеральных удобрений. 2. Производство сульфатов (солей серной кислоты). 3. Производство синтетических волокон. 4. Черная и цветная металлургия. 5. Производство органических красителей. 6. Спирты, кислоты, эфиры(орг. вещества). 7. Пищевая промышленность(патока, глюкоза), эмульгатор (загуститель) Е513. 8. Нефтехимия(минеральные масла). 9. Производство взрывчатых веществ.

Структура потребления серной кислоты в России

Экологический ущерб производства При аварийных выбросах в атмосферу попадают соединения серы: SO2;SO3; H2S; H2SO4; Fe2O3(пыль) Последствия: «закисление» почв и водоёмов, «металлизация» атмосферы РЕШЕНИЕ ЭКОЛОГИЧЕСКИХ ПРОБЛЕМ: Непрерывность технологического процесса; Комплексное использование сырья; Совершенствование технологического оборудования.