Презентация на тему: Презентация к уроку химии "Аминокислоты, белки"

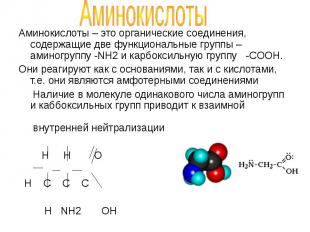
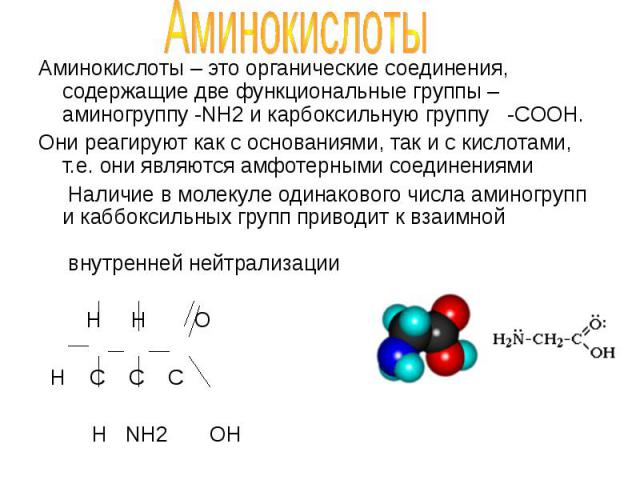
Аминокислоты – это органические соединения, содержащие две функциональные группы – аминогруппу -NH2 и карбоксильную группу -COOH. Аминокислоты – это органические соединения, содержащие две функциональные группы – аминогруппу -NH2 и карбоксильную группу -COOH. Они реагируют как с основаниями, так и с кислотами, т.е. они являются амфотерными соединениями Наличие в молекуле одинакового числа аминогрупп и каббоксильных групп приводит к взаимной внутренней нейтрализации H H O H C C C H NH2 OH

Аминокислоты – бесцветные кристаллические вещества, хорошо растворимые в воде. Многие из них обладают сладким вкусом. Аминокислоты – бесцветные кристаллические вещества, хорошо растворимые в воде. Многие из них обладают сладким вкусом. Реагируют со спиртами, образуя сложные эфиры.

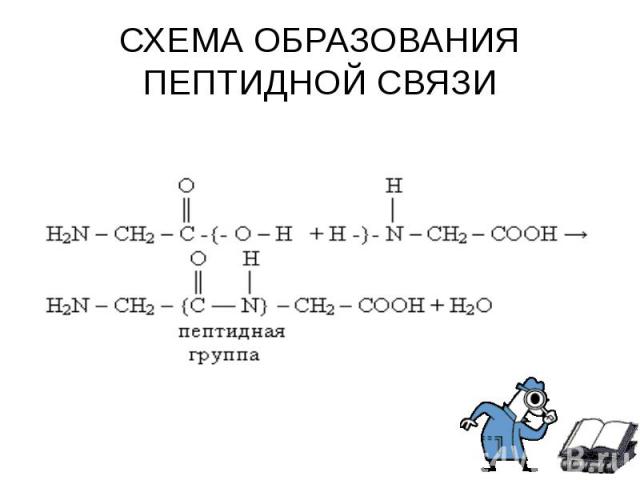
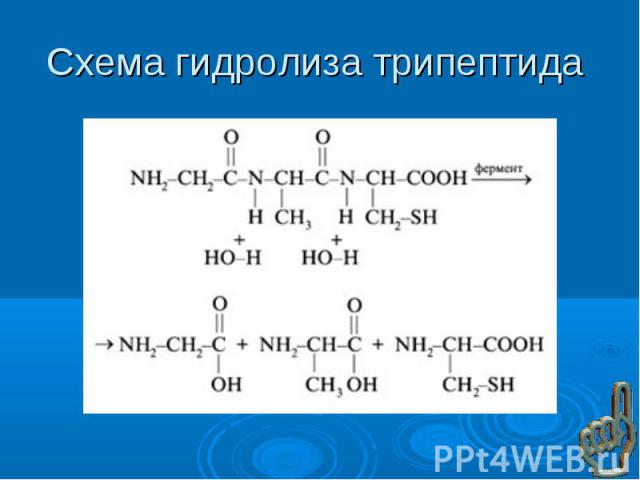
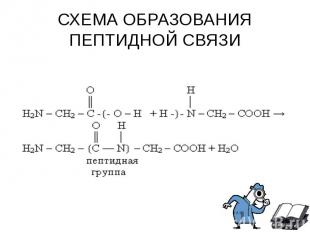
Аминокислоты могут реагировать друг с другом: карбоксильная группа одной аминокислоты реагирует с аминогруппой другой аминокислоты с образованием пептидной связи и молекулы воды. Аминокислоты могут реагировать друг с другом: карбоксильная группа одной аминокислоты реагирует с аминогруппой другой аминокислоты с образованием пептидной связи и молекулы воды. NH2 – CH2 – COOH + NH2 – CH2 – COOH = NH2 – CH2 – CO – NH – CH2 – COOH + H2O Связь – CO – NH – , соединяющая отдельные аминокислоты в пептид, называется пептидной.

Главными поставщиками белков Главными поставщиками белков служат мясо, рыба, яйца, творог.

Белок – это высокомолекулярное органическое соединение, представляющее собой биополимер, состоящий из мономеров, которыми являются аминокислоты соединенные пептидной связью. Белок – это высокомолекулярное органическое соединение, представляющее собой биополимер, состоящий из мономеров, которыми являются аминокислоты соединенные пептидной связью. – – NH – CH – CO – NH – CH – CO – NH – CH – R1 R2 R3

углерод C углерод C водород H2 кислород O2 азот N сера S фосфор P железо Fe

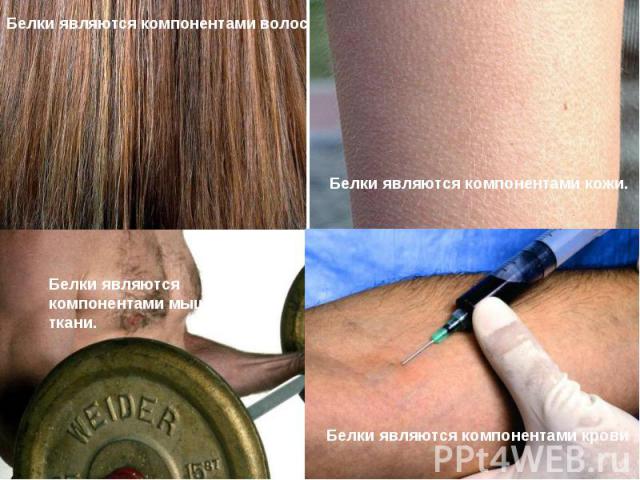
Белки являются компонентами волос Белки являются компонентами волос

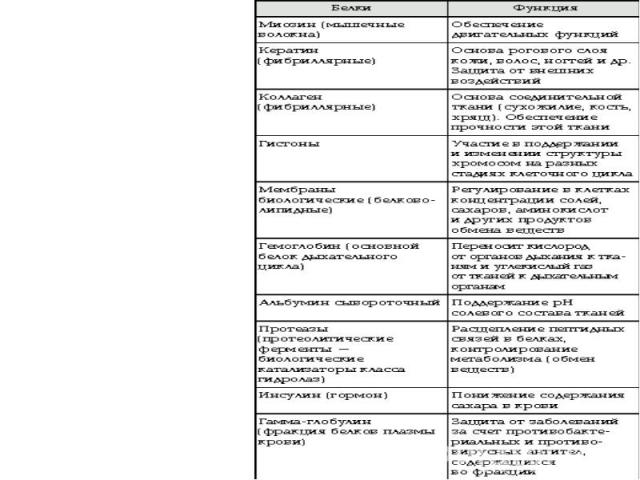
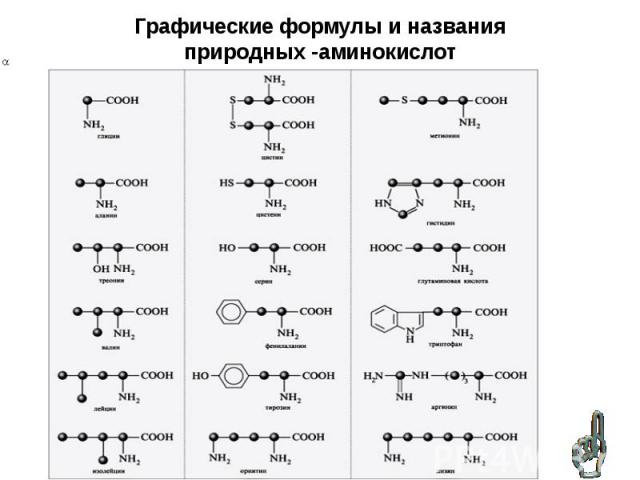
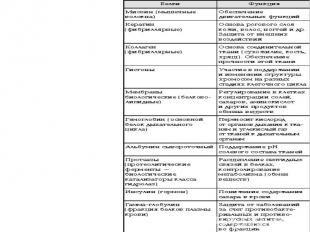
В состав белков входят 20 α - аминокислот, но их остатки могут многократно повторяться в самых различных сочетаниях, поэтому существует огромное число различных белков, каждый из которых имеет свое особенное строение и выполняет свою функцию в жизнедеятельности организма. В состав белков входят 20 α - аминокислот, но их остатки могут многократно повторяться в самых различных сочетаниях, поэтому существует огромное число различных белков, каждый из которых имеет свое особенное строение и выполняет свою функцию в жизнедеятельности организма.
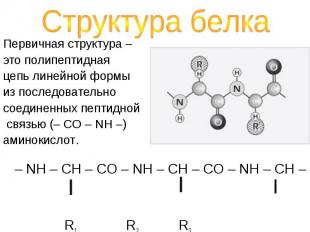
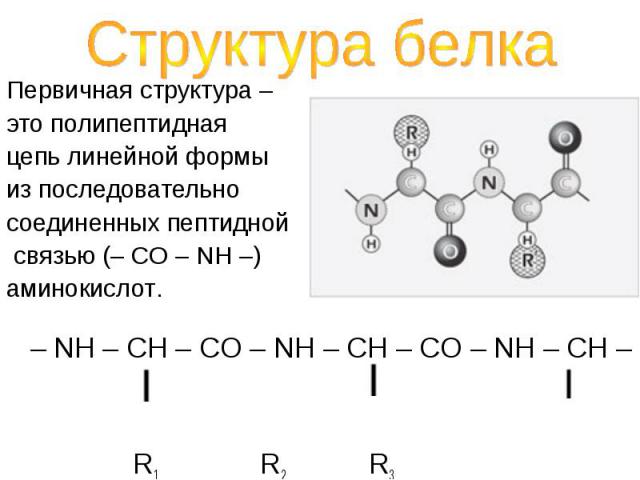
Первичная структура – Первичная структура – это полипептидная цепь линейной формы из последовательно соединенных пептидной связью (– CO – NH –) аминокислот.
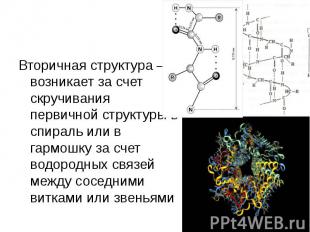
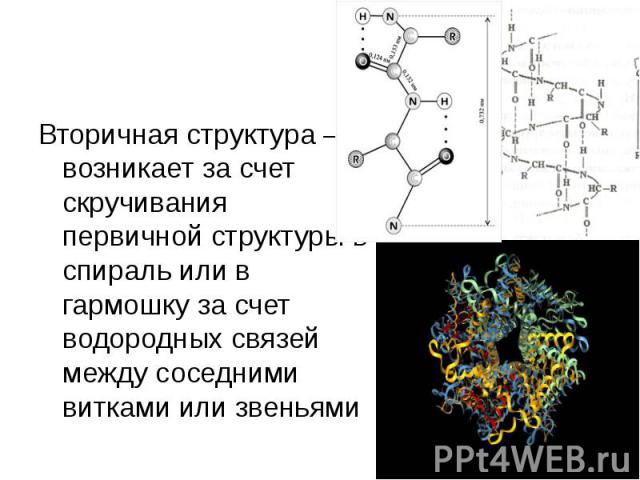
Вторичная структура – возникает за счет скручивания первичной структуры в спираль или в гармошку за счет водородных связей между соседними витками или звеньями Вторичная структура – возникает за счет скручивания первичной структуры в спираль или в гармошку за счет водородных связей между соседними витками или звеньями
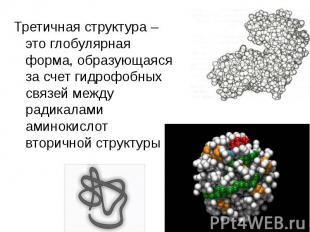
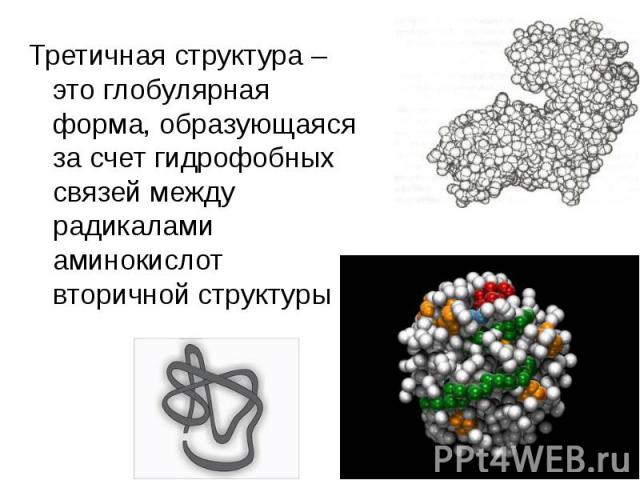
Третичная структура – это глобулярная форма, образующаяся за счет гидрофобных связей между радикалами аминокислот вторичной структуры Третичная структура – это глобулярная форма, образующаяся за счет гидрофобных связей между радикалами аминокислот вторичной структуры
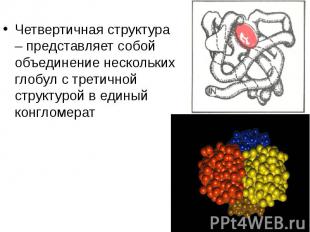
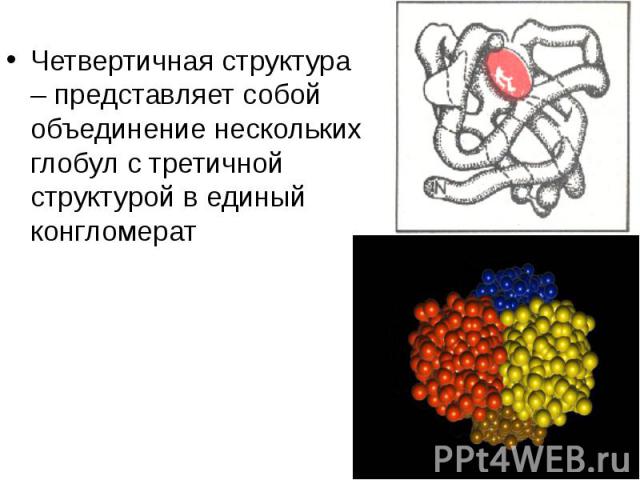
Четвертичная структура – представляет собой объединение нескольких глобул с третичной структурой в единый конгломерат Четвертичная структура – представляет собой объединение нескольких глобул с третичной структурой в единый конгломерат
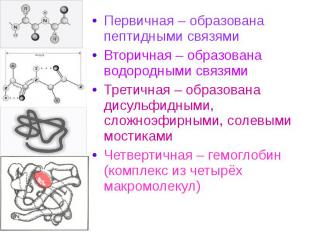
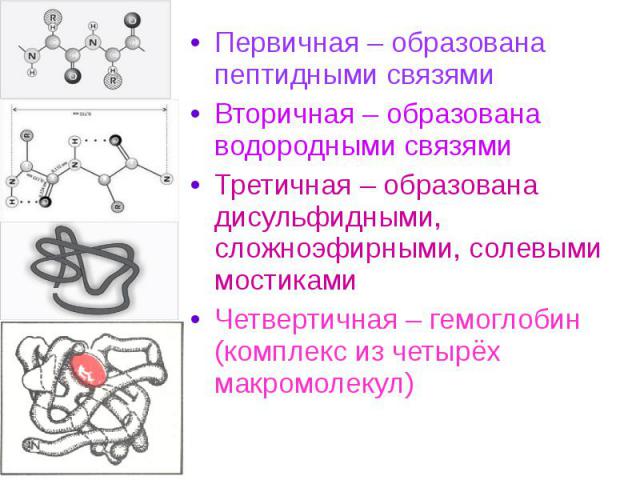
Первичная – образована пептидными связями Первичная – образована пептидными связями Вторичная – образована водородными связями Третичная – образована дисульфидными, сложноэфирными, солевыми мостиками Четвертичная – гемоглобин (комплекс из четырёх макромолекул)

Ксантопротеиновая реакция Ксантопротеиновая реакция В пробирку налейте 2 мл раствора белка и добавьте по каплям 0,5 мл концентрированного раствора азотной кислоты. Осторожно нагревайте пробирку и наблюдайте изменение цвета. РАСТВОР БЕЛКА + HNO3 ? Жёлтый цвет указывает на присутствие ароматических аминокислот Биуретовая реакция К 2–3 мл раствора белка в пробирке добавьте 2–3 мл 10%-го раствора гидроксида натрия. К полученной смеси прилейте 2–3 мл раствора сульфата меди(II). Пробирку встряхните и РАСТВОР БЕЛКА +NaOH + CuSO4 ? Красно – фиолетовый окрас указывает на присутствие пептидной группы РАСТВОР БЕЛКА + СН3СООРb+ NaOH ? Чёрный цвет указывает на присутствие серы


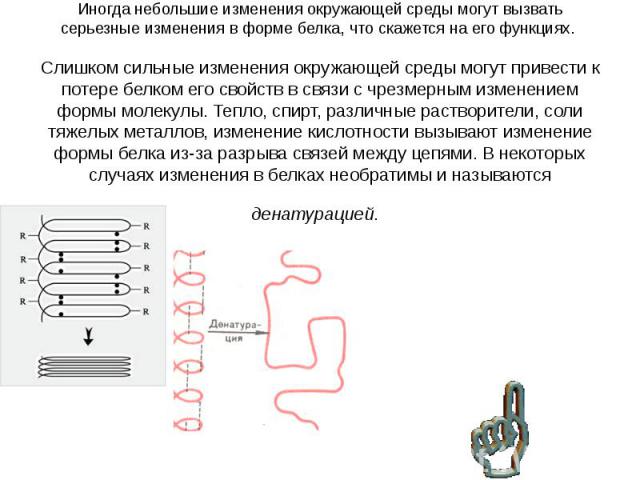
Гидролиз белков – разрушение первичной структуры белка. Гидролиз белков – разрушение первичной структуры белка. Денатурация – полное разрушение пространственной структуры белка. Обратимая денатурация – частичное разрушение пространственной структуры белка. Обратный процесс называется ренатурация.

10 дней - 50 % белков печени и 10 дней - 50 % белков печени и плазмы крови 80 дней - 50 % белков человека 158 дней - белок мышц и кожи человека Жизнь - 200 раз обновление белков организма человека


1. Какие элементы входят в состав белка? 1. Какие элементы входят в состав белка? 2. Какие вещества образуются при гидролизе белков? 3. Опишите физические свойства белков. 4. Какие типы связей наиболее характерны для большинства белковых молекул? 5. Где встречаются белки в природе и каково их значение?

В состав молекулы белка входят: углерод, водород, кислород, азот, сера, фосфор, железо. В состав молекулы белка входят: углерод, водород, кислород, азот, сера, фосфор, железо. При гидролизе белка образуются аминокислоты. Белки бывают растворимые в воде и не растворимые. Для большинства белковых молекул характерны типы связи : пептидные, водородные, сложноэфирные, солевые, дисульфидные. В природе белки встречаются растительного(орехи, масло, жиры, молоко и т.д.) и животного происхождения (яйцо, мясо, рыба) и играют большую роль в биологических процессах живых организмов и людей.

«Жизнь есть способ существования белковых тел…» (Ф.Энгельс) «Жизнь есть способ существования белковых тел…» (Ф.Энгельс)

Искусственное получение природных полипептидов возможно. Для этого необходимо знать, какие аминокислоты входят в состав молекулы, сколько аминокислот каждого вида в полимерной цепи, в какой последовательности они связаны между собой. Искусственное получение природных полипептидов возможно. Для этого необходимо знать, какие аминокислоты входят в состав молекулы, сколько аминокислот каждого вида в полимерной цепи, в какой последовательности они связаны между собой. Выдающимся достижением органической химии стал синтез окситоцина. Этот гормон пептидной природы, стимулирующий выделение молока молочными железами, состоит из остатков 9 аминокислот. Выдающемуся американскому биохимику Винсенту Дю Виньо, всю свою жизнь посвятившему изучению гормонов, витаминов и антибиотиков, в 1932 г. удалось установить структуру окситоцина, а в 1954 г. осуществить его полный синтез из отдельных аминокислот. За эти исследования ему в 1955 г. была присуждена Нобе­левская премия
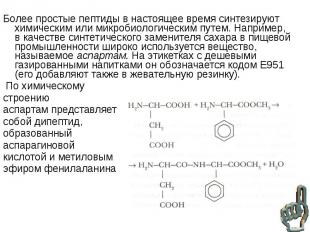
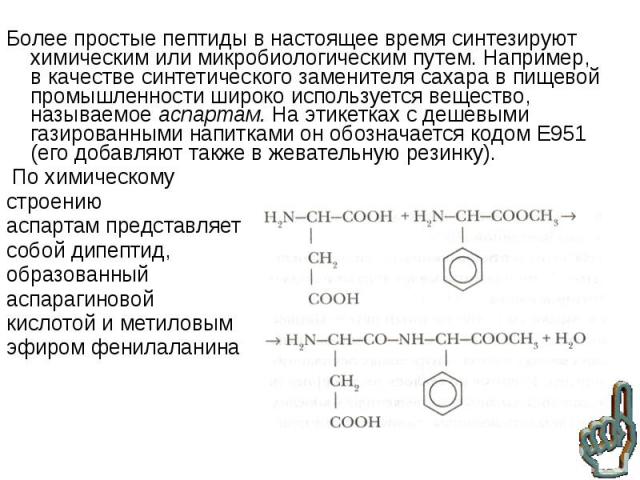
Более простые пептиды в настоящее время синтезируют химическим или микробиологическим путем. Например, в качестве синтетического заменителя сахара в пищевой промышленности широко используется вещество, называемое аспартам. На этикетках с дешевыми газированными напитками он обозначается кодом Е951 (его добавляют также в жевательную резинку). Более простые пептиды в настоящее время синтезируют химическим или микробиологическим путем. Например, в качестве синтетического заменителя сахара в пищевой промышленности широко используется вещество, называемое аспартам. На этикетках с дешевыми газированными напитками он обозначается кодом Е951 (его добавляют также в жевательную резинку). По химическому строению аспартам представляет собой дипептид, образованный аспарагиновой кислотой и метиловым эфиром фенилаланина

Обнаружение белка в мясном бульоне Обнаружение белка в мясном бульоне Поместите в пробирку кусочек мяса и залейте его водой. Нагрейте пробирку до температуры кипения воды и 2–3 мин кипятите содержимое (тем самым получите бульон). Отфильтруйте бульон через марлю с помощью воронки в другую пробирку. Определите наличие белка в бульоне с помощью биуретовой и ксантопротеиновой реакций. Сделайте вывод.