Презентация на тему: Кислотные дожди

Кислотные дожди

Введение Оксиды серы и азота образуются при сгорании каменного угля, нефти, при работе автомобилей. Диоксид серы также выделяется при извержениях вулканов. Растворяясь в атмосферной влаге, они становятся причиной «кислотных дождей», которые поражают растительность, губят живые организмы водоемов, вызывают у людей болезни, разрушают металлоконструкции и строительные материалы. Поэтому очень важно понимать причину кислотных дождей и научиться предотвращать их появление.

Цель работы Изучить процессы сгорания серы: а) на воздухе, б) в кислороде Изучить растворение продуктов сгорания серы в воде Выяснить, как образуются кислотные дожди Изучить их влияние на растения

Что нужно для опыта Сжигание серы в воздухе: Серный цвет (порошок серы) Стеклянный цилиндр Ложечка для сжигания Часовое стекло Спиртовка Лист зеленого растения (хлорофитум)

Сжигание серы в воздухе Набираем порошок серы в ложечку Поджигаем серу в ложечке в пламени спиртовки Вносим ложечку с горящей серой в цилиндр Наблюдаем белый дым от горения серы Смотреть видео

Добавление воды С помощью промывалки вливаем в цилиндр воду В полученный раствор кладем лист зелёного растения хлорофитума Закрываем цилиндр часовым стеклом и оставляем на сутки Смотреть видео

Что нужно для опыта Сжигание серы в кислороде: Серный цвет (порошок серы) Пероксид водорода и диоксид марганца (для получения кислорода) Стеклянный цилиндр Ложечка для сжигания Часовое стекло Спиртовка Лист зеленого растения (хлорофитум)

Получение кислорода Наливаем в цилиндр примерно 10 мл раствора пероксида водорода, добавляем диоксид марганца Начинается выделение кислорода по реакции 2H2O2 = 2H2O + O2 (диоксид марганца – катализатор реакции)

Сжигание серы в кислороде Серу насыпаем в ложечку и поджигаем в пламени спиртовки Ложечку с зажженной серой вносим в цилиндр и кислородом Сера горит ярко-фиолетовым пламенем Образуется белый дым Смотреть видео

Добавление воды С помощью промывалки вливаем в цилиндр воду В полученный раствор кладем лист зелёного растения хлорофитума Закрываем цилиндр часовым стеклом и оставляем на сутки Смотреть видео

Через сутки На фотографии видно, как сильно повреждаются листья хлорофитума при действии «кислотного дождя»

Добавили лакмус, мел и магний С помощью пипетки капаем на полоски красной и синей лакмусовой бумаги по 2 капли «кислотного дождя – раствора продуктов сгорания серы в воде Капаем «кислотный дождь» на кусочек мела Капаем «кислотный дождь» на магниевую стружку Красная лакмусовая бумага осталась без изменений, а синяя покраснела Мел запузырился, выделяется углекислый газ Магний начал растворяться, выделился водород
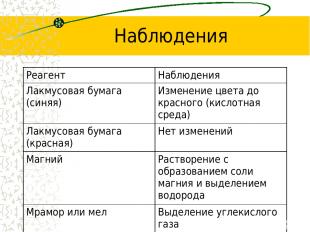
Наблюдения Реагент Наблюдения Лакмусовая бумага (синяя) Изменение цвета до красного (кислотная среда) Лакмусовая бумага (красная) Нет изменений Магний Растворение с образованием соли магния и выделением водорода Мрамор или мел Выделение углекислого газа

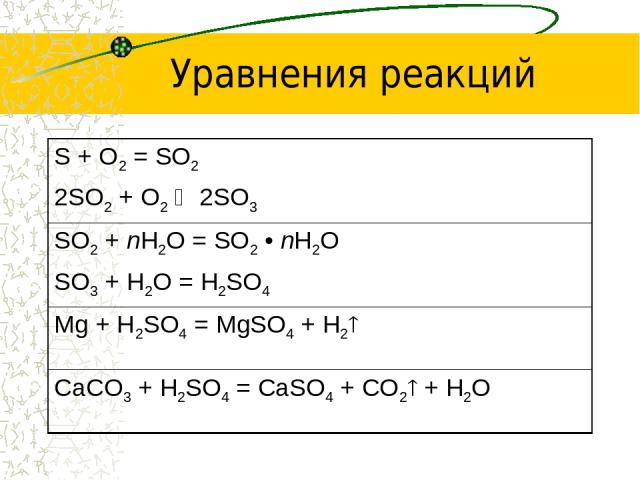
Уравнения реакций S + O2 = SO2 2SO2 + O2 2SO3 SO2 + nH2O = SO2 • nH2O SO3 + H2O = H2SO4 Mg + H2SO4 = MgSO4 + H2 CaCO3 + H2SO4 = CaSO4 + CO2 + H2O

Выводы При проведении опыта окисление диоксида серы до триоксида серы не происходит. Но эта реакция идет в атмосфере и в промышленности при нагревании в присутствии катализатора. Кислотные дожди разрушают растительные клетки, растворяют магний и мел. Металлические детали и памятники архитектуры, если на них постоянно действуют кислотные дожди, будут разрушаться (из-за коррозии). Чтобы предотвратить кислотные дожди, надо улавливать примеси диоксида серы (из трубы).

Опыты сделали: Маша Бородаевская, Таня Меженова и Рома Балакин