Презентация на тему: Бериллий

Бериллий Работу выполнила ученица 9Б Завилейская Екатерина

Положение в периодической таблице. N=4 => Z=+4 => p=4 => e=4 => A=9 => n=5 2 группа => 2 внешних е => Ме 2 период => )) => 2 ряд Электронный паспорт: Be)2)2 Электронная формула: 1s22s2

Особенности строения. В природе встречается только один изотоп 9Be. Атомный радиус 0,113нм. В соединениях проявляет только степень окисления +2. Электроотрицательность 1,5. Химическая формула- Be. Щелочноземельный металл

Вид связи и кристаллическая решетка. Связь - металлическая Металлическая связь - химическая связь, которая обусловлена взаимодействием положительных ионов металлов, составляющих кристаллическую решетку, с электронным газов из валентных электронов. Кристаллическая решетка: α-Ве решетка гексагонального типа β-Ве решетка кубическаго типа
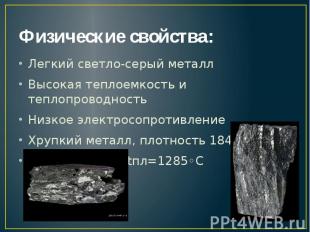
Физические свойства: Легкий светло-серый металл Высокая теплоемкость и теплопроводность Низкое электросопротивление Хрупкий металл, плотность 1847,7 кг/м3 tкип=2470◦С и tпл=1285◦С

Химические свойства: Амфотерный гидроксид Оксид и гидроксид бериллия реагируют со щелочами с образованием солей: Бериллий плохо вступает в реакции. Если поджечь порошок бериллия, он будет гореть ярким пламенем.

Взаимодействует с серной кислотой: Взаимодействует с серной кислотой: Ве + 2Н2SO4(к) = BeSO4 + 2H2O + SO2 Ве + Н2SO4(р) = BeSO4 + H2 Взаимодействует с азотной кислотой: Ве + 4НNO3(к) = Be(NO3)2 + 2H2O + 2NO2 3Be + 8HNO3(р) = 3Be(NO3)2 + 4H2O + 2NO

Получение: В виде простого вещества в 19 веке бериллий получали действием калия на безводный хлорид бериллия: BeCl2 + 2К Be + КCl В настоящее время бериллий получают, восстанавливая его фторид магнием: BeF2 + Mg = MgF2 + Be Либо электролизом расплава смеси хлоридов бериллия и натрия.

Применение: в рентгенотехнике в ядерной энергетике, как замедлитель нейтронов в лазерной технике для изготовления излучателей в аэрокосмической технике, при изготовлении тепловых экранов как огнеупорный материал

Интересные факты: Бериллий ядовит: Летучие (и растворимые) соединения бериллия, в том числе и пыль, содержащая соединения бериллия, высокотоксичны. Бериллий обладает ярко выраженным аллергическим и канцерогенным действием. Вдыхание атмосферного воздуха, содержащего бериллий, приводит к тяжёлому заболеванию органов дыхания — бериллиозу. Открыт в 1798 г. французским химиком Луи Никола Вокленом, который назвал его глицинием. Современное название элемент получил по предложению химиков немца Клапрота и шведа Экеберга. Большую работу по установлению состава соединений бериллия и его минералов провёл российский химик И. В. Авдеев. Именно он доказал, что оксид бериллия имеет состав BeO, а не Be2O3, как считалось ранее.

Знаете ли Вы, что... 1) Из бериллия была сделана внешняя тепловая защита капсулы космического корабля "Фрэндшип-7" 2) Бериллий в несколько раз дороже титана 3) На 1т. земного вещества в среднем приходится лишь 4,2 г бериллия

Конец!!! Спасибо за внимание.
























