Презентация на тему: Поверхностные явления

* Поверхностные явления 900igr.net
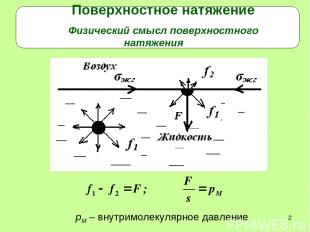
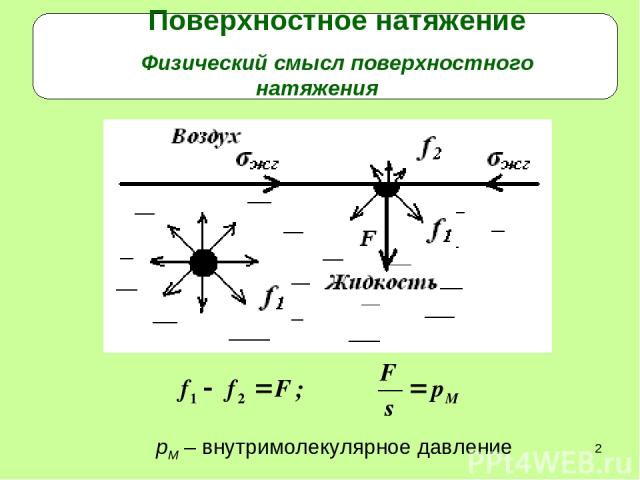
* Поверхностное натяжение Физический смысл поверхностного натяжения рМ – внутримолекулярное давление

* Энергетическое определение поверхностного натяжения Поверхностное натяжение (σ) – работа обратимого изотермического процесса, затраченная на образование единицы площади поверхности раздела фаз:

* Термодинамическое определение поверхностного натяжения Поверхностное натяжение - частная производная от любого термодинамического потенциала по площади межфазной поверхности при постоянных соответствующих параметрах. Единицы измерения Энергетическая – Дж/м2, силовая – Н/м. Для воды при 293 К: СИ: Дж/м2 = Н∙м/м2 =Н/м
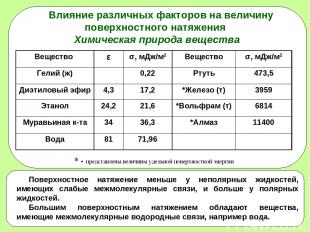
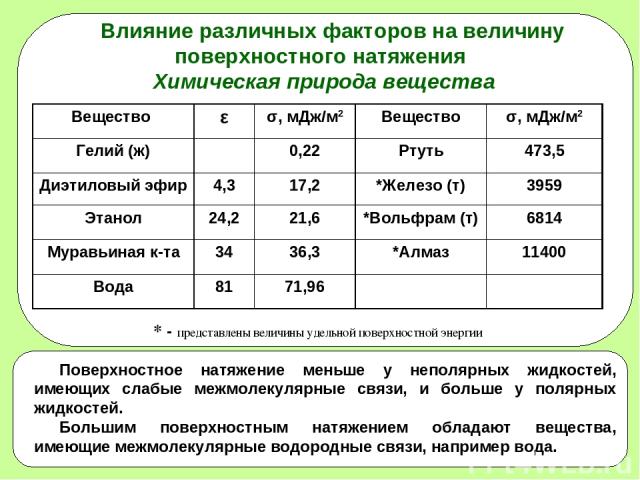
* Влияние различных факторов на величину поверхностного натяжения Химическая природа вещества * - представлены величины удельной поверхностной энергии Вещество ε σ, мДж/м2 Вещество σ, мДж/м2 Гелий (ж) 0,22 Ртуть 473,5 Диэтиловый эфир 4,3 17,2 *Железо (т) 3959 Этанол 24,2 21,6 *Вольфрам (т) 6814 Муравьиная к-та 34 36,3 *Алмаз 11400 Вода 81 71,96

* Природа граничащих фаз Поверхностное натяжение на границе двух жидкостей зависит от полярности.

* Межмолекулярные и межфазные взаимодействия

* Адгезия Адгезия – взаимодействие между разнородными конденсированными телами при их молекулярном контакте. Причина адгезии – молекулярное притяжение контактирующих веществ или их химическое взаимодействие.

* Растекание жидкости
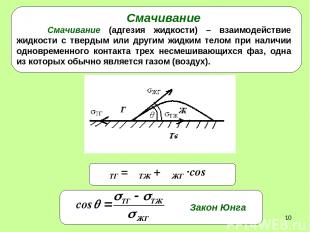
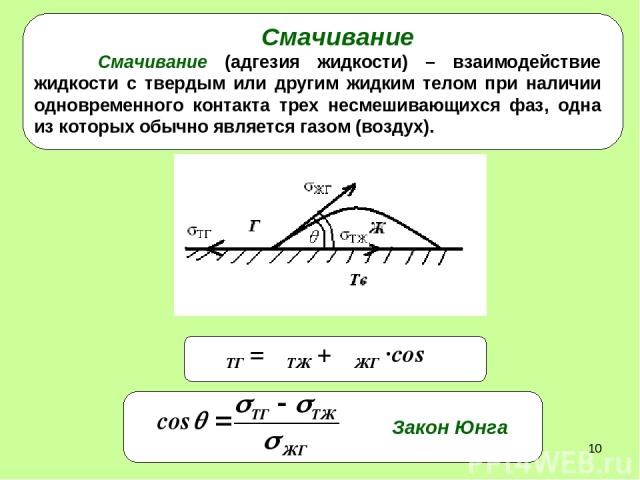
* Смачивание Смачивание (адгезия жидкости) – взаимодействие жидкости с твердым или другим жидким телом при наличии одновременного контакта трех несмешивающихся фаз, одна из которых обычно является газом (воздух).

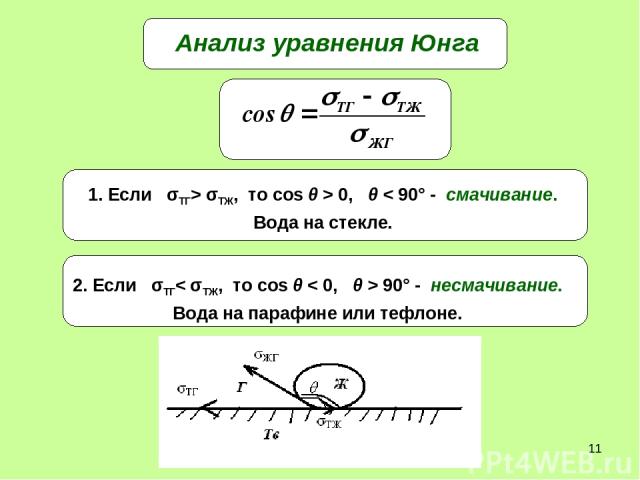
* Анализ уравнения Юнга

* Анализ уравнения Юнга

* Правило: лучше смачивает поверхность та жидкость, которая ближе по полярности к смачиваемому материалу.

* Флотация

* Пример. Порошок кварца и серы высыпали на поверхность воды. Какое явление можно ожидать, если краевой угол смачивания для кварца 0°, а для серы 78°.

* Капиллярные явления капиллярное поднятие (опускание) жидкости; капиллярная конденсация; изотермическая перегонка.
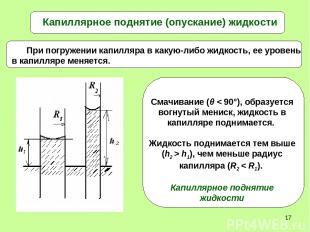
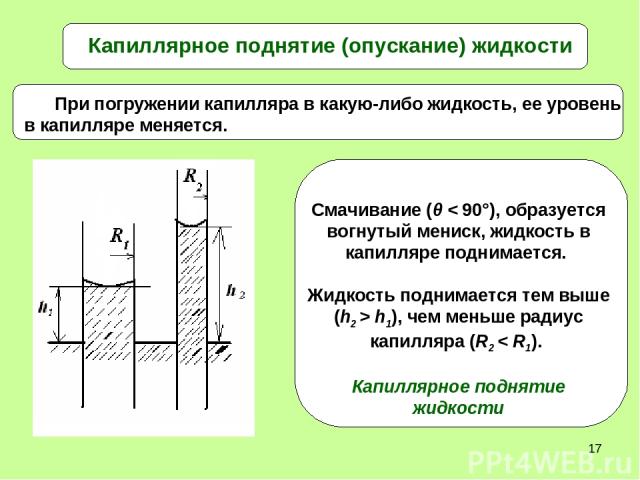
* Капиллярное поднятие (опускание) жидкости

*
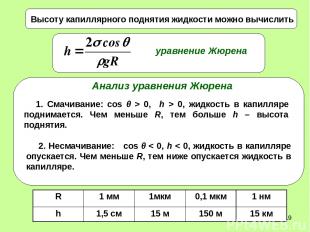
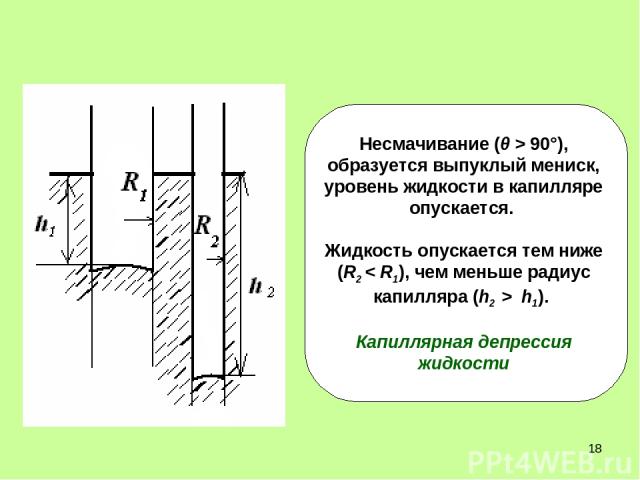
* Высоту капиллярного поднятия жидкости можно вычислить 1. Смачивание: cos θ > 0, h > 0, жидкость в капилляре поднимается. Чем меньше R, тем больше h – высота поднятия. 2. Несмачивание: cos θ < 0, h < 0, жидкость в капилляре опускается. Чем меньше R, тем ниже опускается жидкость в капилляре. R 1 мм 1мкм 0,1 мкм 1 нм h 1,5 см 15 м 150 м 15 км

* Капиллярным поднятием жидкостей объясняется ряд известных процессов и явлений: поднятие грунтовых вод в почвах обеспечивает существование растительного покрова Земли; пропитка бумаги и тканей – поднятие жидкости в порах; водонепроницаемость тканей – ткани пропитывают веществами, которые вода не смачивает – капиллярная депрессия; питание растений (деревьев) – подъем воды из почвы по волокнам древесины; процессы кровообращения в кровеносных сосудах.
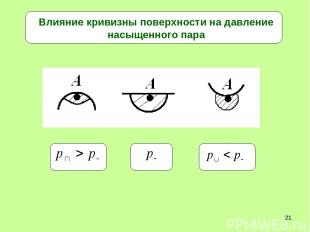
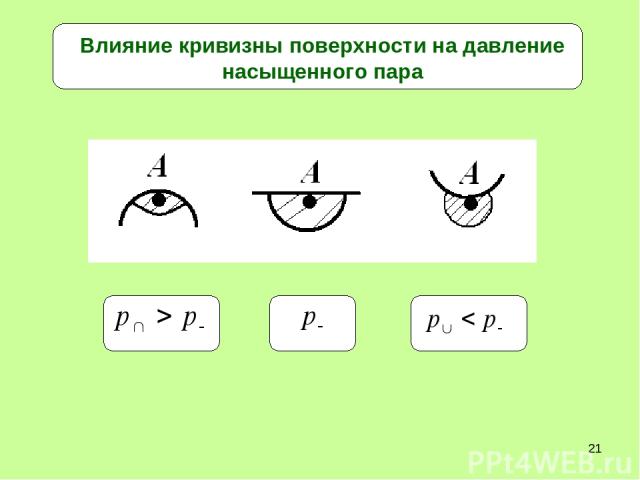
* Влияние кривизны поверхности на давление насыщенного пара
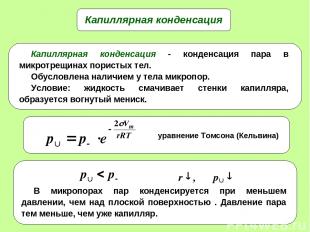
* Капиллярная конденсация

* Изотермическая перегонка
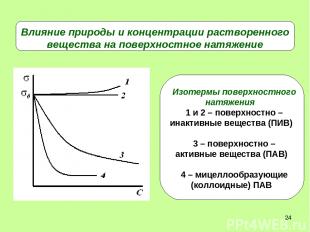
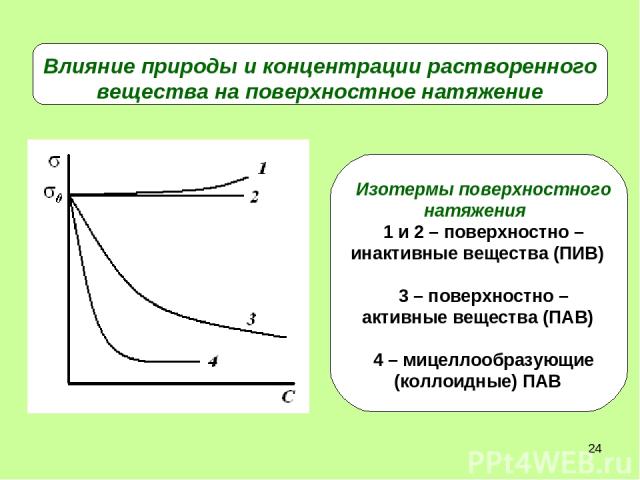
* Влияние природы и концентрации растворенного вещества на поверхностное натяжение
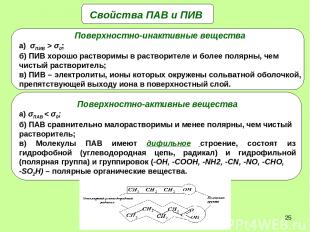
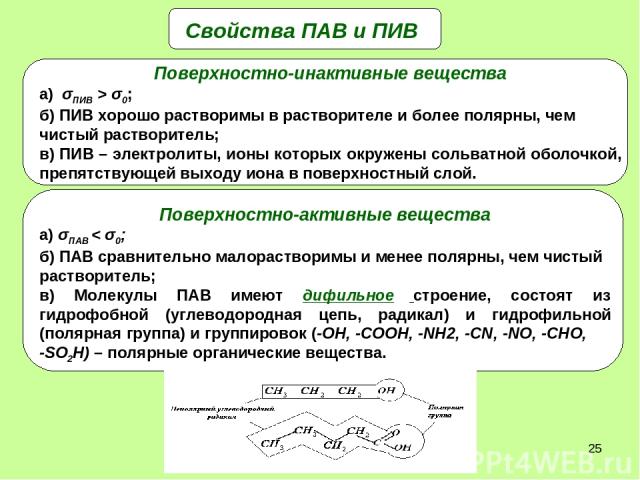
* Свойства ПАВ и ПИВ
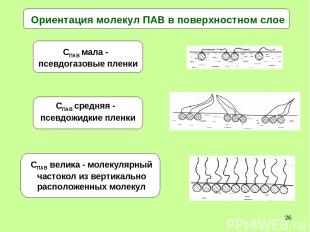
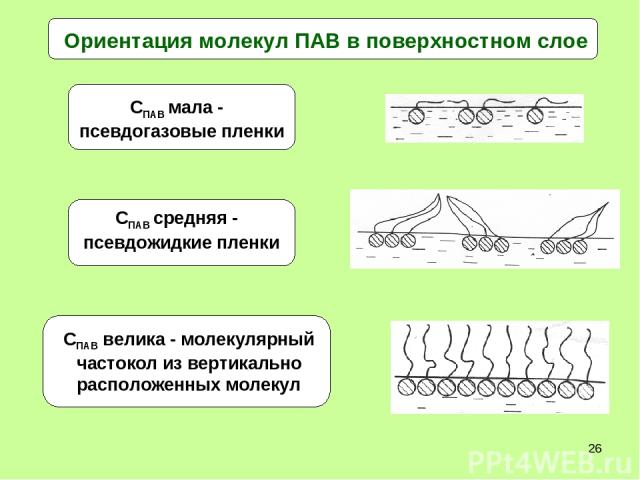
* Ориентация молекул ПАВ в поверхностном слое
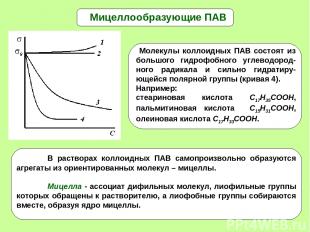
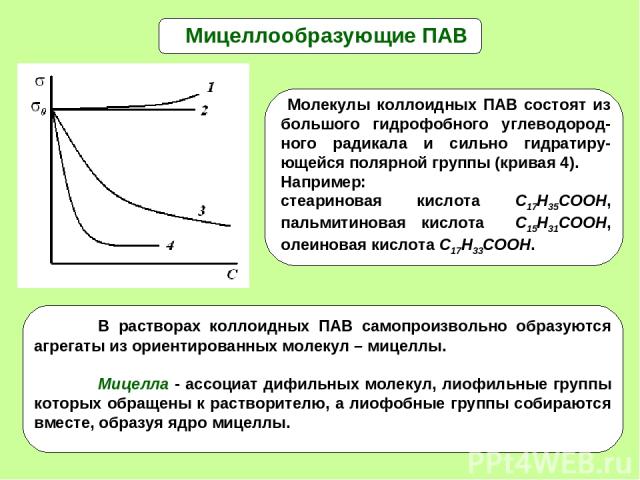
* Мицеллообразующие ПАВ Молекулы коллоидных ПАВ состоят из большого гидрофобного углеводород-ного радикала и сильно гидратиру-ющейся полярной группы (кривая 4). Например: стеариновая кислота С17Н35СООН, пальмитиновая кислота С15Н31СООН, олеиновая кислота С17Н33СООН.
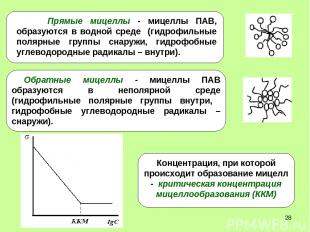
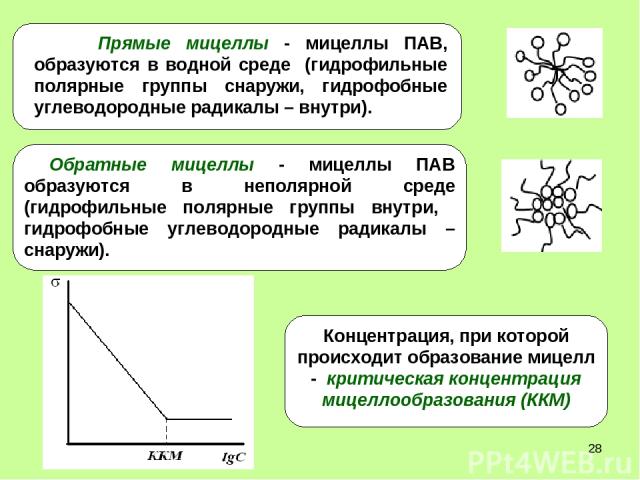
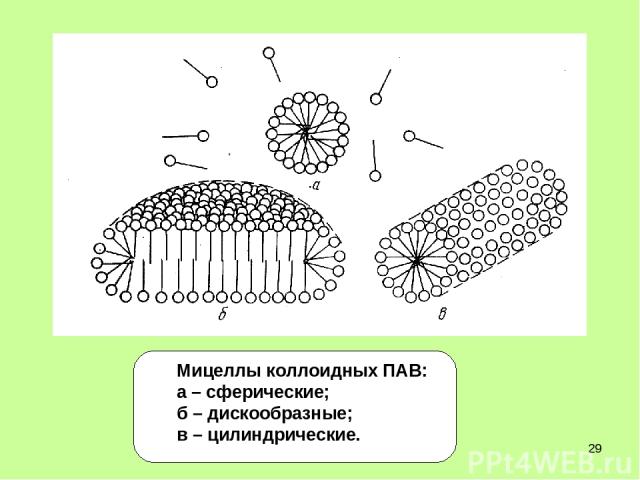
* Прямые мицеллы - мицеллы ПАВ, образуются в водной среде (гидрофильные полярные группы снаружи, гидрофобные углеводородные радикалы – внутри).
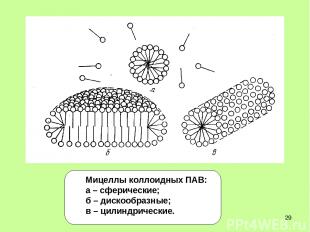
* Мицеллы коллоидных ПАВ: а – сферические; б – дискообразные; в – цилиндрические.

* Солюбилизация

*