Презентация на тему: Первый закон термодинамики

Первый закон термодинамики Цель урока: Сформулировать первый закон сохранения энергии, распространённый на тепловые явления, познакомить учащихся с историей открытия закона, развивать навыки решения задач на применение первого закона термодинамики.

Самостоятельная работа Что называется внутренней энергией? Запишите формулу для работы газа. От каких величин зависит внутренняя энергия идеального одноатомного газа? Какая физическая величина вычисляется по формуле 3/2*р*V При постоянном давлении 10^5 Па объём воздуха, находящийся в квартире увеличился на 20дм^3. Какую работу совершил газ? Ответы.

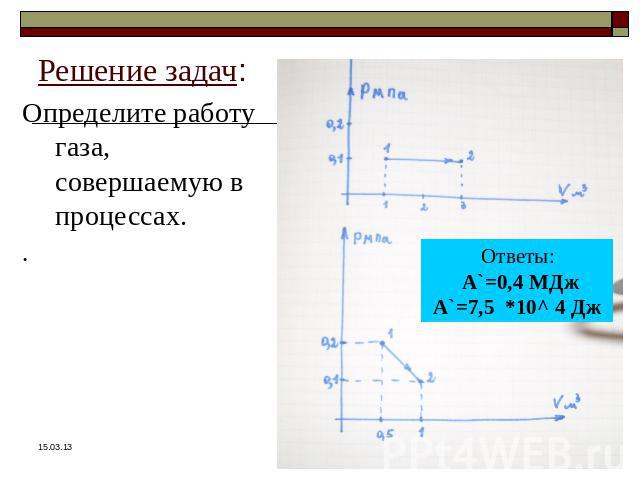
Определите работу газа, совершаемую в процессах. Ответы: А`=0,4 МДж А`=7,5 *10^ 4 Дж

Обсуждение вопросов: Как рассчитать количество теплоты, необходимого для нагревания тела? Что называется удельной теплоёмкостью? Как рассчитать количество теплоты, необходимое для превращения в пар жидкости массой m, взятой при температуре кипения? Что называется удельной теплотой парообразования, конденсации? Запишите формулу для расчёт количества теплоты, необходимого для того, чтобы расплавить кристаллическое тело массой m , взятое при температуре плавления. Что называется удельной теплотой плавления? В каком случае в формулах используется знак «-»

Первый закон термодинамики- это закон сохранения энергии, распространённый на тепловые явления. Он показывает от каких причин зависит изменение внутренней энергии. Причины изменения внутренней энергии: Совершение работы над телом или самим телом. Теплопередача с окружающими телами.
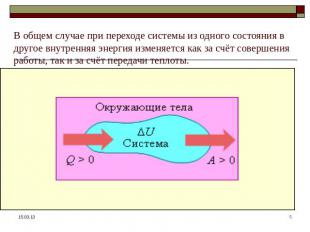
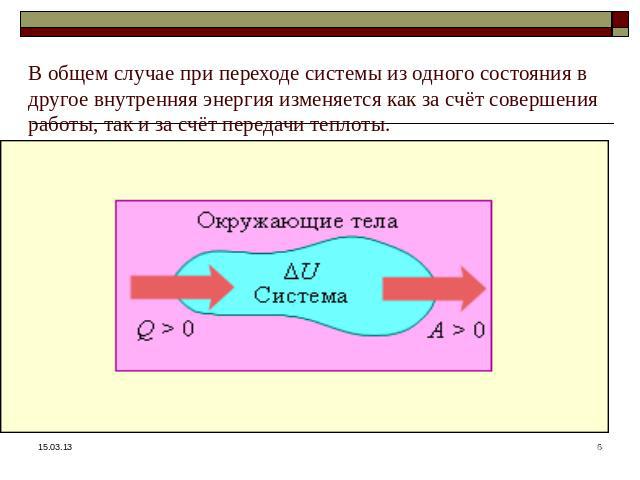
В общем случае при переходе системы из одного состояния в другое внутренняя энергия изменяется как за счёт совершения работы, так и за счёт передачи теплоты.

Формулировка закона для случая, если работа совершается над газом: Формулировка закона для случая, если работа совершается над газом: Изменение внутренней энергии системы при переходе её из одного состояния в другое равно сумме работы внешних сил и количества теплоты , переданного системе.

Формулировка закона для случая, если работа совершает сам газ: Количество теплоты, переданное системе, идёт на изменение её внутренней энергии и на совершение системой работы над внешними телами

Углубление знаний и умений Какое количество теплоты получил идеальный газ, взятый в количестве двух молей при изобарном нагревании на 50 градусов Кельвина и как при этом изменилась его внутренняя энергия? Ответ: Q =2077 Дж Для изобарного нагревания газа, количество вещества которого 800 моль на 500 градусов Кельвина ему сообщили количество теплоты 9,4 МДж. Определите работу газа и изменение его внутренней энергии. Ответ: ΔU =6,1 МДж Решение.

Задача повышенной сложности 3.Объём кислорода массой 160г, температура которого 27 градусов Цельсия, при изобарном нагревании увеличился вдвое. Найти работу газа при расширении, количество теплоты, которое пошло на нагревание кислорода, а также изменение внутренней энергии. Ответ: ΔU =31,3 КДж, Q = 43,8 КДж

Итоги урока Параграф 80 (вопросы)

Энергия в природе не возникает из ничего и не исчезает: количество энергии неизменно, она только переходит из одной формы в другую. Закон сохранения энергии был установлен в середине ХIХ века на основе работ, выполненных несколькими знаменитыми учёными. Немецкий учёный Р. Майер высказал теоретические положения, англичанин Д. Джоуль провёл экспериментальные исследования, а немецкий физик Г. Гельмгольц вывел математическое выражение закона, обобщил и распространил полученные результаты на все явления природы.

1. А`=Р*ΔV=m/М*R*ΔT= =ν*R*ΔT ΔU= 3/2*ν*R*ΔT Q = ΔU + A` Q = 3/2*ν*R*ΔT + ν*R*ΔT = 5/2* ν*R*ΔT = =2,5*2моль*8,31Дж/моль*К**50К = 2077 Дж 2. . А`=ν* R*ΔT= 800моль*8,31Дж/мольК *500К= 33,24*10^4 Дж ΔU = Q - A` ΔU = Q - ν* R*ΔT = 9,4*10^6 Дж –800моль*8,31Дж/мольК *500К= 6,1 МДж

Решение сложной задачи А`= Р*ΔV=m/М*R*ΔT Так как V2/V1=T2/T1, T2/T1=2, T2 = 2*T1 Тогда А`= m/М*R*(2*T1-T1) ΔU=5/2*m/M*R*ΔT=5/2*m/M*R*T1 Q = ΔU + A`=7/2*m/M*R*T1

Ответы на вопросы сам. работы. Внутренняя энергия макроскопического тела равна сумме кинетических энергий беспорядочного движения всех молекул(или атомов) тела и потенциальной энергии взаимодействия всех молекул друг с другом. А`=Р*ΔV U=3/2*m/M*R*T Внутренняя энергия одноатомного идеального газа. А`=Р*ΔV=10^5Па *50*10^3м^3= 2 кДж