Презентация на тему: Бериллий, магний и щелочноземельные металлы

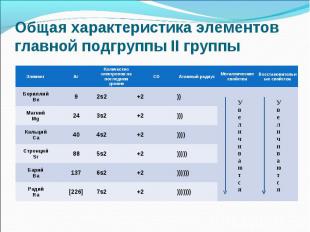

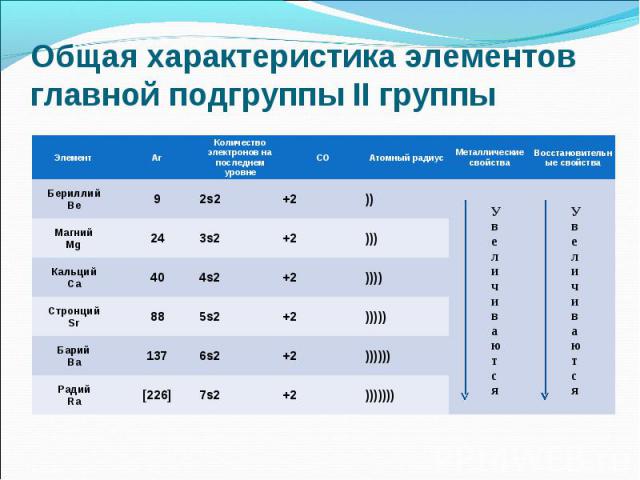
Ве - амфотерный металл, Ве - амфотерный металл, Mg – металл, Сa, Sr,Ba - щёлочноземельные металлы Ra –радиоактивный элемент

Одинаковое строение внешнего электронного слоя Одинаковое строение внешнего электронного слоя Элементы проявляют СО +2 Атомы элементов являются сильными восстановителями, т.к содержат 2 электрона на внешнем энергетическом уровне, которые отдают при взаимодействиями с другими элементами. С увеличением № элементов увеличивается атомный радиус, увеличивается число электронных слоев, следовательно возрастает легкость отдачи электронов. Восстановительные свойства увеличиваются в группе сверху вниз.




BeO – амфотерный оксид BeO – амфотерный оксид MgO CaO SrO Основные оксиды BaO


Ве(ОН)2 – амфотерный гидроксид Ве(ОН)2 – амфотерный гидроксид Mg(OH)2 – нерастворимое основание Ca(OH)2 Sr(OH)2 Ba(OH)2



Са(ОН)2 ←Са→СаО→Са(ОН)2→Са(NO3)2→CaSO4 Са(ОН)2 ←Са→СаО→Са(ОН)2→Са(NO3)2→CaSO4 Be→BeO→BeCl2→Be(OH)2→Na2BeO2 ↓ BeSO4

§12 упр 5 §12 упр 5