Презентация на тему: Методы очистки питьевой воды

Методы очистки питьевой воды Выполнил: Сабадашов К.С. ученик 11 «Б» гимназии №25 Руководитель: Безик Ю.Б. г. Краснодар

Цели и задачи исследования: – знакомство с теорией по данной проблеме; – проведение экологического мониторинга состояния питьевой воды в выбранных районах; – выявление основных загрязнителей воды; – установление соответствия качества питьевой воды санитарным нормам; – сопоставление качества исследуемой воды; – определение химических показателей дополнительно очищенной воды; – составление таблиц и графиков по данному материалу

Что такое питьевая вода? Питьевой считается вода, пригодная к употреблению внутрь и отвечающая критериям качества - то есть вода безопасная и приятная на вкус. В мире эти критерии были утверждены Европейским Сообществом, а затем приняты с некоторой адаптацией каждой из стран. В нашей стране c 1 января 2002 года действует документ с названием "Санитарные правила и нормативы СанПиН 2.1.4.1074-01".

Без воды наше существование невозможно. А без хорошей воды невозможно хорошее существование. Вода доставляет в клетки организма питательные вещества и уносит отходы жизнедеятельности, участвует в процессе терморегуляции и дыхания. Для нормальной работы всех систем человеку необходимо как минимум 1,5 литра воды в день. Парадоксальный факт: вода необходима для жизни, но она же является и одной из главных причин заболеваемости в мире. Опасность употребления некачественной воды может быть микробиологической: вода в природе содержит множество микроорганизмов, некоторые из которых вызывают у человека такие заболевания, как холера, тиф, гепатит или гастроэнтерит. Загрязнение воды может быть и химическим. При этом последствия употребления грязной воды могут наступить как немедленно, так и через несколько лет.

Основные методы очистки воды для хозяйственно-питьевого водоснабжения Проблема очистки воды охватывает вопросы физических, химических и биологических ее изменений в процессе обработки с целью сделать ее пригодной для питья, т.е. очистки и улучшения ее природных свойств. Основными методами очистки воды для хозяйственно-питьевого водоснабжения являются осветление, обесцвечивание и обеззараживание.

Осветление воды путем осаждения взвешенных веществ Эту функцию выполняют осветлители, отстойники и фильтры. В осветлителях и отстойниках вода движется с замедленной скоростью, происходит выпадение в осадок взвешенных частиц. В целях осаждения мельчайших коллоидных частиц, к воде прибавляют раствор коагулянта (сернокислый алюминий, железный купорос или хлорное железо). В результате образуются хлопья, увлекающие при осаждении взвеси и коллоидные вещества.

Фильтрование Фильтрование — самый распространенный метод отделения твердых частиц от жидкости. При этом из раствора могут быть выделены не только диспергированные частицы, но и коллоиды. В процессе фильтрования происходит задержание взвешенных веществ в порах фильтрующей среды и в биологической пленке, окружающей частицы фильтрующего материала. Вода освобождается от взвешенных частиц, хлопьев коагулянта и большей части бактерий.

Обесцвечивание Обесцвечивание воды, т. е. устранение или обесцвечивание различных окрашенных коллоидов или полностью растворенных веществ может быть достигнуто коагулированием, применением различных окислителей (хлор и его производные, озон, перманганат калия) и сорбентов (активный уголь, искусственные смолы).

Обеззараживание воды (дезинфекция) Так как полного освобождения воды от болезнетворных бактерий ни отстаивание, ни фильтрование не дают, с целью дезинфекции применяют следующие способы: введение в воду сильных окислителей (хлор, йод, марганцево-кислый калий, перекись водорода, гипохлорит натрия и кальция, жидкий хлор и хлорную известь), способных убивать ферменты бактериальных клеток; нагревание воды до температуры 80 °С (пастеризация) — 100 °С (стерилизация); облучением воды ультрафиолетовыми лучами; озонированием; воздействием ультразвуком; введением в воду серебра или других металлов, обладающих олигодинамическим действием на микроорганизмы. Практическое применение нашли 1, 3 и 4-й методы.

Для устранения запаха хлора к обрабатываемой воде прибавляют одновременно с хлором в небольших количествах аммиак (аммонизация воды). Хлор, введенный в воду, образует хлорноватистую кислоту и соляную кислоту по уравнению Сl2 + Н2О = = НОСl + НСl. Хлорноватистая кислота НОСl — соединение нестойкое, диссоциирующее с образованием гипохлоритного иона ОСl. При этом окислительное действие на органические вещества, в том числе и бактерии, проявляют как хлорноватистая кислота, так и гипохлоритный ион. Соляная кислота соединяется с карбонатами, находящимися в воде. Для устранения запаха хлора к обрабатываемой воде прибавляют одновременно с хлором в небольших количествах аммиак (аммонизация воды). Хлор, введенный в воду, образует хлорноватистую кислоту и соляную кислоту по уравнению Сl2 + Н2О = = НОСl + НСl. Хлорноватистая кислота НОСl — соединение нестойкое, диссоциирующее с образованием гипохлоритного иона ОСl. При этом окислительное действие на органические вещества, в том числе и бактерии, проявляют как хлорноватистая кислота, так и гипохлоритный ион. Соляная кислота соединяется с карбонатами, находящимися в воде.

Дезодорация воды Для удаления из воды веществ, вызывающих нежелательные привкусы и запахи, применяют следующие методы ее обработки: аэрацию (основана на летучести большинства веществ, обуславливающих привкусы и запахи); окисление хлором, озоном, перманганатом калия и другими окислителями (для удаления из воды запахов, обусловленных жизнедеятельностью микроорганизмов и водорослей); сорбцию активным углем.

Ступени водоочистки Учитывая состав водопроводной воды, которая зачастую содержит хлориды, фториды, сульфиды, сульфаты, металлы, хлор и хлорорганические соединения, а также промышленные загрязнения в виде хрома, никеля, ртути, свинца, мышьяка, меди, радионуклидов, большинство производителей предлагают фильтры многоступенчатой водоочистки. В процессе прохождения через такой фильтр на каждой ступени очистки вода теряет те или иные примеси.

1-ая ступень - это механическая очистка воды, в процессе которой удаляются такие инородные частицы, как песок, ил, ржавчина. Осуществляется она с помощью полипропиленовой сетки, в зависимости от размеров отверстий в которой удерживаются только примеси (микрофильтрация) или примеси и бактерии (ультрафильтрация). 1-ая ступень - это механическая очистка воды, в процессе которой удаляются такие инородные частицы, как песок, ил, ржавчина. Осуществляется она с помощью полипропиленовой сетки, в зависимости от размеров отверстий в которой удерживаются только примеси (микрофильтрация) или примеси и бактерии (ультрафильтрация).

2-ая ступень - удаление хлора, пестицидов, запахов. Происходит адсорбция, то есть поглощение частиц в порах какого-либо материала. Самым распространенным адсорбентом является природный фильтрант уголь, также используются синтетические волокна. 2-ая ступень - удаление хлора, пестицидов, запахов. Происходит адсорбция, то есть поглощение частиц в порах какого-либо материала. Самым распространенным адсорбентом является природный фильтрант уголь, также используются синтетические волокна. Уголь очищает, поглощая остаточный хлор, органические соединения и споры бактерий, и улучшает - вкус, запах, цвет питьевой воды . Многие производители применяют активированный уголь из скорлупы кокоса, адсорбционная способность которого в 4 раза выше. Чтобы предотвратить размножение бактерий внутри фильтра активированный уголь покрывают слоем серебра. В некоторых фильтрах используется полимерное углеродное волокно аквален - смесь угля и синтетических материалов.

3-я ступень - умягчение воды и ее освобождение от тяжелых металлов - ионный обмен. Помимо всего вышесказанного, мягкая вода в несколько раз улучшает вкус чая, кофе и других напитков, а также более пригодна для умывания и применения в быту.

Методы очистки воды Существует несколько методов очистки воды, но все они входят в три группы методов: - механические методы; - физико-химические методы; - биологические методы.

Наиболее дешевая - механическая очистка - применяется для выделения взвесей. Основные методы: процеживание, отстаивание и фильтрование. Применяются, как предварительные этапы. Химическая очистка применяется для выделения из сточных вод растворимых неорганических примесей. При обработке сточных вод реагентами происходит их нейтрализация, выделение растворенных соединений, обесцвечивание и обеззараживание стоков. Физико-химическая очистка применяется для очистки сточных вод от грубо- и мелкодисперсионных частиц, коллоидных примесей, растворенных соединений. Высокопроизводительный и в то же время дорогой способ очистки. Биологические методы применяются для очистки от растворенных органических соединений. Метод основан на способности микроорганизмов разлагать растворенные органические соединения. Наиболее дешевая - механическая очистка - применяется для выделения взвесей. Основные методы: процеживание, отстаивание и фильтрование. Применяются, как предварительные этапы. Химическая очистка применяется для выделения из сточных вод растворимых неорганических примесей. При обработке сточных вод реагентами происходит их нейтрализация, выделение растворенных соединений, обесцвечивание и обеззараживание стоков. Физико-химическая очистка применяется для очистки сточных вод от грубо- и мелкодисперсионных частиц, коллоидных примесей, растворенных соединений. Высокопроизводительный и в то же время дорогой способ очистки. Биологические методы применяются для очистки от растворенных органических соединений. Метод основан на способности микроорганизмов разлагать растворенные органические соединения.

В настоящее время из общего количества сточных вод механической очистки подвергается 68% всех стоков, физико-химической- 3%, биологической - 29%. В перспективе предполагается повысить долю очистки биологическим методом до 80%, что улучшит качество очищаемой воды. Основным методом повышения качества очистки вредных выбросов предприятиям при рыночной экономике является система штрафов, а также система плат за пользование очистными сооружениями. В настоящее время из общего количества сточных вод механической очистки подвергается 68% всех стоков, физико-химической- 3%, биологической - 29%. В перспективе предполагается повысить долю очистки биологическим методом до 80%, что улучшит качество очищаемой воды. Основным методом повышения качества очистки вредных выбросов предприятиям при рыночной экономике является система штрафов, а также система плат за пользование очистными сооружениями.

Исследование качества питьевой воды в г. Краснодаре Объектом исследования выбрана вода микрорайон Комсомольский, Юбилейный, Черёмушки. Задачи исследования: – знакомство с теорией по данной проблеме; – проведение экологического мониторинга состояния питьевой воды в выбранных районах; – выявление основных загрязнителей воды; – установление соответствия качества питьевой воды санитарным нормам; – сопоставление качества исследуемой воды; – определение химических показателей дополнительно очищенной воды; – составление таблиц и графиков по данному материалу

Органолептические показатели воды. Содержание взвешенных частиц. Этот показатель качества воды определяется фильтрованием воды через бумажный фильтр и последующим высушиванием осадка на фильтре в сушильном шкафу до постоянной массы. Для анализа берется 500 мл. воды. Фильтр перед работой взвешивается. После фильтрования осадок с фильтром высушивается до постоянной массы при 105 С, охлаждается в эксикаторе и взвешивается. Весы должны обладать высокой чувствительностью, лучше использовать аналитические весы. Содержание взвешенных веществ в мг/л в испытуемой воде определяется по формуле: (m1 – m2) • 1000/V, где m1 – масса бумажного фильтра с осадком взвешенных частиц, г; m2 – масса бумажного фильтра до опыта, г; V – объем воды для анализа, л. ПДК = 10мг/г.

Цвет (окраска) При загрязнении водоема стоками промышленных предприятий вода может иметь окраску, не свойственную цветности природных вод. Для источников хозяйственно-питьевого водоснабжения окраска не должна обнаруживаться в столбике высотой 20 см, для водоемов культурно-бытового назначения – 10 см. Диагностика цвета – один из показателей состояния водоема. Для определения цветности воды используется стеклянный сосуд и лист белой бумаги. В сосуд набирается вода и на белом фоне бумаги определяется ее цвет (голубой, зеленый, серый, желтый, коричневый) – показатель определенного вида загрязнения.

Прозрачность Прозрачность воды зависит от нескольких факторов: количества взвешенных частиц ила, глины, песка, микроорганизмов, содержания химических соединений. Для определения прозрачности воды используется прозрачный мерный цилиндр с плоским дном, в который наливается вода, подкладывается под цилиндр на расстоянии 4 см от его дна шрифт, высота букв которого 2 мм, а толщина линий букв – 0,5 мм, и сливается вода до тех пор, пока сверху через слой воды не будет виден этот шрифт. Измеряется высота столба оставшейся воды линейкой и выражается степень прозрачности в сантиметрах. При прозрачности воды менее 3 см водопотребление ограничивается. Уменьшение прозрачности природных вод свидетельствует об их загрязнении.

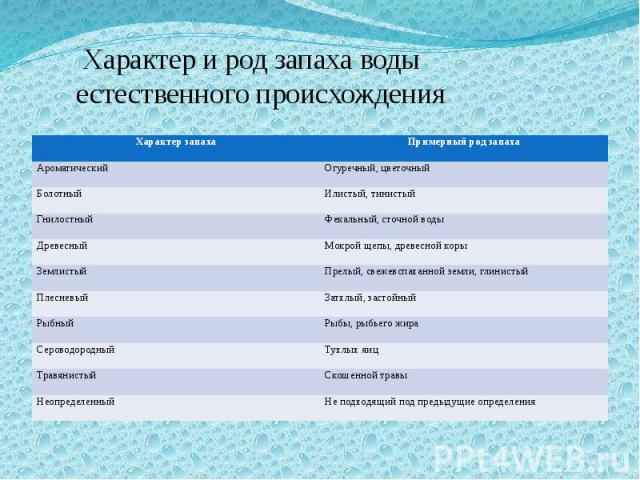
Запах Запах воды обусловлен наличием в ней пахнущих веществ, которые попадают естественным путем и со сточными водами. Запах воды водоемов, обнаруживаемый непосредственно в воде или (водоемов хозяйственно-питьевого назначения) после ее хлорирования, не должен превышать 2 баллов. Определение основано на органолептическом исследовании характера и интенсивности запахов воды при 20 ˚ и 60˚С.

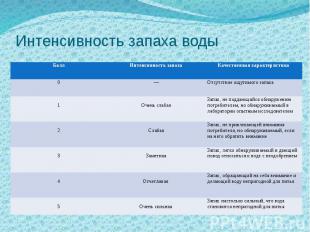
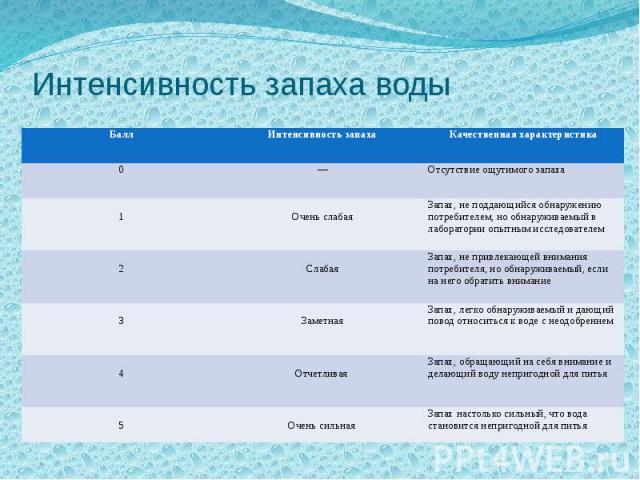
Интенсивность запаха воды
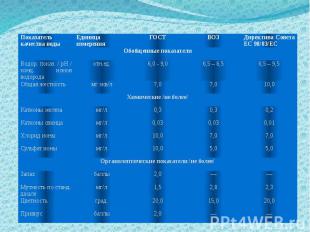

Определение качества воды методами химического анализа. Водородный показатель (pH). Питьевая вода должна иметь нейтральную реакцию (pH около 7). Значение pH воды водоемов хозяйственного, питьевого, культурно-бытового назначения регламентируется в пределах 6,5 – 8,5. Оценивать значение pH можно разными способами. 1. Приближенное значение pH определяют следующим образом. В пробирку наливают 5 мл исследуемой воды, 0,1 мл универсального индикатора, перемешивают и по окраске раствора определяют pH: розово-оранжевая – pH около 5; светло-желтая – 6; зеленовато-голубая – 8. 2. Можно определить pH с помощью универсальной индикаторной бумаги, сравнивая ее окраску со шкалой.

Жесткость воды Различают общую, временную и постоянную жесткость воды. Общая жесткость обусловлена главным образом присутствием растворимых соединения кальция и магния в воде. Временная жесткость иначе называется устранимой или карбонатной. Она обусловлена наличием гидрокарбонатов кальция и магния. Постоянная (некарбонатная) жесткость вызвана присутствием других растворимых солей кальция и магния. Общая жесткость варьирует в широких пределах в зависимости от типа пород и почв, слагающих бассейн водосбора, а также от сезона года. Значение общей жесткости в источниках централизованного водоснабжения допускается до 7 ммоль • экв./л, в отдельных случаях по согласованию с органами санитарно – эпидемиологической службы – до 10 ммоль • экв./л. При жесткости до 4 ммоль • экв./л вода считается мягкой, 4 – 8 ммоль • экв./л – средней жесткости, 8 – 12 ммоль • экв./л – жесткой, более 12 ммоль • экв./л – очень жесткой. Методами химического анализа обычно определяют жесткость общую (Жо) и карбонатную (Жк), а некарбонатную (Жн) рассчитывают как разность Жо – Жк.

Обнаружение катионов свинца. Реагент: хромат калия (10 г K2CrO4 растворить в 90 мл H2O). Условия проведения реакции 1. pH = 7,0. 2. Температура комнатная. 3. Осадок нерастворим в воде, уксусной кислоте и аммиаке. Выполнение анализа В пробирку помещают 10 мл пробы воды, прибавляют 1 мл раствора реагента. Если выпадает желтый осадок, то содержание катионов свинца более 100 мг/л: Pb2+ + CrO2- = PbCrO4 жёлтый

Обнаружение катионов железа. Реагенты: тиоцианат аммония (20 г NH4CNS растворить в дистиллированной воде и довести до 100 мл); азотная кислота (конц.); перекись водорода (ω (%) = 5 %). Условия проведения реакции 1. pH 3,0 2. Температура комнатная. 3. Действием пероксида водорода ионы Fe (II) окисляют до Fe (III). Выполнение анализа К 10 мл пробы воды добавляют 1 каплю азотной кислоты, затем 2 – 3 капли пероксида водорода и вводят 0,5 мл тиацианата аммония. При концентрации ионов железа более 2,0 мг/л появляется розовое окрашивание, при концентрации более 10 мг/л окрашивание становится красным: Fe3+ + 3CNS– = Fe(CNS)3 красный

Обнаружение хлорид – ионов. Реагенты: нитрат серебра (5 г AgNO3 растворить в 95 мл воды); азотная кислота (1:4). Условия проведения реакции 1. pH 7,0 2. Температура комнатная. Выполнение анализа К 10 мл пробы воды прибавляют 3 – 4 капли азотной кислоты и приливают 0,5 мл раствора нитрата серебра. Белый осадок выпадает при концентрации хлорид – ионов более 100 мг/л: Cl– + Ag+ = AgCl белый

Обнаружение сульфат – ионов. Реагент: хлорид бария (10 г BaCl2 x 2H2O растворить в 90 г H2O); соляная кислота (16 мл HCl (p = 1,19) растворить в воде и довести объем до 100мл). Условия проведения реакции 1. pH 7,0. 2. Температура комнатная. 3. Осадок нерастворим в азотной и соляной кислотах. Выполнение анализа. К 10 мл пробы воды прибавляют 2 – 3 капли соляной кислоты и приливают 0,5 мл раствора хлорида бария. При концентрации сульфат – ионов более 10 мг/л выпадает садок: Ba2+ + SO42- = BaSO4 белый

Проведено исследование питьевой воды Проведено исследование питьевой воды в следующих точках города: – М.-Н. Юбилейный – М.-Н Комсомольский – М.-Н. Черёмушки
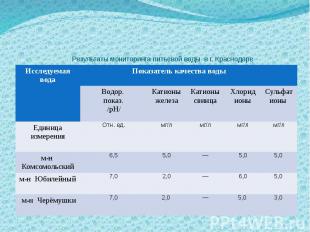
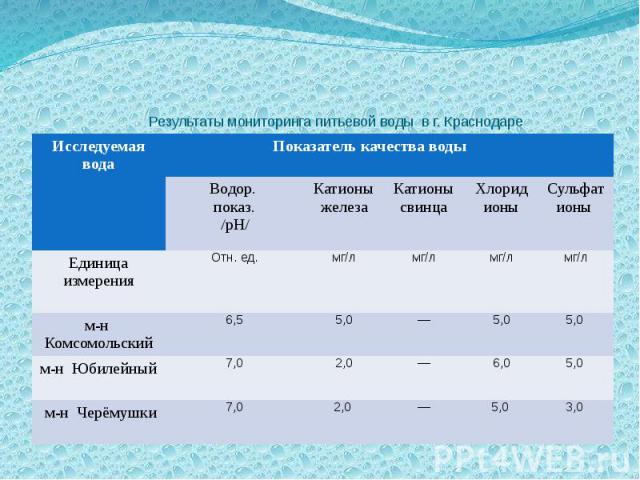
Результаты мониторинга питьевой воды в г. Краснодаре
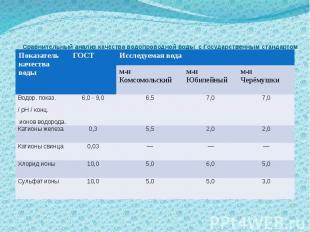
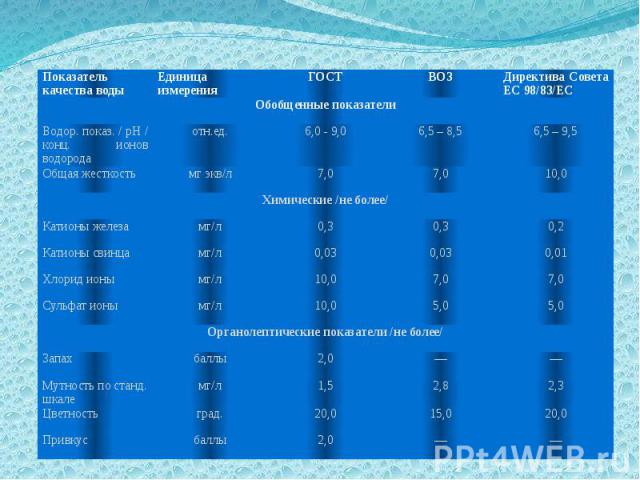
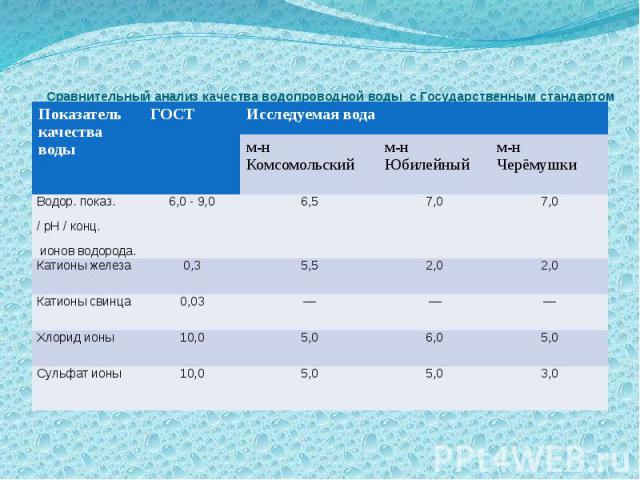
Сравнительный анализ качества водопроводной воды с Государственным стандартом
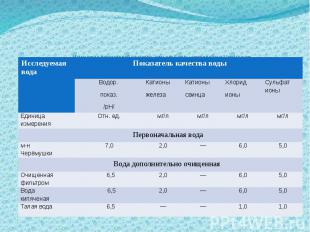
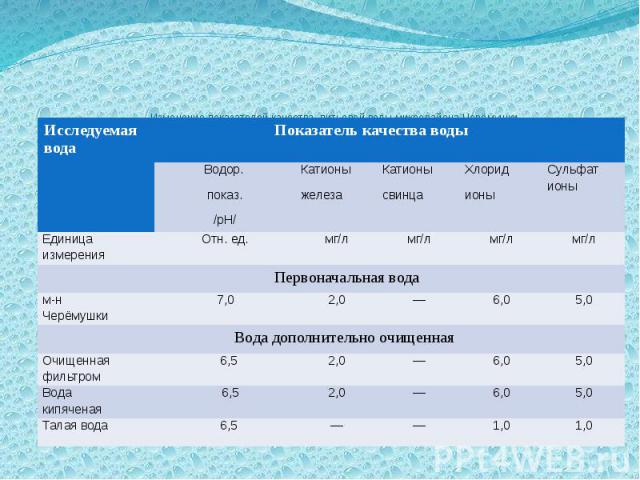
Изменение показателей качества питьевой воды микрорайона Черёмушки в результате дополнительной обработки

В результате исследований я выяснил, что в воде, прошедшей дополнительную обработку фильтром и кипячением, снижается кислотность. Наиболее очищенной явилась талая вода, уменьшилось содержание хлорид и сульфат ионов, катионы железа в талой воде не обнаруживаются. В результате исследований я выяснил, что в воде, прошедшей дополнительную обработку фильтром и кипячением, снижается кислотность. Наиболее очищенной явилась талая вода, уменьшилось содержание хлорид и сульфат ионов, катионы железа в талой воде не обнаруживаются.

Выводы из проведенного исследования качества питьевой воды г. Краснодара можно сделать следующие выводы: 1. Качество питьевой воды по органолептическим и большинству химических показателей соответствует нормам Всемирной Организации Здравоохранения (ВОЗ), Европейского сообщества (ЕС) и Государственного стандарта (ГОСТ). 2. Питьевая вода нашей местности является водой средней жесткости, однако водопроводная вода мягче природной. 3. При движении по многокилометровым магистралям из чугунных и стальных труб, подверженных коррозии, в водопроводной воде повышается содержание ионов железа.

4. Рекомендуется производить дополнительную обработку питьевой воды 4. Рекомендуется производить дополнительную обработку питьевой воды непосредственно на месте потребления: а) отстаивание водопроводной воды; при этом улетучивается остаточный свободный хлор, который применяют для обеззараживания воды. б) кипячение воды; основное предназначение процесса кипячения – обеззараживание воды и снижение карбонатной жесткости. в) вымораживание воды; считается, что такая вода самая чистая, лучше проникает через биологические мембраны, быстрее выводится из организма экскреторными органами. г) фильтрование; фильтры уменьшают ее жесткость и содержание свободного хлора. 5. Подземные воды являются основным источником питьевой воды в нашей местности, они гораздо ценнее по качеству и наиболее надежны в санитарном отношении.

ЛИТЕРАТУРА: 1. Алексеев С.В., Груздева Н.В., Муравьев А.Г., Гущина Э.В. Практикум по экологии: учебное пособие. Москва, Издательство АО МДС, 1998г. 2. Ашихмина Т.Я Школьный экологический мониторинг. Издательство «Агар», 2000 г. 3. Браун Т., Лемей Г. Химия – в центре наук. Пер. с англ. Москва «Мир», 1983 г. 4. Мигунов Л.Н., Мигунова М.И. Природа и общество. г. Старый Оскол, 2000 г. 5. Муравьев А.Г. Руководство по определению показателей качества воды полевыми методами. – СПб.: Крисмас +, 1999 г. 6. Небел Б. Наука об окружающей среде. Пер. с англ. – М., «Мир», 1993 г. 7. Новиков Ю.В. и др. Методы исследования качества воды водоемов. – М.: Медицина, 1990 г. 8. Паус К.Ф. Основы промышленной экологии г. Белгород, 2001 г.

Интернет ресурсы: http://www.physicon. http://www.hemi.wallst.ru http://picanal.narod.ru/ http://www.hemi.wallst.ru/ http://www.alhimik.ru/ http://www.chem.msu.su/ http://www.cnit.msu.ru/