Презентация на тему: Теллур

«Теллур»

Теллур Теллур (лат. Tellurium) — это химический элемент с атомным номером №52 в периодической системе и атомным весом 127,60; обозначается символом Te, относится к семейству металлоидов. В природе встречается в виде восьми стабильных изотопов с массовыми числами 120, 122—126, 128, 130, из которых наиболее распространены 128Тe и 130Тe. Из искусственно полученных радиоактивных изотопов широкое применение в качестве меченых атомов имеют 127Тe и 129Te .

Из истории… Впервые был найден в 1782 году в золотоносных рудах Трансильвании горным инспектором Францом Иозефом Мюллером (впоследствии барон фон Рейхенштейн), на территории Австро-Венгрии. В 1798 году Мартин Генрих Клапрот выделил теллур и определил важнейшие его свойства. Первые систематические исследования химии теллура выполнены в 30-х гг. 19 в. И. Я. Берцелиусом.

"Аурум парадоксум" - парадоксальное золото, так называли теллур, после того как в конце XVIII столетия он был открыт Рейхенштейном в соединении с серебром и желтым металлом в минерале сильваните. Неожиданным явлением казался факт, когда золото, обычно всегда встречающееся в самородном состоянии, было обнаружено в соединении с теллуром. Вот почему, приписав свойства, подобные желтому металлу, его назвали желтым металлом парадоксальным.

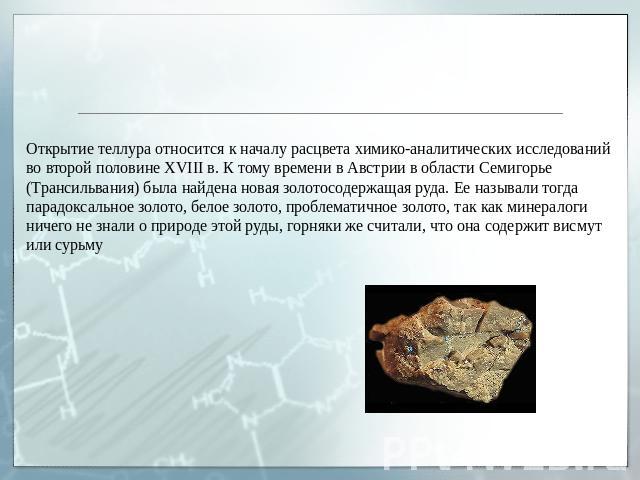
Открытие теллура относится к началу расцвета химико-аналитических исследований во второй половине XVIII в. К тому времени в Австрии в области Семигорье (Трансильвания) была найдена новая золотосодержащая руда. Ее называли тогда парадоксальное золото, белое золото, проблематичное золото, так как минералоги ничего не знали о природе этой руды, горняки же считали, что она содержит висмут или сурьму

В 1782 г. Мюллер исследовал руду и выделил из нее, как он полагал, новый металл. Чтобы удостовериться в своем открытии, Мюллер послал пробу "металла" шведскому химику-аналитику Бергману. Бергман, тогда уже тяжело больной, начал исследование, но успел установить лишь то, что новый металл отличается по химическим свойствам от сурьмы. Последовавшая вскоре смерть Бергмана прервала исследования и, прошло более 16 лет, прежде чем они возобновились. Тем временем в 1786 г. профессор ботаники и химии университета в Пеште Китаибель выделил из минерала верлита (содержащего теллуриды серебра, железа и висмута) какой-то металл, который он счел до тех пор неизвестным. Китаибель составил описание нового металла, но не опубликовал его, а лишь разослал некоторым ученым. Так оно попало к венскому минералогу Эстнеру, который познакомил с ним Клапрота. Последний дал благоприятный отзыв о работе Китаибеля, но существование нового металла пока еще не было окончательно подтверждено. Клапрот продолжил исследования Китаибеля и в результате их полностью устранил всякие сомнения. В январе 1798 г. он выступил с сообщением перед Берлинской академией наук об открытии им в трансильванском "белом желтом металле" особого металла, который получен «от матери земли». И действительно, первые десятилетия XIX в. теллур причисляли к металлам. В 1832 r. Берцелиус обратил внимание на сходство теллура с селеном и серой (на что делались указания и раньше), после чего теллур причислили к металлоидам (по номенклатуре Берцелиуса)
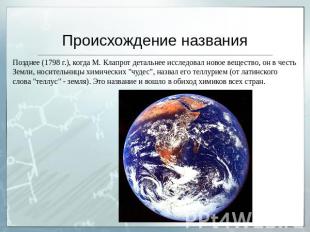
Происхождение названия Позднее (1798 г.), когда М. Клапрот детальнее исследовал новое вещество, он в честь Земли, носительницы химических "чудес", назвал его теллурием (от латинского слова "теллус" - земля). Это название и вошло в обиход химиков всех стран.

Нахождение в природе Содержание в земной коре 1·10-6 % по массе. Металлический теллур можно встретить разве что в лаборатории, но его соединения можно найти вокруг нас гораздо чаще, чем может показаться. Известно около 100 минералов теллура. Важнейшие из них: алтаит PbTe, сильванит AgAuTe4, калаверит AuTe2, тетрадимит Bi2Te2S, креннсрит AuTe2, петцит AgAuТе2. Встречаются кислородные соединения теллура, например ТеО2 — теллуровая охра. Встречается самородный теллур и вместе с селеном и серой (японская теллуристая сера содержит 0,17 % Те и 0,06 % Se).

модуль Пельтье Многие знакомы с термоэлектрическими модулями Пельтье, которые используют в портативных холодильниках, термоэлектрических генераторах и иногда для экстремального охлаждения компьютеров. Основной материал полупроводников в таких модулях это теллурид висмута. В настоящее время это самый ходовой полупроводниковый материал.Если посмотреть сбоку на термоэлектрический модуль, можно заметить ряды маленьких «кубиков».

Физические свойства Теллур серебристо-белого цвета с металлическим блеском, хрупок, при нагреве становится пластичным. Кристаллизуется в гексагональной системе. Теллур - полупроводник. При обычных условиях и вплоть до температуры плавления чистый Теллур имеет проводимость p-типа. С понижением температуры в интервале (-100 °С) - (-80 °С) происходит переход: проводимость Теллура становится n-типа. Температура этого перехода зависит от чистоты образца, и она тем ниже, чем чище образец. Плотность = 6,24 г/см³ Температура плавления = 450°C Температура кипения = 990°C Теплота плавления = 17,91 кДж/моль Теплота испарения = 49,8 кДж/моль Молярная теплоемкость = 25,8 Дж/(K·моль) Молярный объем = 20,5 см³/моль

Химические свойства Теллур – неметалл. В соединениях теллур проявляет степени окисления: -2, +4, +6 (валентность II, IV, VI). Химически теллур менее активен, чем сера и кислород. Теллур устойчив на воздухе, но при высокой температуре горит с образованием двуокиси TeO2. С галогенами Те взаимодействует на холоде. При нагревании реагирует со многими металлами, давая теллуриды. Растворим в щелочах. При действии азотной кислоты Те превращается в теллуристую, а при действии царской водки или 30%-ной перекиси водорода – в теллуровую кислоту.

Физиологическое действие При нагревании Теллур взаимодействует с водородом с образованием теллуроводорода - H2Te бесцветного ядовитого газа с резким, неприятным запахом. Теллур и его летучие соединения токсичны. Попадание в организм вызывает тошноту, бронхиты, пневмонию. Предельно допустимая концентрация в воздухе колеблется для различных соединений 0,007—0,01 мг/м³, в воде 0,001—0,01 мг/л.

Получение Основной источник — шламы электролитического рафинирования меди и свинца. Шламы подвергают обжигу, теллур остается в огарке, который промывают соляной кислотой. Из полученного солянокислого раствора теллур выделяют, пропуская через него сернистый газ SO2. Для разделения селена и теллура добавляют серную кислоту. При этом выпадает диоксид теллура ТеО2, а H2SeO3 остается в растворе. Из оксида ТеО2 теллур восстанавливают углем. Для очистки теллура от серы и селена используют его способность под действием восстановителя (Al) в щелочной среде переходить в растворимый дителлурид динатрия Na2Te2: 6Te + 2Al + 8NaOH = 3Na2Te2 + 2Na[Al(OH)4]. Для осаждения теллура через раствор пропускают воздух или кислород: 2Na2Te2 + 2H2O + O2 = 4Te + 4NaOH. Для получения теллура особой чистоты его хлорируют Te + 2Cl2 = TeCl4. Образующийся тетрахлорид очищают дистилляцией или ректификацией. Затем тетрахлорид гидролизуют водой: TeCl4 + 2H2O = TeO2 + 4HCl, а образовавшийся ТеО2 восстанавливают водородом: TeO2 + 4H2 = Te + 2H2O.

Цены Теллур — редкий элемент, и значительный спрос при малом объёме добычи определяет высокую его цену (около 200—300 долл. за кг в зависимости от чистоты), но, несмотря на это, диапазон областей его применения постоянно расширяется.

Применение Сплавы с повышенной прочностью Термоэлектрические материалы Узкозонные проводники Производство резины Источник света СD-RW В керамике

Использованные материалы http://forexaw.com Энциклопедия школьника «Неорганическая химия»