Презентация на тему: Физические и химические явления. Химические уравнения

Физические и химические явления. Химические уравнения Составил: учитель химии МОУ «Бурханкульская ООШ» Кулешова С.Е.

Содержание 1. Химические и физические явления 2. Признаки протекания химических реакций 3. Условия протекания химических реакций 4. Закон сохранения масс 5. Уравнения химических реакций

«Ах сколько нам открытий чудных готовит просвещенья дух» А.С.Пушкин Задачи : Повторить признаки и условия течения химических реакций Выяснить , что называется химическим уравнением Научить составлять химические уравнения

Химические и физические явления Физические явления Химический состав молекул не меняется Кристаллизация Плавление Фильтрация Отстаивание Перегонка Химические явления Химический состав молекул изменяется Изменяются физические свойства веществ ( цвет, запах, агрегатное состояние, электропроводность, теплопроводность, упругость, пластичность и т.д.)

Признаки протекания химической реакции Появление запаха Выделение осадка Выделение газа Изменение цвета Выделение тепла (экзотермическая реакция) Поглощение тепла (эндотермическая реакция)

Проверь себя! В каком случае произошла химическая реакция? Почему вы так думаете? В крепко заваренный чай добавили дольку лимона Осадок в ведре с водой В негашеную известь добавили воды В печке сгорел уголь

Условия протекания химических реакций Чистота веществ (минимум примесей) Пропорциональность веществ по массе Пример:Ar (S)=32, Ar (Fe) = 56 S : Fe = 32 : 56 = 4 : 7 Для проведения реакции между серой и железом надо взять четыре части серы и семь частей железа ( 12г серы и 21г железа) Задание : В какой пропорциональности надо взять углерод и кислород для протекания химической реакции? Решение : Ar (O) = 16, Ar (C)= 12, О : С = 16 : 12 = 4 : 3 Ответ : в отношении 4:3

3. Тщательное перемешивание 4. Применение катализатора Катализатор - Вещества, которые изменяют скорость химической реакции, оставаясь к концу её неизменными 5. Площадь соприкосновения реагирующих веществ

Михаил Васильевич Ломоносов 1711-1765 гг. Создатель многих химических производств в России (неорганических пигментов, глазурей, стекла, фарфора). Изложил в 1741-1750 гг. основы своего атомно-корпускулярного учения, выдвинул кинетическую теорию теплоты. Первым из русских академиков написал учебники по химии и металлургии. Основатель Московского Университета Антуан Лоран Лавуазье 1743-1794 гг. Французский химик. Один из основоположников классической химии. Ввел в химию строгие количественные методы исследования. Доказал сложный состав атмосферного воздуха. Правильно объяснив процессы горения и окисления, создал основы кислородной теории. Заложил основы органического анализа. В 1756 г М.В. Ломоносов открыл закон сохранения масс. Позднее А.Л. Лавуазье подтвердил правильность этого закона Масса веществ, вступивших в реакцию, равна массе веществ , получившихся в результате её
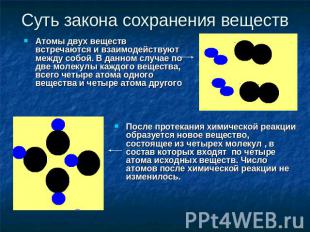
Суть закона сохранения веществ Атомы двух веществ встречаются и взаимодействуют между собой. В данном случае по две молекулы каждого вещества, всего четыре атома одного вещества и четыре атома другого После протекания химической реакции образуется новое вещество, состоящее из четырех молекул , в состав которых входят по четыре атома исходных веществ. Число атомов после химической реакции не изменилось.

Проверь себя! Сколько атомов каждого элемента потребовалось для получения молекулы оксида алюминия и трех молекул сернистой кислоты. Молекула оксида алюминия : 2 атома алюминия и 3 атома кислорода 3 атома серы, 6 атомов водорода и 9 атомов кислорода

Для получения сульфида железа смешали 36 г серы и железо, в результате реакции получили 99 г соли . Сколько грамм железа взяли для этой реакции? 63г железа

Химические уравнения Химическим уравнением называется условная запись химической реакции с помощью химических формул и математических знаков 2 Н2О = 2Н2 + О2 коэффициенты индексы 4Al + 3O2 = 2Al2O3

Алгоритм составления химического уравнения В левой части уравнения записывают формулы веществ, вступивших в реакцию, соединяют их знаком «+», в правой части уравнения записывают формулы(формулу) образующихся веществ, также с помощью знака «+». Между уравнениями ставят стрелку CuCl2 + Al AlCl3 + Cu Находим и расставляем коэффициенты к формулам так, чтобы число атомов одинаковых элементов в левой и правой частях уравнения были одинаковы. Заменяем стрелку знаком «=» . 3CuCl2 + 2Al = 2 AlCl3 + 3Cu Меди : с правой стороны 3 и с левой 3 хлора : 6 и 6 Алюминия: 2 и 2

Попробуйте свои силы Расставьте коэффициенты в уравнениях P+O2 P2O5 4P + 5O2 = 2P2O5 Al + H2SO4 Al2(SO4)3 + H2 2Al + 3H2SO4 = Al2(SO4)3 + 3H2 САМОСТОЯТЕЛЬНО S + O2 SO3 Na + H2O NaOH + H2 MgCO3 + Al Al2(CO3)3 + Mg Проверь ! 2S +3O2 = 2SO3 2Na + 2H2O = 2NaOH + H2 3MgCO3 + 2Al = Al2(CO3)3 + 3Mg