Презентация на тему: Ионизирующие излучения и радиационная защита


Ионизирующие излучения - излучения, которые создаются при радиоактивном распаде, ядерных превращениях, торможении заряженных частиц в веществе и образуют при взаимодействии со средой ионы разных знаков.

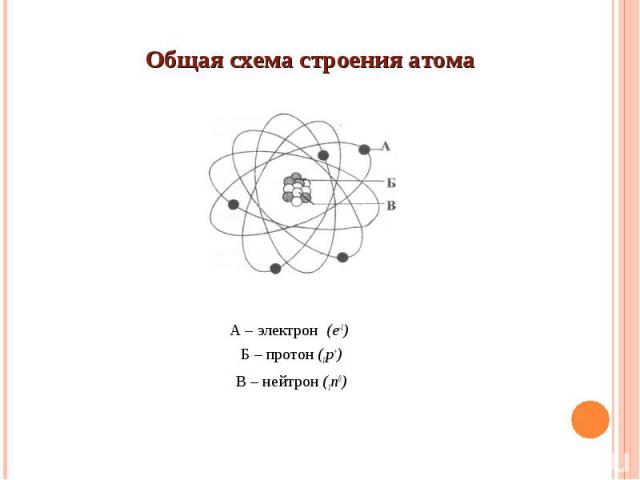
А – электрон (e-1) Б – протон (1р+) В – нейтрон (1n0)

Атомное ядро представляет собой совокупность ядерных частиц – нуклонов, к которым относятся положительно заряженные протоны и электрически нейтральные нейтроны. Атомное ядро представляет собой совокупность ядерных частиц – нуклонов, к которым относятся положительно заряженные протоны и электрически нейтральные нейтроны. Самое простое строение имеет ядро водорода, которое состоит только из одного протона.

Протон (1р+) – стабильная положительно заряженная элементарная ядерная частица с зарядом +1 (= 1,6·10-19 Кл*) и массой 1 а.е.м.**. _________ * Кл – Кулон – единица измерения элементарного заряда (количества электричества) заряженных частиц. 1 Кл равен количеству электричества, проходящему через поперечное сечение при токе силой 1А за время 1 с.

Международная система единиц (СИ) была принята XI Генеральной конференцией по мерам и весам (Париж, 1960). Международная система единиц (СИ) была принята XI Генеральной конференцией по мерам и весам (Париж, 1960). Ей было присвоено краткое наименование SI (system international), в русской транскрипции СИ, т.е. Система Интернациональная. В нашей стране она была введена как обязательная к применению в 1981 году (ГОСТ 8.417-81). Другие, существовавшие ранее системы измерения (СГС, МКС, МКГСС и т.д.) должны быть изъяты из применения.
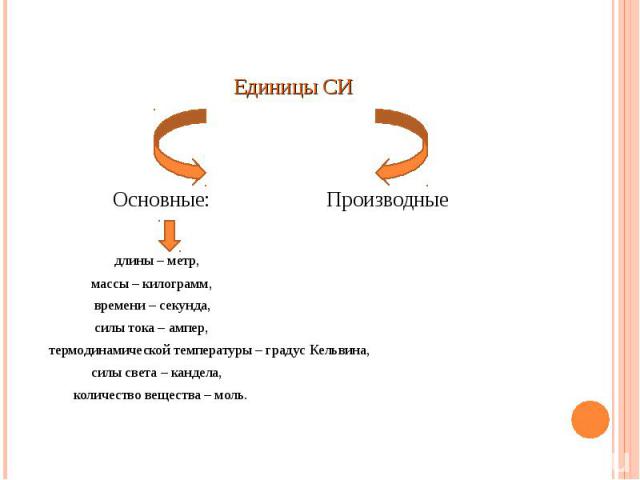
Единицы СИ Единицы СИ Основные: Производные длины – метр, массы – килограмм, времени – секунда, силы тока – ампер, термодинамической температуры – градус Кельвина, силы света – кандела, количество вещества – моль.

Десятичные кратные и дольные единицы: Десятичные кратные и дольные единицы: 1012 – тера ( T / T); 10-1 – деци ( d / д); 109 – гига ( G / Г); 10-2 – санти ( с / с); 106 – мега ( М / М); 10-3 – милли ( m / м); 103 – тера ( k / к); 10-6 – микро ( µ / мк); 102 – гекто ( h / г); 10-9 – нано ( n / н); 10 – дека ( da / да); 10-12 – пико ( р / п);

____________ ____________ ** Масса частицы, ядра, атома измеряется в системе СИ в килограммах (кг). Однако в ядерной физике для ее измерения допускается применение, наравне с единицей СИ, относительной величины получившей название – атомная единица массы (а. е. м.). 1 а. е .м. = 1 условной единице (у.е.) = 1/12 массы атома углерода = 1,66 · 10-24 г.

Число протонов в ядре: Число протонов в ядре: - строго постоянно для атомов одного элемента, - соответствует номеру химического элемента в Периодической системе Д.И. Менделеева, - определяет заряд ядра (Z), - количество электронов вращающихся вокруг ядра, - химические свойства элемента. Находясь вне ядра, протоны сохраняют стабильность и не испытывают превращений.

Нейтрон (1n0) – электрически нейтральная ядерная частица с массой, близкой массе протона (1 а.е.м.). Нейтрон (1n0) – электрически нейтральная ядерная частица с массой, близкой массе протона (1 а.е.м.). - в ядрах стабильны, - в свободном состоянии неустойчивы и распадаются на протон и электрон, испуская и антинейтрино, а также некоторое количество энергии (0,78 МэВ*).

_____________ _____________ * Электрон-вольт (эВ) – единица энергии, используемая в ядерной физике (хотя данная единица является внесистемной, ее применение допускается к применению наравне с единицами СИ). Равна энергии, которую получает электрон, проходя через поле с разностью потенциалов в 1 В. 1 эВ = 1,6 · 10-19 Дж. В практике широко используют кратные единицы: МэВ – мегаэлектрон-вольт, кэВ – килоэлектрон-Вольт и др.

Масса ядра атома химического элемента (М) равна сумме масс протонов и нейтронов входящих в его состав: М = 1р+ + 1n0

Электрон (e-1) – отрицательно заряженная частица с зарядом -1 и массой ≈ 0. Электрон (e-1) – отрицательно заряженная частица с зарядом -1 и массой ≈ 0. - Электроны вращаются вокруг ядра по орбитам. - Группируются в несколько электронных слоев (К, L, М и т.д.) , образуя электронную оболочку ядра (электронное облако). - Количество электронных слоев определяет положение химического элемента в одном из семи периодов периодической системы и соответствует его номеру. - Электроны в каждом слое имеют свой уровень энергии, однако в определенных условиях возможен перескок отдельных электронов с орбиты на орбиту с поглощением или выделением энергии.

Атомы, имеющие определенный состав и структуру ядра, называются нуклидами. Атомы, имеющие определенный состав и структуру ядра, называются нуклидами. - Индивидуальные свойства нуклида определяются электрическим зарядом ядра (числом протонов). Поэтому химические элементы обозначаются следующим образом: ZXA, где Х – химический элемент, Z – заряд ядра (число протонов), А – масса атома.

Изотопы (isos – одинаковый, topos - место) – разновидности химического элемента с одинаковым числом протонов, но различным числом нейтронов в атомных ядрах и, следовательно, атомной массой, сохраняя при этом практически одинаковые химические свойства. Изотопы (isos – одинаковый, topos - место) – разновидности химического элемента с одинаковым числом протонов, но различным числом нейтронов в атомных ядрах и, следовательно, атомной массой, сохраняя при этом практически одинаковые химические свойства. - В Периодической системе Д.И. Менделеева изотопы одного химического элемента занимают одно место (клеточку).

- Изотопы одного и того же элемента имеют разные массовые числа. Например, природный хлор состоит из двух видов атомов, в ядрах которых содержится по 18 или 20 нейтронов, при постоянном количестве протонов – по 17 (17Cl35 и 17Cl37). !! Масса большинства химических элементов выражаются не целыми числами. Например, масса хлора равна 35,5. Это объясняется тем, что соотношение природных изотопов хлора 17Cl35 и 17Cl37 составляет 75,4 % и 24,6 % соответственно.

Если число протонов в ядре совпадает с числом электронов, то атом в целом оказывается электрически нейтральным. Если число протонов в ядре совпадает с числом электронов, то атом в целом оказывается электрически нейтральным. Если атом обладает некоторым положительным или отрицательным зарядом, то называется ионом, например Li+, Li2+ или О-, О2-.

Ионизация атома – процесс, в котором один или более электронов освобождаются от материнского атома или молекулы, или из другого связанного состояния. Ионизация атома – процесс, в котором один или более электронов освобождаются от материнского атома или молекулы, или из другого связанного состояния. Обратный процесс нейтрализации атома из двух разнополярных ионов называется рекомбинацией. В случае передачи недостаточной для ионизации энергии электрон может переходить на более удаленную от ядра орбиту, в этом случае атом называется возбужденным.