Презентация на тему: Энергия топлива

МОУ Паршиковская СОШФизика 8 класс Тема урока: "Энергия топлива"Учитель физики: Воротынцева Надежда АлексеевнаКонкурс "Победим пожары" 2007МОУ Паршиковская СОШ


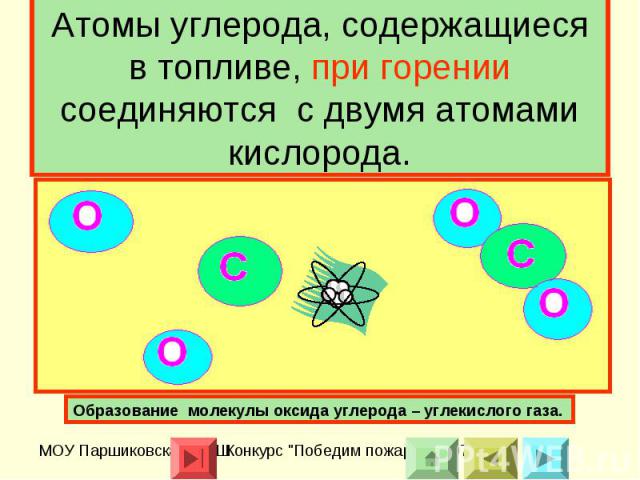
Человек использует топливо именно для того, чтобы потреблять выделяемую энергию. Молекула воды состоит из двух атомов водорода и одного атома кислорода, чтобы разделить её на атомы надо преодолеть силы притяжения между атомами, т.е. совершить работу, другими словами затратить некоторую энергию. При сжигании топлива происходит обратный процесс, процесс образования молекул из атомов, значит, энергия должна выделятся.

Процесс горения топлива человечество использует в разных областях деятельности: тепловые двигатели (сгорание топлива );тепловые электростанции (сгорание топлива);обогрев жилища, приготовление пищи и др.в промышленности (работа доменных печей) и т.д.
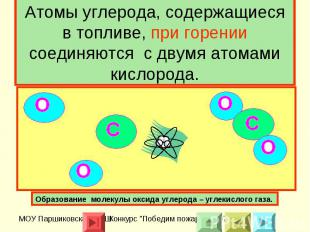
Атомы углерода, содержащиеся в топливе, при горении соединяются с двумя атомами кислорода. Образование молекулы оксида углерода – углекислого газа.

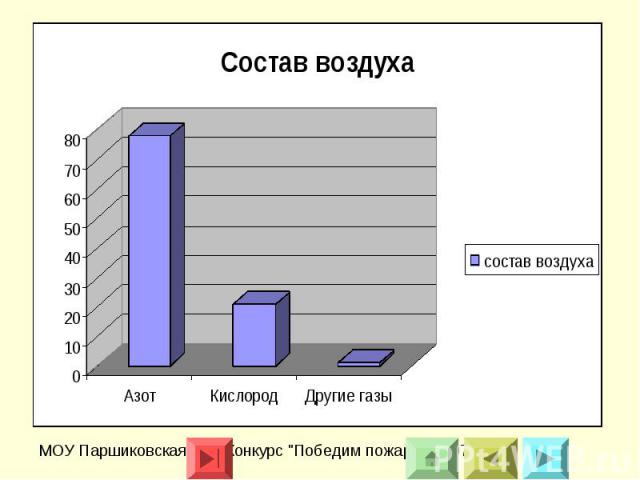
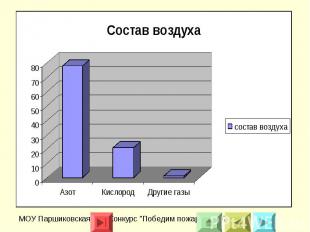
Горение это физико-химический процесс, для которого характерны три признака: химическое превращение, выделение тепла, излучение света. Очень часто окислителем является кислород (могут быть и другие вещества: хлор, сера, бром и кислородосодержащие вещества). Однако чаще всего приходится иметь дело с горением в атмосфере воздуха, при этом окислителем является кислород. Состав воздуха мы знаем: 78% - азота, 21% - кислорода и 1 % других газов.

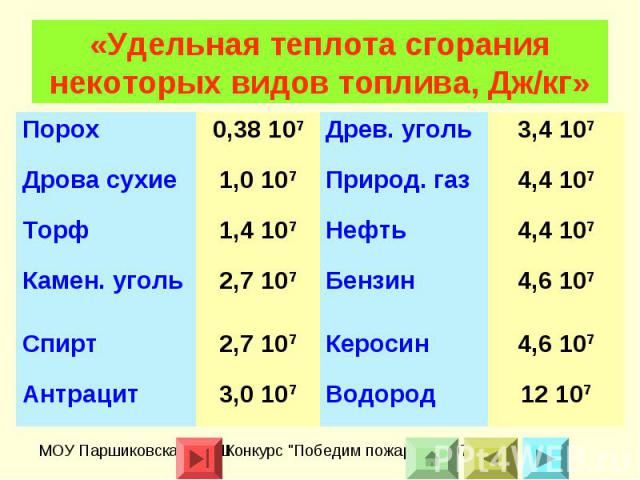
Физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой 1 кг, называется удельной теплотой сгорания топлива.Удельная теплота сгорания обозначается буквой q. Единицей удельной теплоты сгорания является 1Дж/кг.

Общее количество теплоты Q (Дж), выделяемое при полном сгорании m (кг) топлива, вычисляется по формуле:Q=qm.
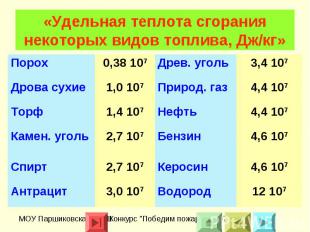
«Удельная теплота сгорания некоторых видов топлива, Дж/кг»

В жизни человек часто сталки-вается со случаями неуправ-ляемого процесса горения т.е. пожаром. Чем опасен пожар? Что мы должны знать о горении различных веществ? Как должны действовать при пожарах?

Мы должны знать, что в результате процесса горения выделяются продукты химической реакции. Вещества, входящие в состав топлива, находятся в продуктах горения и выделяются в виде соединений, например: азот выделяется в свободном виде N2 , хлор – в виде хлористого водорода HCl, а сера – в виде SO2.

Для возникновения горения необходимы определенные условия: наличие горючего вещества, окислителя и источника воспламенения. Горючее вещество и окислитель должны быть нагреты до определенной температуры источником тепла: пламенем, искрой, накаленным телом или теплом, выделяемым при какой-либо химической реакции или механической работе.

В установившемся процессе горения постоянным источником воспламенения является зона горения, т.е. область, где происходит реакция, выделяется тепло и свет.

Сгорание может быть полным и неполным. При полном сгорании образуются продукты не способные к дальнейшему горению (СО2, Н2О, НСl) при неполном – получающиеся продукты способны к дальнейшему горению (СО, Н2S, НСN, NH3 и т.д.). Признаком неполного сгорания является наличие дыма, содержащего несгоревшие частицы углерода и других веществ.

Фотография, демонстрирующая дым при пожаре нефтепродуктов.


ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ Что должен знать о процессе горения человек, чтобы мог не только использовать горение для своего блага, но и защитить себя от пожара?Какие факторы и как влияют на ход процесса горения во время пожара?Какие меры надо предпринять человеку, чтобы эффективнее потушить пожар и избежать его поражающего действия?

Темы сообщений учащихся: Состав дыма при горении различных веществ и их вред для здоровья человека, способы защиты от дыма.Основные правила пожарной безопасности при возникновении пожара в квартире.Современные средства пожаротушения.Основные правила пожарной безопасности при возникновении пожара в лесу.Как помочь человеку, который загорелся .

Домашнее задание: § 10, упражнение 5 (2,3).Учить основные правила ПБ

КОНЕЦ